
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
В-88 Квантування електронних орбіт і виникнення хімічного зв’язку в твердих тілах
Мета: ознайомитись із: 1) особливостями виникнення хімічного зв’язку в твердих тілах; 2) квантуванням значень основних характеристик електронів (енергії, дебройлівської довжини хвилі, відстані від ядра, моменту імпульсу, частоти та ін.), коли атом перебуває в різних стаціонарних станах .
Устаткування: комп’ютерна програма “Квантування електронних орбіт”.
Теоретичні відомості
Відмінність між різними типами твердих тіл зумовлена відмінністю в характері розподілу електронів і ядер в атомах і молекулах і, особливо, в характері розподілу найбільш віддалених від ядра (валентних) електронів та йонних остовів атомів.
Для вивчення того чи іншого кристалу необхідно вияснити, перш за все, просторове розташування ядер та електронів. Що ж утримує разом атоми в кристалах? Зв’язок між атомами майже повністю забезпечується силами електростатичного притягання між негативно зарядженими електронами і позитивно зарядженими ядрами.[1]
Для того щоб за допомогою сил електростатичного притягання між валентними електронами і йонними остовами утворити із атомів тверде тіло, необхідно виконати наступні чотири умови, які не завше можна сумістити одна з одною:
♦ позитивно заряджені йонні остови повинні перебувати на такій відстані одне від одного, щоб при цьому було до мінімуму зведено електростатичне (кулонівське) відштовхування між ними.
♦ валентні електрони також повинні знаходитись на певних відстанях один від одного, які відповідають попередній вимозі.
♦ в той же час валентні електрони повинні перебувати настільки близько від позитивних йонів, щоб електростатичне притягання між ними було максимальним.
♦ виконання цих трьох умов приведе до зменшення потенціальної енергії системи, однак воно повинно відбуватись таким чином, щоб кінетична енергія системи тільки незначно збільшилась.

Існування стабільних зв’язків між атомами в кристалах передбачає, що повна енергія кристала – кінетична плюс потенціальна – повинна бути меншою за повну енергію такої ж кількості вільних атомів. Різниця цих двох значень енергій називається енергією хімічного зв’язку або просто енергією зв’язку.
На рисунку 88.1 схематично показані основні типи зв’язків в кристалах.
Реалізація ван-дер-ваальсівського зв’язку продемонстровано на прикладі кристалічного аргону. Нейтральні атоми аргону (рисунок 88.1,а) утворюють кристал за рахунок слабих сил Ван-дер-Ваальса, які діють між ними і виникають в результаті флуктуацій в розподілі заряду атома.
Йонний зв’язокреалізується за рахунок сил електростатичного притягання між додатними йонами лужного металу Na+ і негативними йонами галогену Cl- (рисунок 88.1,б). Тобто атоми Натрію віддають свої валентні електрони атомам Хлору.
Металічний зв’язок продемонстровано на прикладі натрію (рисунок 88.1,в). Валентні електрони атомів лужного металу натрію покидають свої атоми і утворюють “електронну рідину”, в яку занурені позитивні йони.
Ковалентний зв’язок утворюється, коли нейтральні атоми (наприклад Карбону – рисунок 88.1,г) за рахунок перекриття (успільнення) їх електронних оболонок утворюють кристал (алмаз).
Експериментальні дослідження значення енергії зв’язку атома в кристалах свідчать, що вона складає від одного і менше відсотка від енергії йонізації електрона атома. Таким чином цієї енергії недостатньо для того, щоб сильно спотворити (збурити, деформувати) електронні оболонки атома. Тобто можна вважати, що розподіл електронів у вільних атомах незначно відрізняється від розподілу електронів в атомах кристалу (принаймні у тих, де реалізується ван-дер-ваальсівський зв’язок).
В даній роботі робиться акцент на те, щоб зрозуміти і побачити на моделі найпростішого атома, які основні властивості електронів, особливо валентних, як відбувається квантування їх основних характеристик. Для цього детально розглянемо будову найпростішого із атомів – Гідрогену. Подивимося, як електрон веде себе, коли атом перебуває в різних стаціонарних станах.
Пригадаємо, що серія дослідів Резерфорда та його учнів на початку минулого століття дали змогу Резерфорду накреслити ядерну модель атома: в центрі атома міститься позитивно заряджене ядро, розміри якого приблизно 10-15 м; навколо ядра замкнутими орбітами в просторі, обмеженому об’ємом сфери радіусом 10-10 м обертаються електрони, причому кількість їх дорівнює порядковому номеру елемента. Проте з погляду класичної фізики така модель була неспроможна пояснити закономірності в лінійчатих спектрах атомів і навіть самого факту випромінювання атомом монохроматичного світла; не могла пояснити характерної стійкості атома.
Правильні висновки з труднощів ядерної моделі Резерфорда зробив датський фізик Нільс Бор у 1913р. Він не відкинув самої моделі атома, оскільки вона ґрунтувалась на дослідних даних, але зробив сміливі припущення про те, що в мікроструктурі атома закони класичної електродинаміки не справджуються і що для з’ясування внутрішнього механізму атома треба керуватися ідеєю квантової теорії випромінювання Планка.
У пошуках загальної квантової теорії Бор сформулював постулати, в яких, зокрема, твердив, що
♦ атому властиві цілком стійкі стани з відповідним значенням енергії, перебуваючи в яких він не поглинає і не випромінює електромагнітних хвиль.
♦ цим станам відповідають певні орбіти, на яких перебувають електрони, моменти імпульсу яких квантуються:
 , (88.1)
, (88.1)
де mе – маса електрона, υт – його орбітальна швидкість, rn – радіус n-ої стаціонарної орбіти.
Ціле число n називається головним квантовим числом.
Правило квантування орбіт Бора одержало наочну інтерпретацію в теорії де Бройля, який запропонував гіпотезу про наявність в електрона хвильових властивостей (1924 р.). Згідно цієї теорії електрону (і будь-якому іншому мікрооб'єкту) відповідає хвильовий процес з довжиною хвилі
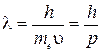 , (88.2)
, (88.2)
де p – імпульс електрона.
Застосувавши до орбітального руху електрона на стаціонарній круговій орбіті в атомі Гідрогену правила квантування Бора, отримуємо співвідношення
 |
nλ = 2πrn. (88.3)
Це означає, що довжина хвилі де Бройля ціле число раз укладається на довжині стаціонарної кругової орбіти електрона, тобто стаціонарна орбіта відповідає круговій стоячій хвилі де Бройля на довжині орбіти.
Комп'ютерна модель є якісною ілюстрацією ідеї де Бройля виникнення стоячих хвиль на стаціонарних орбітах.
Комп'ютерна модель на прикладі орбіт із квантовими числами n = 2, 3 і 4 ілюструє закономірність, якій підкоряються радіуси стаціонарних кругових орбіт в атомі Гідрогену. Відповідно до теорії Бора
rn = n2r1, (88.4)
де r1 = 5,29·10–11 м – радіус першої борівської орбіти.
Модель дозволяє, плавно змінюючи радіус, вибирати стаціонарні орбіти, на довжині яких укладається ціле число довжин хвиль де Бройля й утворюється стояча хвиля.
Слід зауважити, що теорія Бора, а слід за нею і гіпотеза де Бройля були тільки першими кроками квантового підходу до пояснення властивостей електрона і атома.
Подальший розвиток цих ідей привів до створення квантової фізики, яка відкидає поняття орбіти, а, відповідно, і радіуса орбіти. Говорять про величину ймовірності знаходження електрона на певній відстані від ядра атома в певному напрямі. А квантування моменту імпульсу та інших характеристик електронів в атомах здійснюють так:
Абсолютна величина можливих значень механічного моменту електрона:
орбітального спіну

l = 0, 1, 2, … – орбітальне s =1/2 – спінове
квантове число квантове число
Читайте також:
- L2.T4. Транспортування рідких, твердих та газоподібних речовин.
- L2.T4/1.Переміщення твердих речовин по території хімічного підприємства.
- XVII ст.). Виникнення козацтва.
- А) Поліпшення системи зворотного зв’язку.
- Аварії на хімічно-небезпечних об’єктах та характеристика зон хімічного зараження.
- Алгоритми шифрування в електронних картах
- Аналіз властивостей радіоелектронних кіл
- Аналіз причин виникнення проблеми та обґрунтування її розв’язання програмним методом
- Аналіз стану дебіторської заборгованості за термінами її виникнення
- Безпосередньо збутові ризики та причини їх виникнення
- Біохімічна гіпотеза виникнення життя.
- Біохімічні чинники виникнення втоми при виконанні короткочасних вправ максимальної і субмаксимальної потужності
| <== попередня сторінка | | | наступна сторінка ==> |
| Хід роботи | | | Абсолютна величина можливих значень |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |