
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Хід виконання роботи
1. Визначити концентрацію вихідного розчину одноосновної карбонової кислоти (мурашиної, оцтової або пропіонової - за вказівкою викладача). Для цього відібрати піпеткою зі склянки з кислотою в колбу для титрування 5 см3 розчину кислоти та відтитрувати його 0,1–молярним розчином лугу КОН в присутності індикатора – фенолфталеїну. Розчин титрувати 3 рази до одержання результатів, що співпадають між собою з точністю ± 0,2 см3. Результати титрування занести в табл. 1.1. За середнім значенням об’єму розчину лугу, витраченого на титрування, розрахувати концентрацію вихідного розчину кислоти.
Таблиця 1.1. Дані для розрахунку концентрації вихідного розчину кислоти
| Назва кислоти | Об’єм розчину лугу, витраченого на титрування, 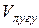 , см3 , см3
| |||
| 1 проба | 2 проба | 3 проба | Середнє значення 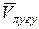
| |
Концентрація кислоти у вихідному розчині, кмоль/м3:

|
2. Приготувати п’ять розчинів кислоти різних концентрацій об’ємом 60 см3 кожний, відміряючи бюреткою в п’ять окремих колб зазначені в табл. 1.2 об’єми вихідного розчину кислоти (Vк-ти) та дистильованої води (Vводи). Розрахувати початкові концентрації кислоти  (кмоль/м3) у п’яти отриманих розчинах за рівнянням:
(кмоль/м3) у п’яти отриманих розчинах за рівнянням:
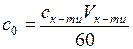 ,
,
де Vк-ти – об’єм вихідного розчину кислоти (см3) із концентрацією ск-ти, взятого для приготування розчину за табл. 1.2. Результати розрахунків записати у табл. 1.4.
Таблиця 1.2. Дані для приготування розчинів кислоти
| Номер колби | |||||
| Vк-ти , см3 | |||||
| Vводи, см3 |
3. Зважити на технічних терезах з точністю до 0,01 г 5 наважок активованого вугілля масою 1 г (або іншою масою за вказівкою викладача).
4. Висипати зважені наважки активованого вугілля в колби з приготованими розчинами. Процес адсорбції повинен тривати не менше 20 хвилин до встановлення адсорбційної рівноваги. Протягом цього часу вміст колб необхідно періодично (з інтервалом у півтори – дві хвилини) збовтувати.
5. Після встановлення рівноваги профільтрувати розчини у пронумеровані чисті колби в два етапи:
– спочатку через сухі! складані паперові фільтри пропустити перші порції розчинів (~ 1/10 всього об’єму кожного з розчинів, тобто 5¼7 см3), змочуючи таким чином фільтри. Ці перші частини фільтратів необхідно вилити, оскільки концентрація кислоти в них занижена внаслідок її адсорбції на фільтрувальному папері;
– після цього профільтрувати залишки розчинів.
6. Відтитрувати отримані фільтрати, відбираючи піпеткою з кожної колби об’єми проб, які зазначено в табл. 1.3 (для забезпечення однакової точності титрування об’єми аліквот для фільтратів із різним вмістом кислоти повинні бути різними). Титрування, як і в попередніх випадках, проводити 0,1 М розчином лугу в присутності фенолфталеїну 2 рази до одержання співпадаючих з точністю ± 0,2 см3 результатів. Об’єми витраченого на титрування розчину лугу записати в табл. 1.3.
Таблиця 1.3. Результати титрування розчинів кислоти
| Номер колби | |||||
| Vпроби, см3 | |||||
| Vлугу, см3 | |||||
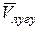 , см3 , см3
|
7. Визначити рівноважні концентрації кислоти с у розчинахза формулою:
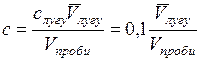 ,
,
де 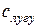 – концентрація розчину лугу, кмоль/м3; Vлугу – об’єм розчину лугу, який витрачено на титрування об’єму Vпроби, см3. Розраховані значення рівноважних концентрацій кислоти у фільтратах занести у табл. 1.4.
– концентрація розчину лугу, кмоль/м3; Vлугу – об’єм розчину лугу, який витрачено на титрування об’єму Vпроби, см3. Розраховані значення рівноважних концентрацій кислоти у фільтратах занести у табл. 1.4.
8. Використовуючи дані табл. 1.4, обчислити експериментальні значення питомої адсорбції aексп. (кмоль/кг):
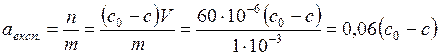 ,
,
де  – початкова концентрація кислоти у розчині, кмоль/м3; с – рівноважна концентрація кислоти після встановлення адсорбційної рівноваги, кмоль/м3; V – об’єм розчину кислоти (в нашому випадку V = 60 см3 = 60·10–6 м3); m – маса наважки активованого вугілля, кг. Записати обчислені експериментальні значення питомої адсорбції у табл. 1.4.
– початкова концентрація кислоти у розчині, кмоль/м3; с – рівноважна концентрація кислоти після встановлення адсорбційної рівноваги, кмоль/м3; V – об’єм розчину кислоти (в нашому випадку V = 60 см3 = 60·10–6 м3); m – маса наважки активованого вугілля, кг. Записати обчислені експериментальні значення питомої адсорбції у табл. 1.4.
9. Апроксимувати експериментально отримані значення величини адсорбції 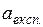 за допомогою рівняння Фрейндліха (1.2), користуючись для визначення його констант логарифмічною формою у вигляді:
за допомогою рівняння Фрейндліха (1.2), користуючись для визначення його констант логарифмічною формою у вигляді:
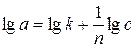 .
.
Для цього розрахувати значення логарифмів рівноважних концентрацій і логарифмів величин експериментальної адсорбції, записати їх у табл. 1.4 та побудувати графік в координатах 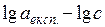 (рис. 2).
(рис. 2).
В зазначених координатах рівняння Фрейндліха є прямою, тангенс кута нахилу якої дорівнює  , а відрізок, який лінія відтинає на осі ординат, відповідає
, а відрізок, який лінія відтинає на осі ординат, відповідає 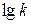 .
.
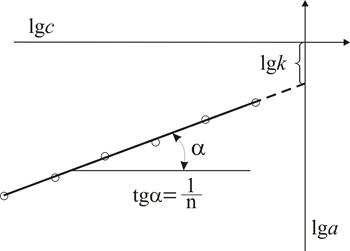
Рис. 2. Графік для визначення констант рівняння Фрейндліха
10. Користуючись отриманими значеннями константk та n, обчислити за рівнянням (1.2) для кожної рівноважної концентрації с апроксимовані величини питомої адсорбції aапр.. Розраховані апроксимовані значення записати у табл. 1.4, побудувати графік 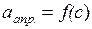 і визначити за ним максимальне експериментальне значення величини адсорбції amax.
і визначити за ним максимальне експериментальне значення величини адсорбції amax.
Таблиця 1.4. Експериментальні та розрахункові дані адсорбції кислоти на вугіллі
| Номер колби |  , кмоль/м3 , кмоль/м3
| с, кмоль/м3 | аексп., кмоль/кг | 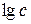
| 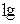 aексп. aексп.
| аапр., кмоль/кг | 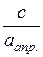
|
11. Визначити константи 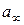 і
і 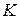 рівняння Ленгмюра (1.1), використовуючи його лінеаризовану форму
рівняння Ленгмюра (1.1), використовуючи його лінеаризовану форму
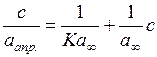 .
.
Для цього розрахувати значення величин 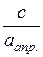 та побудувати лінійну залежність
та побудувати лінійну залежність 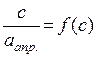 (рис. 3). За графіком обчислити величину граничної адсорбції a¥, яка є оберненою до тангенса кута нахилу прямої. За величиною граничної адсорбції та за відрізком, який пряма відтинає на осі ординат, розрахувати константу
(рис. 3). За графіком обчислити величину граничної адсорбції a¥, яка є оберненою до тангенса кута нахилу прямої. За величиною граничної адсорбції та за відрізком, який пряма відтинає на осі ординат, розрахувати константу 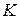 рівняння Ленгмюра.
рівняння Ленгмюра.
12. Визначити ефективність процесу адсорбції c за формулою:
 ,
,
де аmах – максимальне експериментальне значення величини адсорбції.
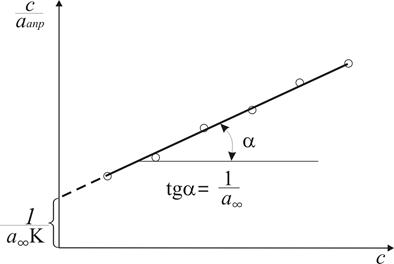
Рис. 3. Графік для визначення граничної адсорбції та константи рівноваги процесу
13. Розрахувати значення питомої поверхні адсорбенту за величиною граничної адсорбції, скориставшись рівнянням
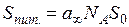 ,
,
де a¥ – величина граничної адсорбції; NA – число Авогадро; S0 – площа, яку займає молекула кислоти на поверхні адсорбенту. Ця площа визначається розміром гідрофільної частини молекули, тому для молекул одного гомологічного ряду вона є однаковою. У випадку одноосновних карбонових кислот S0 = 22×10–20 м2 = 22 Å2.
Звіт
Таблиці 1.1, 1.3 та 1.4.
Графіки 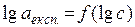 ;
; 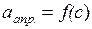 ;
; 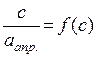 .
.
Константи рівняння Фрейндліха k = та n = .
Величина граничної адсорбції a¥ = кмоль/кг.
Константа рівняння Ленгмюра K = м3/кмоль.
Ефективність адсорбції c = %.
Питома поверхня активованого вугілля Sпит. = м2/кг.
Висновок.
Питання до лабораторної роботи
1. Що таке адсорбція, від чого вона залежить?
2. Як експериментально підтверджується мономолекулярний характер адсорбції кислоти на поверхні активованого вугілля?
3. З якою метою будують і як використовують графік 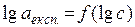 ?
?
4. Як визначають рівноважні концентрації кислоти після процесу адсорбції?
5. Які основні кількісні характеристики процесу адсорбції?
6. Навіщо при дослідженні адсорбції беруть п’ять різних вихідних концентрацій кислоти?
7. Як визначають значення граничної адсорбції?
8. Як змінюються константи рівняння Ленгмюра в межах гомологічного ряду?
Література: [1] 103 –104, 137–145; [2] 128 –132, 162–166; [3] 149, 174 –184.
Читайте також:
- I. Аналіз контрольної роботи.
- II. Вимоги безпеки перед початком роботи
- II. Вимоги безпеки праці перед початком роботи
- II.ТЕОРЕТИЧНІ ПИТАННЯ КУРСОВОЇ РОБОТИ
- III. Виконання бюджету
- III. Вимоги безпеки під час виконання роботи
- III. Вимоги безпеки під час виконання роботи
- III. Вимоги безпеки під час виконання роботи
- III. ПОРЯДОК ПРОВЕДЕННЯ РОЗРАХУНКІВ КУРСОВОЇ РОБОТИ
- Internet. - це мережа з комутацією пакетів, і її можна порівняти з організацією роботи звичайної пошти.
- IV Етап: Вибір стратегії керування виявленими ризиками й виділення пріоритетних напрямків роботи
- IV. Вимоги безпеки під час роботи на навчально-дослідній ділянці
| <== попередня сторінка | | | наступна сторінка ==> |
| Стислі теоретичні відомості | | | Лабораторна робота № 2 «ПОВЕРХНЕВИЙ НАТЯГ. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |