
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Закони електролізу
Електродні процеси підпорядковуються законам Фарадея.
1. Маса речовини, що виділилася (або розклалася) при електролізі, прямо пропорційна кількості електрики, що пройшла через розчин:
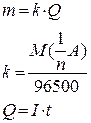 ,
,
де m – маса речовини, що виділилася внаслідок електролізу, г;
Q – кількість електрики, Кл.
2. При проходженні через розчин однієї і тої самої кількості електрики на електродах виділяється одна і та сама кількість еквівалентів речовини.
Обидва закони Фарадея можна виразити рівнянням:
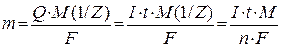 ,
,
де F – постійна Фарадея i дорівнює 96500 Кл/моль;
m – маса хімічно перетвореної речовини, г;
M(1/Z) – молярна маса еквівалента, г/моль;
Q – кількість електрики, Кл (Q=i·t).
Ця залежність лежить в основі електрогравіметричного методу аналізу.
Важливою характеристикою процесу електролізу є вихід за струмом, який дорівнює відношенню кількості речовини, яка виділилась, до кількості яка повинна була виділитись за законом Фарадея.
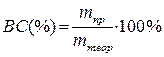 .
.
| <== попередня сторінка | | | наступна сторінка ==> |
| Електрогравіметричний метод | | | Напруга розкладання |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |