
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Типи кристалічних структур
Геометрична модель кристалу, будучи граничним спрощенням його фізико-хімічної моделі, дозволяє в наглядній формі сформулювати та описати ряд загальних закономірностей кристалів.
Геометричне моделювання здійснюється трьома способами:
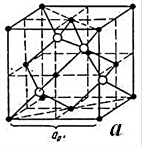
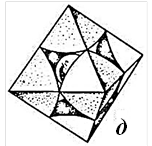
- рис. 2.7 а - системою точок що відбивають центри тяжіння відповідних складових елементів граток. Воно наочне, але не дає уявлення про істинне заповнення елементарної комірки;
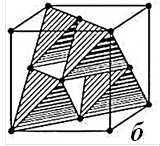
- рис. 2.7 б – координаційними поліедрами. Наочно відображає ступінь заповнення, тобто, коефіцієнт упаковки гратки, але не дозволяє оцінити центри розташування матеріальних часток та відносне співвідношення розмірів атомних або іонних сфер;
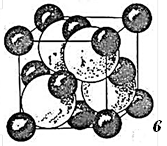
- рис. 2.7 в – найщільнішою упаковкою куль. Модель дозволяє вирішити обидві задачі. Сама графічна презентація – кулі різних розмірів у своїх позиціях.
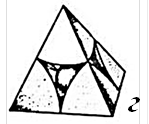
У третьому випадку (рис. 2.7 в), при використанні методу Полінга‑Бєлова, тобто, при поєднані центрів щільних куль (рис. 2.7 г, д), можна отримати два види порожнеч – тетраедричну (рис. 2.7 г) та октаедричну (рис. 2.7 д) у вигляді координаційних багатогранників (див. рис. 2.4).
При цьому, при максимальній ретикулярній щільності (ГЦК та ГП - к.ч. = 12):
- тетраедрична порожнина к.ч. = 4,
- октаедрична порожнина к.ч. = 6,
-  ,
,
η – коефіцієнт компактності
n –базис гратки (число атомів в елементарній комірці
Vатому, Vелементарної комірки – відповідні об’єми.
- rокт. = 0,41R,
- rтетр. = 0,225R, де:
rокт., rтетр. – розмір сфери, що поміщається в порожнечу,
R – радіус куль, що утворюють порожнечу.
ГЦК гратка: Cu; Ag; Au; Al; γ – Fe, Ni та інш.
ГП гратка:Mg; Zn; α – Ti; α – Co; Cd та інш.
| 
|
| |
| 
|
| Рисунок 2.7 – Типи моделювання кристалічної структури сфалериту (ZnS) системою точок (а), координаційними поліедрами (б) та найщільнішою упаковкою куль (в). Порожнечі – тетраедрична (г) та октаедрична (д) |
На геометричному рівні кінцевими структурними елементами гратки малися на увазі атоми або іони.
Але на етапі формування гратки можлива хімічна взаємодія між атомами або іонами (у тому числі з утворенням молекул хімічних сполук), що призводить до утворення стійких угруповань, взаємодія усередині яких сильніша, ніж в міжвузоллях. Тоді такі угруповання слід розглядати як структурні одиниці кристалів.
За наявністю або відсутністю таких угруповань, за числом їх просторових вимірів та за протяжністю розрізняють 5 типів структур:
Рис. 2.7 в – координаційні структури. Атоми або іони формують структуру, відповідну правильному координаційному поліедру (октаедр, кубооктаедр). Такі структури мають високе значення к.ч.: 12; 6+8;8+6 і т.п.
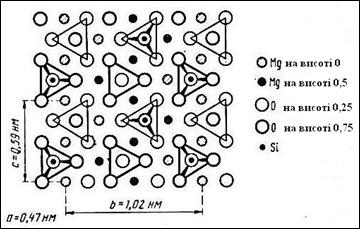
Рис. 2.8 а – острівні структури. Структурні одиниці складаються із двох або більше атомів. Зв’язок усередині угруповань сильний. Між атомами різних угруповань – зв’язок слабкий. До острівних структур відносяться молекулярні сполуки.
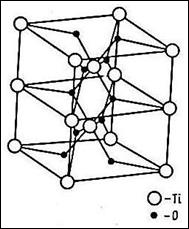
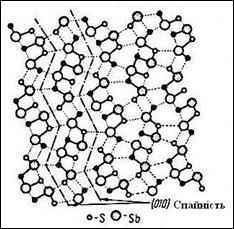
Рис. 2.8 б – ланцюжкові структури. Одновимірні угруповання, окремі структурні вузли яких пов’язані однаковим зв’язком у ланцюжки, витягнуті в одному напрямі. При здвоєнні такої структури завдяки відображенню на площині симетрії отримують стрічкові структури (рис. 2.6 в).
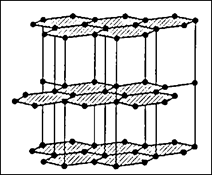
Рис. 2.9 а – шаруваті структури. Угруповання атомів пов’язані сильними хімічними зв’язками. Тягнуться нескінченно в двох напрямах. Зв’язок між угрупованнями слабкий – звичайно металічний або молекулярний.
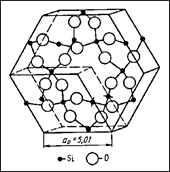
Рис. 2.9 в - каркасні структури. Координаційні поліедри в таких структурах мають спільні вершини, але ніде не стикаються ребрами або гранями. Характерною особливістю таких структур є наявність великих порожнеч.
 а
а
| |
 б
б
|  в
в
|
| Рисунок 2.8 – Острівний тип структури (а) олівіну MgFe[SiO4], ланцюжковий (б) тип структури рутилу TiO2 та стрічковий (в) тип антимоніту Sb2S2 |
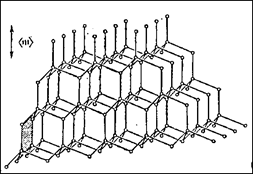
На рис. 2.9 б представлена кристалічна гратка алмазу з його координаційною структурованістю по чотирьом ковалентним гомеополярним зв’язкам. Закономірно віднесена до кубічної сингонії з к.ч. = 4 (за кількістю атомних зв’язків). Коефіцієнт компактності η = 0,34.
| 
| 
|
| а | б | в |
| Рисунок 2.9 – Шаруватий тип структури графіту (а), алмазна кристалічна гратка вуглецю (б) та каркасний тип структури кварцу SiO2 (в) |
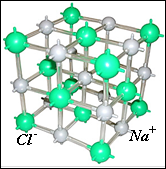
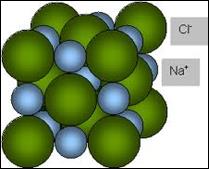
Рисунок 2.10 ілюструє модель структури кам’яної солі, побудований точечним методом (рис. 2.10 б), кубічна будова елементарної гратки, представлена методом найщільнішої упаковки (рис. 2.10 в) та кубічний габітус природного кристалу у макромасштабі (рис. 2.10 а).

| 
| 
|
| а | б | в |
| Рисунок 2.10 – Природний кристал кам’яної солі (а), його схема (б) та модель атомної будови (в) |
| <== попередня сторінка | | | наступна сторінка ==> |
| | | Ізоморфізм та поліморфізм |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |