
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Реакція клітин на опромінення
В результаті реакції біологічних систем на продукти, що з’явилися на хімічному етапі променевого ураження клітин, настає біологічний етап, що охоплює різні ієрархічні рівні організації живого організму.
Таким чином, іонізовані та збуджені молекули, що виникли на фізичному етапі, запускають складний ланцюг реакцій, що призводить у підсумку до ефектів, які фіксуються в біологічному експерименті. Тому чітке розуміння первинних механізмів взаємодії іонізуючого випромінювання з речовиною є відправною точкою аналізу механізмів біологічної дії випромінювання.
Перші коректно поставлені (в 20-х роках) кількісні експерименти дали змогу виявити фундаментальну закономірність, що зв’язує біологічний ефект з дозою опромінення:
навіть малі дози опромінення спричиняють ушкодження клітин та макромолекул; у той же час при значних дозах виявляються об’єкти, не ушкоджені випромінюванням. Такий діапазон виявлених ефектів опромінення перевищує природну біологічну мінливість вивчених об'єктів і не може бути пояснений їх біологічними особливостями. Отже, вирішальний вплив на характер кривих доза - ефект мають не біологічні особливості об'єктів, а спосіб передачі енергії. Частки іонізуючого випромінювання передають енергію дискретними порціями і процес передачі енергії має статистичний характер. Через це в клітині, що має високу різноякісність у морфологічному і функціональному відношенні, окремі мікроструктури при опроміненні з певною ймовірністю поглинають енергію опромінення, а інші взагалі не взаємодіють з випромінюванням.
На основі цих фундаментальних фізичних концепцій сформульовано принципи потрапляння в мішень, які дали змогу пояснити кількісні закономірності, що спостерігаються в біологічних експериментах. Вперше концепція потрапляння в мішень, що стала класичною, була запропонована в 20-х роках Ф. Дессауером (1922), розвинена в роботах Дж. Краузера (1924), Д. Лі (1946) і М.В. Тимофеєва-Ресовського (1956). Її загальні положення такі:
- іонізуючі випромінювання перадають енергію дискретними порціями;
- акти потрапляння не залежать один від одного;
- біологічний ефект виникає в разі потрапляння у чутливу структуру (мішень).
Теорія потрапляння в мішень повністю грунтується на фізичній основі і описує кількісні закономірності радіаційного ушкодження окремих мішеней. Вона не бере до уваги процесів, що відбуваються між актом ураження мішені і кінцевим біологічним ефектом, тобто не враховує біологічної специфіки об'єкта, а саме: яскраво виражену гетерогенність біологічних структур, можливість модифікації променевого ураження і здатності до пострадіаційного відновлення.
У 60-х роках О. Хуг і А. Келлерер запропонували стохастичну гіпотезу як загальну теорію впливу іонізуючого випромінювання на клітину. Вона базується на тому, що випадкові й дифузно розміщені акти збудження та іонізації лише в рідкісному випадку однозначно спричиняють загибель клітини. На цю «стохастику першого порядку» накладається «стохастика вищих порядків», зумовлена динамічною нестабільністю життєвих процесів, здатних усувати або посилювати радіаційне ушкодження. Стохастична гіпотеза враховує сучасні дані про мікророзподіл енергії, мінливість радіочутливості біологічних об'єктів, а також роль відновлювальних процесів.
Початкові процеси променевого ураження організму виникають у клітині, тому вивчення її реакції на опромінення має велике значення для розуміння закономірностей розвитку ураження всього організму.
Внаслідок ураження пошкоджуються абсолютно всі внутріклітинні структури, в ній спостерігається безліч різноманітних реакцій. При опроміненні знижується щільність цитоплазми за зменшення кількості рибосом і відбувається накопичення залишків зруйнованих органел, спостерігаються руйнівні процеси в хлоропластах. Пошкодження ендоплазматичних мембран спричиняє порушення багатьох складних процесів клітинного метаболізму, для перебігу яких необхідна просторова організація груп ферментів, яку забезпечують мембрани. Порушення цілісності мембран може змінити іонний баланс клітини, що також несприятливо впливає на хід метаболічних процесів.
Слід зазначити, що в клітині значна кількість органел, здатних до поділу (розмноження), тому пошкодження їх не призводить до незворотних наслідків на відміну від ушкодження ядра клітини. Міра цих реакцій залежить від того, на якій стадії життєвого циклу клітини сталося опромінення.
Клітинний цикл. Клітини, здатні до поділу, послідовно проходять такі етапи: інтерфазу і мітоз, що складають разом так званий клітинний або мітотичний цикл. В інтерфазі - найтривалішому етапі мітотичного циклу - розрізняють три періоди:
- передсинтетичний (G1), в якому відбуваються процеси і підготовка до подвоєння ДНК;
- синтетичний (S), в якому синтезується ДНК;
- постсинтетичний (G2), в якому відбуваються процеси, пов'язані з формуванням мітотичного веретена і накопичення енергії. Таким чином, мітотичний цикл складається з чотирьох основних періодів (G1, S, G2) і мітозу (М).
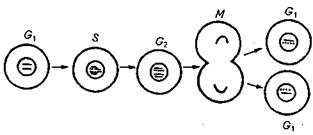
Рис. Фази клітинного циклу: G1 − пресинтетична, протягом якої відбувається підготовка до реплікації ДНК; S − реплікативна, або синтетична, в ході якої подвоюється генетичний матеріал, і клітина стає тетраплоїдною; G2 − постреплікативна, за час якої клітина здійснює підготовку до мітотичного поділу; М − власне мітотичний поділ, унаслідок якого виникають дочірні диплоїдні клітини.
Мітоз, в свою чергу, складається з послідовних фаз − профази, метафази, анафази і телофази. В профазі відбувається збільшення ядра, в якому чітко видно спіралізовані хромосомні нитки. Хромосоми складаються з двох сестринських хроматид, з'єднаних центромерою (механічний центр хромосоми). Наприкінці профази щезає ядерна оболонка і ядерця. Центріолі (центри поділу клітини) розходяться і формують два полюси клітини.
У метафазі хромосоми досягають максимальної спіралізації, переміщуються до екватора клітини і розміщуються так, що центромери всіх хромосом перебувають в одній площині, формуючи метафазну пластинку. В клітині вже сформоване мітотичне веретено, що складається з опорних і тягнучих ниток. Перші з них простягаються між полюсами, а другі зв'язують центромери хромосом з полюсами.
В анафазі відбувається поділ центромер і розходження сестринських хроматид хромосом до різних полюсів за допомогою мітотичного веретена. Так відбувається точний розподіл генетичного матеріалу між дочірніми клітинами.
У телофазі хромосоми на кожному полюсі деспіралізуються, мітотичне веретено руйнується, утворюється ядерна оболонка і з'являються ядерця, формується клітинна стінка, що ділить вміст цитоплазми на дві рівних частини.
Тривалість мітотичного циклу - час між двома послідовними поділами клітини - неоднакова у різних клітин. Наприклад, у клітинах кінських бобів тривалість мітотичного циклу становить 30 годин, при цьому мітоз триває 4 години, а інтерфаза - 26 годин, із яких період G1 -12 годин; період S - 6 годин; період G2 - 8 годин. У клітин скерди найкоротший мітотичний цикл - 8 годин (Паушева З.П., 1974). У тканинах, що мало обновлюються, більшість клітин тривалий час перебуває в періоді G1, що зумовило виділення ще однієї стадії – G0. Клітини, що перебувають у цій стадії, прийнято вважати поза циклом, або такими, що перебувають в стані спокою. Такі клітини складають резерв відновлення клітинної популяції у разі загибелі частини клітин, здатних до поділу за будь-яких причин.
- Тимчасові реакції клітин на опромінення.Серед реакцій клітин на опромінення є такі, які легко витримує клітина. До них належать різноманітні порушення метаболізму. Як правило, такі реакції виникають безпосередньо після опромінення і з часом минають. Найбільш характерною з них є тимчасова затримка клітинного поділу. Тривалість затримки поділу залежить від дози опромінення і проявляється у всіх клітин опроміненої популяції. Час затримки у клітин різних організмів відрізняється, але завжди зростає з дозою опромінення.
Характерною особливістю цієї реакції клітин на опромінення є те, що зі збільшенням дози зростає тривалість затримки поділу кожної опроміненої клітини. Тривалість затримки поділу залежить від стадії клітинного циклу, в якій перебувала клітина під час опромінення: найтриваліша вона при опроміненні в стадії S або G2 і найменш тривала - при опроміненні в мітозі.
Механізм радіаційної затримки поділу клітин повністю не з'ясовано. Найчастіше її пов'язують з пошкодженням множинних внутріклітинних структур, втрата яких з часом компенсується.
- Летальні реакції клітин, форми клітинної загибелі.Найчутливіші до опромінення тканини, клітини яких здатні до активного поділу. Тому серед багатьох проявів дії іонізуючого опромінення на життєдіяльність клітини найважливішим є втрата цієї функції. В зв'язку з цим клітинною загибеллю або летальним ефектом опромінення вважається втрата клітиною здатності до поділу. Клітинами, що вижили, вважаються ті, що зберегли здатність до необмеженого розмноження. Отже, йдеться про репродуктивну загибель клітин. Репродуктивна форма променевої інактивації клітин найбільш поширена в природі. Залежно від дози загибель настає як у процесі першого післярадіаційного поділу, так і в кількох подальших мітозах.
Таким чином, репродуктивною чи мітотичною формою загибелі клітин називають види променевої інактивації клітин, що настають після першого післярадіаційного мітозу і призводять до припинення клоноутворення.
Кількісним методом оцінки летального ушкодження є рівень виживання клітин у клітинних культурах in vitro, що визначається як відношення кількості клітинних колоній, що утворилися після опромінення кожною дозою, до кількості колоній, що утворилися в контролі. Критерієм радіочутливості клітин є летальна доза 50 % (ЛД50). Це доза, при якій виживають 50 % опромінених клітин.
Слід звернути увагу на специфічну особливість летальних реакцій клітин. Вона полягає в тому, що зі збільшенням дози зростає не лише рівень пошкодження всіх опромінених клітин, як це буває при затримці поділу, а й частка ушкоджених клітин. Іншими словами, як при найменших дозах можуть виявитися уражені клітини, так і при досить значних дозах можуть зберегтися окремі життєздатні клітини, але з малою ймовірністю.
Клітини, які зазнали проліферативної загибелі, виявляють певні ознаки життєдіяльності: відбуваються основні процеси метаболізму, біосинтез білків та інших речовин, рух цитоплазми, зберігається мембранна проникність тощо.
Дозовізалежності проліферативної виживаностіздебільшого мають вигляд експоненціальних кривих (рис.1), а в системі напівлогарифмічних координат — прямих ліній. Відповідно аналітичний вираз, що описує криву дозової залежності виживаності, є експоненціальною функцією:
N / N0 = e-kD,
де N − кількість клітин, що вижили після опромінення; N0 − загальна кількість клітин, опромінених у дозі D; k− коефіцієнт, що характеризує кут нахилу експоненти до осі абсцис; e − основа натурального логарифма.
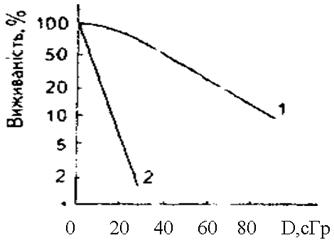
Рис. 1.Залежність виживаності сперматогоніїв від дози опромінення: 1 − гамма-радіацією (60Со); 2 − швидкими нейтронам (1 МеВ).
Очевидно, чим ця крива крутіша, тим більше зменшується виживаність у разі зростання дози, що є свідченням вищої радіочутливості клітин. Тому константу k можна використовувати як коефіцієнт радіочутливості, хоча це не дуже зручно: k —безрозмірна величина, а її чисельне значення залежить від масштабу системи координат. Проте на експоненціальній кривій немає таких особливих точок, які можна було б використовувати для характеристики радіочутливості.
На кривих, які описують залежність виживаності клітин або організму від концентрації токсичних хімічних сполук, така характерна точка є, вона відповідає граничній концентрації токсину, за якої клітини гинуть. Очевидно, така точка є й на концентраційних кривих сигмоїдальної форми, які описують функцію «все або нічого» й відповідно мають «поріг». Радіочутливішим клітинам відповідає менше значення порогової концентрації токсину, ніж радіостійкішим.
Оскільки на кривій доза ~ ефект немає чіткого граничного значення дози, за якого не виживає жодна клітина, для характеристики радіостійкості клітин введено спеціальну величину — дозу, за якої гине певна частина клітин у популяції, наприклад 30, 90 % і т. д. Часто використовують значення дози, за якого гине половина клітин.
Це − так звана напівлетальна доза ЛD50. У разі опромінення клітин у цій дозі відповідно виживає 50 % клітин. Використовують також LD95- дозу, за якої 95 % клітин інактивуються, а 5 % − залишаються неушкодженими.
Порівнянням значень ЛD50 або LD95 для різних клітинних популяцій з'ясовують, які клітини є радіостійкішими.
Експоненціальність кривих доза ~ ефект дає змогу достатньо просто визначити, в скільки разів слід збільшити дозу опромінення, щоб виживаність клітин знизилася до певного рівня.
Поняття напівлетальної дози стосується популяції − достатньо великої кількості однорідних клітин, що зазнають опромінення.Стосовно ж окремої клітини ця величина трансформується в характеристику ймовірності її інактивації. Дозі ЛD50 відповідає ймовірність інактивації 0,5, тобто клітина або загине, або залишиться неушкодженою.
Досить часто криві виживаності за малих значень доз відхиляються від експоненти й складаються з двох частин: початкової, в якій зростання дози не супроводжується істотним зменшенням виживаності, та власне експоненціальної. Перша частина кривої називається «плечем». Для характеристики кривої з «плечем» уведено такі параметри: екстраполяційне число п і розмір плеча Dq.
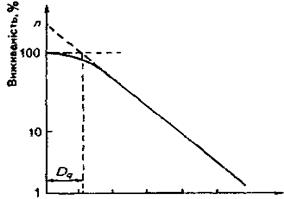
Екстраполяційне число п − це координати точки перетину прямолінійного продовження експоненціальноїчастини кривої з віссю ординат (рис.2). Очевидно, якщо в кривої виживаності с «плече», значення екстраполяційного числа буде там більшим, чим вища радіочутливість опромінюваного об'єкта.
0 1 2 3 4 5 D,ум.од.
Рис. 2. Дозова крива в напівлогарифмічному масштабі та параметри n іDq,.
Розмір плеча Dq характеризують значенням дози, яке відповідає точці перетину прямої, що екстраполює експоненціальну частину кривої, з прямою, паралельною осі абсцис і проведеною з точки повної виживаності (рис.2).
Визначимо значення дози D*, за якої виживаність зменшується в e разів (e — основа натурального логарифма):
N / N0 = e-kD =1/e,
KD* = 1,
D* = 1 / k,
Як правило, дозу D* називають нульовою(D0).
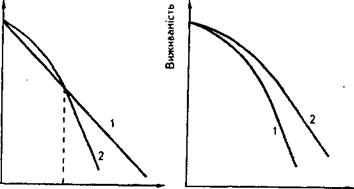
D D
А б
Рис. 3.Приклади залежностей доза ~ ефект для клітин або багатоклітинних організмів:
а − криві 1 і 2 перетинаються в точці, що відповідає значенню дози, до якої перша популяція визначається як менш радіостійка порівняно з другою; б − у всьому інтервалі доз опромінення перша популяція менш радіостійка, ніж друга.
Якщо дозова крива не має «плеча», то D0 дорівнює так званій 37 %-ній дозі (D37 ), за якої відповідно виживає 37 % клітин. Якщо ж дозова крива − це експонента з «плечем», то D0 = D37 лише в експоненціальній частині. Для всього інтервалу доз, починаючи з нульового, значення D37 більше за D0.
Дози D0, D37 та D50 використовують як показники радіостійкості опромінюваних об'єктів.
Якщо виживаність описується дозовою кривою з «плечем», то може статися ситуація, проілюстрована на рис.3, де зображено дві дозові криві з різними значеннями «плечей» і D. Криві 1 і 2 перетинаються в точці, що відповідає значенню дози, до якого Перша популяція поводить себе як менш стійка до опромінення порівняно з другою популяцією. За більших значень дози перша популяція характеризується вищою радіостійкістю. Аби уникнути такого подвійного тлумачення порівняльних радіостійкостей, вважають, що радіостійкість визначається лише значенням D0, тобто нахилом експоненціальної частини дозової кривої.
Природа радіаційної загибелі клітин.При аналізі причин радіаційного ушкодження клітини слід розглянути питання про відносну радіочутливість ядра і цитоплазми. В дослідах з опромінення ядра і цитоплазми виявлено значно більшу чутливість ядра, тому в променевій загибелі клітин вирішальну роль відіграє саме пошкодження ядра.
До складу ядра в основному входять молекули ДНК, що мають велику довжину (в клітинах ссавців загальна довжина молекул ДНК становить від 1 до 2 м). Опромінення спричиняє різноманітні пошкодження ДНК та її комплексів, як от: розриви молекул ДНК, утворення лужно-лабільних зв'язків, втрату основ і зміну їх складу, зміну нуклеотидних послідовностей.
Процеси, які відбуваються внаслідок опромінення ДНК безпосередньо в живій клітині, ускладнюються тим, що до власне радіаційно-хімічних перетворень азотистих основ і розривів фосфоефірних зв'язків приєднуються вторинні реакції, в котрих беруть участь ферменти.
Переглядів: 3609