
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Самовільний процес концентрування розчиненої речовини на межі поділу розділу фаз називають адсорбцією.
Адсорбцію можна розглядати як надлишок речовини в поверхневому шарі, віднесений до одиниці площі поверхні. Величина адсорбції позначається Г і дорівнює: Г = n/S, n – кількість речовини, моль; S – площа поверхні, м2.
В 1978р. Дж. Гіббс вивів рівняння яка дає можливість визначити величину адсорбції в розчині на основі експериментальних данних відносно зміни поверхневого натягу із змінами концентрації розчиненої речовини. Це рівняння називається рівнянням Гіббса
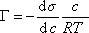
де Г – величина адсорбції, моль/м2; С – рівноважна концентрація речовини, моль/л; R – універсальна газова стала, 8,31 Дж/моль К; Т – абсолютна температура, К; - ∆σ/ ∆С – поверхнева активність речовини, Дж/м2
- Адсорбція на межі поділу тверде тіло – газ.
Усі випадки поглинання газів і випарів твердими тілами називають сорбцією.Якщо цей процес відбувається тільки на поверхні, то його називають адсорбцією, а коли речовина, яка поглинається поверхнею, дифундує усередину поглинаючої речовини і розподіляється по її об’єму , то таке явище називають абсорбцією.
Тверде тіло, на поверхні якого відбувається адсорбція, прийнято називати адсорбентом, а речовину, яка адсорбується – адсорбатом.
Десорбція –це видалення адсорбованих молекул з поверхні адсорбенту. Швидкість адсорбції з часом зменшується, а швидкість десорбції збільшується.
Залежно від природи адсорбційних сил розрізняють два види адсорбції: фізичну і хімічну.
Фізична адсорбція зумовлена дією силових полів поверхневих молекул адсорбенту, при цьому молекули адсорбату не втрачають своєї індивідуальності. Цей процес відбувається тільки на певних ділянках адсорбенту (адсорбційних центрах) – виступах, вузлах кристалічної решітки, які мають надлишкову поверхневу енергію. Фізична адсорбція характеризується такими чинниками: швидкою оборотністю процесів адсорбції – десорбції, зменшення адсорбції при підвищенні температури.
Хімічна адсорбція або хемосорбція зумовлена взаємодіями між поверхневими молекулами адсорбенту і адсорбату. На поверхні адсорбенту утворюються хімічні сполуки і окремі молекули втрачають свою індивідуальність. Хемосорбція характеризується необоротністю, збільшенням адсорбції за підвищення температури.
Рівняння адсорбції Ленгмюра.
Адсорбція газу на твердій поверхні є найпростішим випадком адсорбції. Теорію цього процесу (мономолекулярної адсорбції) запропонував американський вчений І.Ленгмюр.
Основні положення цієї теорії:
1) Адсорбція має локалізований характер, тобто молекули адсорбату не можуть переміщуватися по поверхні адсорбенту, вони зв’язані з молекулами адсорбенту силами, близькими до сил хімічних зв’язків.
2) Адсорбція молекул адсорбату відбувається на активних центрах. Це дефекти кристалічної гратки. Кожен такий центр адсорбує лише одну молекулу адсорбату, тому на поверхні адсорбенту утворюються лише мономолекулярний шар адсорбату;
3) Встановлення адсорбційної рівноваги – це результат конкуренції сил притягання молекул адсорбату до адсорбенту та теплового руху молекул. Коли швидкість цих двох протилежних процесів зрівнюється, настає стан динамічної рівноваги, внаслідок якої розподіл молекул газу між поверхнею і об’ємом залишається сталим.
Рівняння адсорбцій газу на твердій поверхні називають рівнянням ізотерми адсорбції Ленгмюра.
Г = Гмах р/ К+ р
де к – константа пропорційності, р – тиск.
Це рівняння можна застосовувати і до мономолекулярної адсорбції із розчинів. Якщо молекули розчиненої речовини адсорбуються на поверхні адсорбенту, а їх концентрація дорівнює С, то
Г = Гмах С/ К+ С
Адсорбція газів на твердій поверхні грає важливу роль в процесах газообміну організму з оточуючим середовищем. Принцип дії протигазів, системи життєзабезпечення в підводних і космічних човнах складає саме адсорбція газів і випарів на поверхні твердих речовин.
Читайте також:
- A) правові і процесуальні основи судово-медичної експертизи
- H) інноваційний менеджмент – це сукупність організаційно-економічних методів управління всіма стадіями інноваційного процесу.
- I. Доповнення до параграфу про точкову оцінку параметрів розподілу
- II. Поняття соціального процесу.
- IV. Запасні речовини
- IV. План навчального процесу.
- Iзобаричний процес
- Iзотермiчний процес
- Iзохоричний процес
- V Практично всі психічні процеси роблять свій внесок в специфіку організації свідомості та самосвідомості.
- V Процес інтеріоризації забезпечують механізми ідентифікації, відчуження та порівняння.
- А. В. Петровський виділяє три стадії розвитку особистості в процесі соціалізації: адаптацію, індивідуалізацію і інтеграцію.
| <== попередня сторінка | | | наступна сторінка ==> |
| Лекція № 7 | | | Адсорбція електролітів |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |