
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Потенціометричне титрування заліза діхроматом калію
Мета роботи: визначити концентрацію солі заліза(ІІ) методом потенціометричного титрування.
Іони заліза(ІІ) характеризуються відновними властивостями (Е0=0,77 В), тому у розчині легко окислюються такими окисниками, як Cr2O72–, VO3–, MnO4– та інші.
Сумарна реакція взаємодії з біхроматом калію має вигляд:
6FeSO4 + K2Cr2O7 + 7H2SO4 = 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
або у іонному вигляді:
6Fe2+ + Cr2O72– + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O.
У якості індикаторного використовують електрод з інертного металу, потенціал якого буде залежати від концентрації іонів у розчині як описано у розділі 4.2.3.1 пункт 2) та на кривій титрування буде спостерігатися один стрибок титрування.
У реальних системах, що необхідно проаналізувати, іони заліза знаходяться у трьохвалентному стані, тому їх спочатку відновлюють станум(ІІ) хлоридом, додаючи до гарячого досліджуваного розчину, підкисленого HCl. Розчин буде містити іони Fe2+ та надлишок іонів Sn2+, таким чином на кривій титрування біхроматом калію буде спостерігатися два стрибки титрування: перший обумовлений окисненням Sn2+ до Sn4+, другий – Fe2+ до Fe3+.
Обладнання та реактиви
1. Потенціометр.
2. Платиновий та хлорсрібний електроди.
3. Розчини солі Мора та K2Cr2O7, 0.1 моль-екв/л.
4. Сульфатна кислота, 1:4.
5. Бюретка, мірні стакани та циліндри, хімічні стакани на 100 мл.
6. Магнітна мішалка.
Методика виконання роботи
У викладача отримують хімічний стакан, що містить розчин з невідомою кількістю Fe2+. Додають приблизно 25 мл розчину сульфатної кислоти та дистильовану воду (≈25 мл). Опускають у розчин магнітну мішалку та занурюють закріплені на штативі електроди таким чином, щоб вони не торкались мішалки на дні стакану. Після додавання кожної порції титранту K2Cr2O7 (0,2 мл) вимірюють значення ЕРС та заносять до таблиці. Будують криві титрування та знаходять точку еквівалентності як показано у розділі 4.2.3.2.
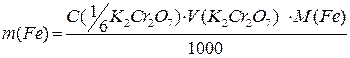 ,
,
де 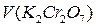 – об’єм точки еквівалентності.
– об’єм точки еквівалентності.
| <== попередня сторінка | | | наступна сторінка ==> |
| | |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |