
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Швидкість хімічних реакцій. Закон діючих мас. Константа рівноваги
Кожна хімічна реакція протікає з певною швидкістю і закінчується після досягнення певного стану рівноваги. Швидкість хімічної реакції визначається зміною концентрації одного з компонентів реакції за одиницю часу і залежить від природи реагуючих речовин, їх концентрації, температури, присутності каталізатора. Вплив концентрації реагуючих речовин на швидкість хімічної реакції визначається законом дії мас.
Швидкість хімічних реакцій за постійної температури прямо пропорційна добутку молярних концентрацій (активностей) реагуючих речовин, піднесених до степенів їх стехіометричних коефіцієнтів.
Оскільки більшість хімічних реакцій за однакових умов можуть відбуватися у двох протилежних напрямках (єзворотними), то для реакції, що відбувається за схемою:
aA + bB « cC + dD ( І )
де a, b, c, d – стехіометричні коефіцієнти; A, B – вихідні речовини; C, D – продукти реакції
швидкість прямої реакції описується рівнянням
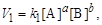
а швидкість зворотної запишеться як
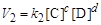 ,
,
де V1,2 - швидкості реакцій; k1,2– константи швидкості реакцій; [A] і [B]- концентрації реагуючих речовин, моль/дм3; [С] і [D]- концентрації продуктів реакції, моль/дм3.
Через певний час швидкість обох реакцій вирівнюється і процес приходить до стану хімічної рівноваги:
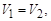
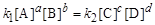 .
.
При постійних температурі і тиску константа рівноваги залишається постійною та не залежить від концентрації учасників реакції.
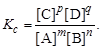 (3.1)
(3.1)
Це рівняння є математичним виразом закону дії мас стосовно стану хімічної рівноваги. Константу Kc називають концентраційною константою рівноваги. Вона залежить від температури, але не залежить від концентрацій речовин, які реагують.
Напрям зміщення рівноваги системи визначається принципом Ле-Шательє: якщо змінювати одну з умов стану системи, яка знаходиться в рівновазі (температуру, концентрацію, тиск), то рівновага зміститься у напрямку реакції, яка протидіє цій зміні.
Для ендотермічних реакцій (DH > 0) Ka зростає з ростом температури, а для екзотермічних (DH < 0) – спадає.
Переглядів: 926