
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Рівняння Нернста
Якщо компоненти окисно-вiдновної пари не перебувають в стандартному станi, то змiна вiльної енергiї i величина окисно-вiдновного потенцiалу системи будуть залежати вiд активностi даної пари. Так, для реакцiї
Ок. + ne– « Вiдн. (VII)
змiна вiльної енергiї системи описується рiвнянням
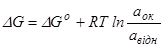 , (6.5)
, (6.5)
де R=8.31441 Дж/(моль´К) – унiверсальна газова постiйна; Т – абсолютна температура, К; аок, авідн– активностi окисненої та вiдновленої форм речовини. Або
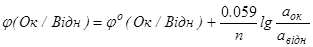 . (6.6)
. (6.6)
Цей вираз носить назву рівняння Нернста.
Переходячи вiд активностей до рiвноважних концентрацiй частинок в розчинi одержимо:
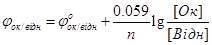 . (6.7)
. (6.7)
Потенцiал окисно-вiдновної пари, обчислений за рiвнянням Нернста для будь-яких концентрацiй, називають рівноважним потенціалом.
Величина окисно-вiдновного потенцiалу залежить вiд природи речовини (joок/відн), йонної сили розчину, концентрацiї окисненої [Ок] та вiдновленої [Вiдн] форм речовини, рН середовища та температури.
Переглядів: 965