
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
А. Рівняння стану ідеального газу
Рівняння Клапейрона: для 1кг - Pn = RT , для М кг - PV= МRT; для 1 Кмоля - PµV=µRT , де Р - абсолютний тиск газу, Н/м²; n - питомий об'єм газу, м³/кг; V - об'єм газу, м³; µV - об'єм 1 Кмоля газу, м³; µ- молярна маса газу , кг/кмоль; R – газова постійна, Дж/(кг К); Т - абсолютна температура газу, К.
Газова постійна: 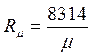 ,
,
де 8314 - універсальна газова постійна, Дж /(кмоль·К).
Абсолютний тиск газу, Н/м²:
- якщо абсолютний тиск більше тиску навколишнього середовища Р = Рн + В,
де Рн - надмірний тиск, вимірюваний манометром, Н/м²; В - тиск навколишнього середовища, вимірюваний барометром, Н/м²;
- якщо абсолютний тиск менше тиску навколишнього середовища Р = В + Рв,,
де Рв - розрідження, вимірюване вакуумметром, Н/м².
Приклад 1. Визначте температуру кисню, який знаходиться в резервуарі місткістю V = 10 м³ за умови, що на манометрі Р = 7·10 Н/м², барометричний тиск В = 740 мм рт.ст., масса М=100 кг.
Рішення. З рівняння Клапейрона для маси М кг газа Т = PV/(MR). Тоді:
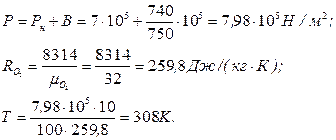
Переглядів: 324