
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Г. Термодинамічні процеси ідеального газу
Термодинамічним процесом називають зміну параметрів стану робочого тіла. Існує нескінченна кількість термодинамічних процесів, їх називають політропними, і зміна параметрів в них підкоряється рівнянню: PVn = const, де n - показник політропи.
Окремими процесами є ізохорний (V=const), ізобарний (P=const), ізотермічний (T=const) і адіабатний (dq=const), який протікає без відведення і підведення теплоти. Для будь-якого процесу зміна внутрішньої енергії 1 кг газу обчислюється за виразом:
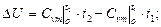 при Сv = const DU = Cv (t2 – t1).
при Сv = const DU = Cv (t2 – t1).
зміна ентальпії 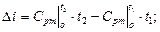 при Сv = const Dt = Cp (t2 – t1).
при Сv = const Dt = Cp (t2 – t1).
зміна ентропії :

Приклад 5. В закритій посудині знаходиться повітря при тиску Р1=5 бар і температурі t1=270 С. Визначте тиск повітря після охолодження до 0°С. Зобразите процес в P-V і Т-S - координатах.
Рішення. Залежність між початковими і кінцевими параметрами в ізохорному процесі 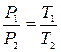 . Тоді
. Тоді 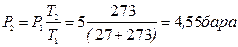

Приклад 6. Визначте роботу ізобарного розширення азоту масою 7 кг при нагріванні в інтервалі температур від t1= 2000С до t2= 6000С. Покажіть процес в P-V-і Т-S - діаграмах.
Рішення. Робота розширення 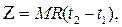

де М - маса газу, R - газова постійна, Дж/ (кг×0С); t1, t2 - відповідно початкова і кінцева температура азоту, 0С.
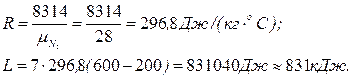
Приклад 7. 0,2 кг кисню при температурі t1=250С розширюється ізотермічно до триразового збільшення об'єму. Визначте кількість теплоти, що надається тілу.
Рішення. Оскільки в ізотермічному процесі вся підведена теплота йде на здійснення роботи, то 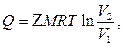
де Q - підведена теплота, Дж; М - маса газу, кг; R - газова постійна, Дж/(кг·К );
Т – температура газу, К; V1 і V2 - відповідно початковий і кінцевий об'єм, м³.
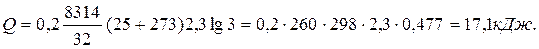

Приклад 8. Газ СО при тиску Р1=0,9 бар і початковій температурі t1=120С адіабатно стискається до тиску Р2=3,6 бара. Визначте температуру в кінці стиснення.
Рішення. Кінцеву температуру визначають із співвідношення параметрів Р і Т в адіабатному процесі:
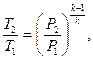
де k – показник адіабати. Для двоатомного газу k=1,4. Тоді
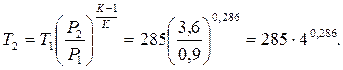
Позначимо  через N. lg N = 0,286×ln4 = 0,286·0,602 = 0,172.
через N. lg N = 0,286×ln4 = 0,286·0,602 = 0,172.
Звідси N=1,49. Отже T2=285·1,49=425K.
Д. Термодинамічні процеси зміни стану водяної пари
Водяна пара – робоче тіло в парових турбінах і машинах, теплоносій в різних теплообмінниках і т.д. Водяна пара не може розглядатися як ідеальний газ і до неї не застосовні залежності, отримані для ідеальних газів, в тих випадках, коли вони є робочим тілом парових установок.
Графічне зображення термодинамічних процесів з водяною парою
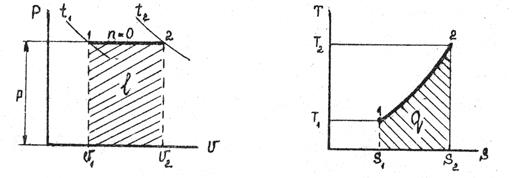
Ізохорний процес (V=const ). На P-V – діаграмі ізохору зображують відрізком прямої, паралельної осі ординат; на T-S – діаграмі - в області вологої насиченої пари - кривою лінією з опуклістю вгору, а в області перегрітої пари - опуклістю вниз.

Ізобарний процес (P=const). На P-V–діаграмі ізобару зображують горизонтальною прямою лінією; на T-S–діаграмі - в області вологої пари ізобара є одночасно і ізотермою, і її зображають горизонтальною прямою; в області перегрітої пари - кривою з опуклістю вниз; на I-S - діаграмі в області вологої пари – це похила пряма, а в області перегрітої пари - крива з опуклістю вниз.
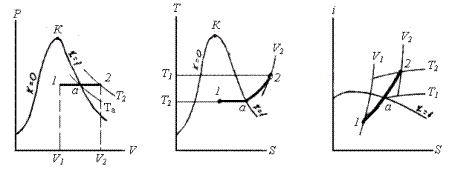
Ізотермічний процес (T=const). На P-V-діаграмі ізотерму зображають в області вологої пари горизонтальною прямою, в області перегрітої пари - кривою з опуклістю вниз; на T-S - діаграмі - це горизонтальна пряма. В I-S-діаграмі в області вологої пари ізотерма співпадає з ізобарою, а в області перегрітої пари її зображають кривою з опуклістю вгору.
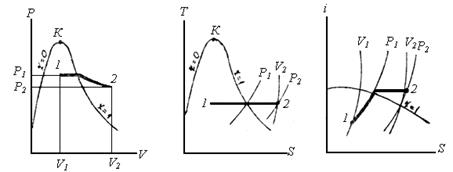
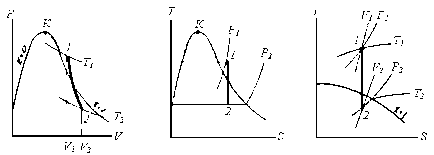
Адіабатний процес. На P-V-діаграмі адіабату зображають кривою з опуклістю вниз, що йде в області вологої пари більш полого, ніж в області перегрітої пари; на T-S і I-S-діаграмах – це вертикальні прямі.
Основні розрахункові формули для процесів, в яких водяна пара є робочим тілом, зведені в табл. 2.2.
Таблиця 2.2
Основні розрахункові формули
 Значення параметрів для сухої насиченої пари, води і перегрітої пари беруть з таблиць водяної пари.
Значення параметрів для сухої насиченої пари, води і перегрітої пари беруть з таблиць водяної пари.
Значення параметрів вологої насиченої пари визначають по таких формулах:
vx = v'(1-x) + v"x; ix = i'(1-x) + i"x; Sx = S'(1-x) + S"x;
де x- ступінь сухості; v', i', S' і v'', i'', S''– питомий об'єм, ентальпія і ентропія відповідно киплячої рідині і сухої насиченої пари (беруть з таблиць водяної пари).
Необхідні значення параметрів для будь-якої пари також можуть бути визначені по I-S - діаграмі, але з меншою точністю.
Приклад 10. Визначте кількість теплоти, що підводиться до 2 кг вологої насиченої пари в процесі v=const при P=5,5 бар і ступені сухості x=0,9 для отримання сухої насиченої пари.
Рішення. Теплота, що підводиться Qv= ΔU = U2 - U1; U1 = M (i1 - P1 v1);
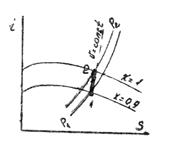 U2=M (i2-P2 v2).
U2=M (i2-P2 v2).
По I-S- діаграмі водяної пари знаходимо:
i1=608 кДж/кг; i2=660 кДж/кг;
v1=0,3 м3/кг; v2=0,3 м3/кг; P2=6,4 бара.
Тоді
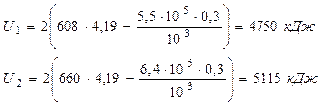
Qυ = U2 - U1 = 5115 – 4750 = 365кДж.
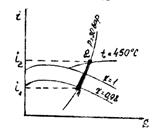
Приклад 11. Визначте кількість теплоти, що витрачається на перегрів 5 кг вологої насиченої пари із ступенем сухості x=0,98 при Р=const=30 бар до температури t= 450 °С.
Рішення. По I-S- діаграмі водяної пари знаходимо:
i1 = 660 ккал/кг; i2 = 798 ккал/кг.
 Тоді Qp=M(i2-i1) = 5·4,19(798-660) = 2880 кДж.
Тоді Qp=M(i2-i1) = 5·4,19(798-660) = 2880 кДж.
Приклад 12. 1кг вологої насиченої пари при P1=15 бар і x1= 0,8 изотермічно розширюється до P2= 8 бар. Визначте кількість теплоти, зміну внутрішньої енергії і роботу розширення.
Рішення. По I-S- діаграмі знаходимо:
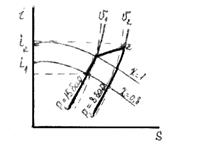 v1 = 0,105 м3/кг; v2 = 0,25 м3/кг;
v1 = 0,105 м3/кг; v2 = 0,25 м3/кг;
i1 = 573 ккал/кг; i2 = 676 ккал/кг;
S1 = 1,34 ккал/(кг·град);
S2 = 1,62 ккал/(кг·град).
Кількість теплоти:
Q = T(S2-S1) = (198 + 273)·(1,62 - 1,34)·4,19 = =552 кДж/кг.
Внутрішня енергія в початковому стані:
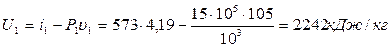 .
.
Внутрішня енергія в кінцевому стані:
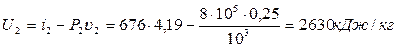 .
.
Робота розширення
і = q – ΔU = 552 – (2630-2242) 552 – 388 = 164 кДж/кг.
Переглядів: 3133