
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
ПРИКЛАДИ РОЗВ’ЯЗУВАННЯ ЗАДАЧ
1. Маса атома Карбону дорівнює 1,993×10-26 кг, маса атома Сульфуру – 5,3238×10-26. Розрахувати відносну атомну масу Сульфуру.
Розв’язання
1/12 ma(C12)= 1,66×10-27 кг
 .
.
Таким чином, відносна атомна маса Сульфуру становить 32,06.
2. Обчислити молярну масу сірки, якщо середня маса її молекули дорівнює 5,3238×10-23 г.
Розв’язання
M(S) = ma×NA = 5,3238×10-23г × 6,022×1023 моль-1 = 32,06 г/моль.
Таким чином, молярна маса сірки дорівнює 32,06 г/моль.
3. Визначити еквівалентні числа для хлору, азоту, вуглецю та фосфору, застосовуючи масові співвідношення, наведені далі:
| Реакція H2 + A | m(H2) : m(A) | Реакція A + O2 | M(A) : m(O2) |
| H2 + Cl2 = 2HCl | 1 : 35,5 | 2H2 + O2 = 2H2O | 1 : 8 |
| 3H2 + N2 = 2NH3 | 1 : 4,7 | C + O2 = CO2 | 3 : 8 |
| 2H2 + C = CH4 | 1: 3 | P4 + 5O2 = P4O10 | 6,2 : 8 |
Розв’язання
Для хлору реальна частинка (молекула) має масу M(Cl2)=71, у даній реакції m(Cl2) = 35,5, тобто це вдвічі менше за реальну частинку. Таким чином, z(Cl2)=2.
Для азоту М(N2) = 28; 28/4,7 = 6, таким чином, z(N2) = 6.
M(C) = 12; 12/3 = 4, z(C) = 4.
M(O2) = 32; 32/8 = 4, z(O2) = 4.
M(P4)= 124; 124/6,2=20, z(P4)=20.
Таким чином, еквівалентні числа для хлору, азоту, вуглецю та фосфору дорівнюють відповідно 2, 6, 4, 20 .
4. Визначити масову частку Карбону в метані.
Розв’язання
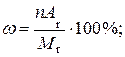
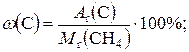
Ar(C) = 12;
Mr(CH4) = 12 + 4×1 = 16;
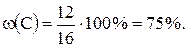
Таким чином, масова частка Карбону в метані становить 75%.
5. Визначити число атомів Оксигену, що містяться в 320 г кисню.
Розв’язання
n(O2) = 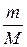 ; n(O2) =
; n(O2) =  =10 моль;
=10 моль;
n(O) = 2n(O2) = 2×10 моль = 20 моль;
N(O) = n(O)×NA = 20 моль×6,02×1023 моль-1 = 1,204×1025.
Таким чином, число атомів Оксигену становить 1,204×1025.
6. Відносна густина пари речовини за повітрям становить 2. Визначити молярну масу цієї речовини.
Розв’язання
Dпов.=  ; M=Dпов.×М(пов.).
; M=Dпов.×М(пов.).
М(пов.) = 29 г/моль ; M = 2 × 29 г/моль = 58 г/моль.
Таким чином, молярна маса речовини 58 г/моль.
7. Обчислити, скільки молекул і атомів міститься в 11,2 л гідроген сульфуру за нормальних умов.
Розв’язання
N(H2S) = n(H2S)×NA; n(H2S) =  ;
;
n(H2S) = 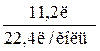 = 0,5 моль.
= 0,5 моль.
N(H2S) = 0,5 моль×6,02×1023 моль-1 = 3,01×1023 молекул.
Кожна молекула гідроген сульфіду містить 2 атоми Гідрогену і 1 атом Сульфуру, тобто кількість атомів у молекулі втричі більша.
Naтомів(H,S) = N(H2S) ×3 = 3×3,01×1023 =9,03×1023 атомів.
Таким чином, кількість молекул - 3,01×1023 ; кількість атомів – 9,03×1023 .
8. Визначити густину за воднем газової суміші, що складається з азоту об’ємом 56 л та неону об’ємом 28 л. Об’єми газів зведені до нормальних умов.
Розв’язання
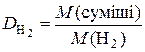 ;
;
Визначимо молярну масу суміші:
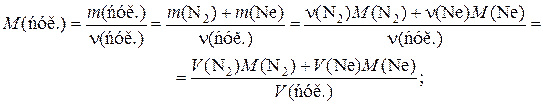
M(сум.) =  .
.
Таким чином,  .
.
9. Визначити атомну масу двовалентного металу та встановити цей метал, якщо його 8,34 г окиснюється 0,680 л кисню (н.у.).
Розв’язання
Згідно із законом еквівалентів 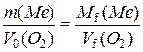 .
.
Молярну масу еквівалента металу можна знайти так:
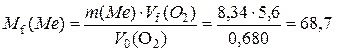 г/моль.
г/моль.
Оскільки метал двовалентний, то його атомна маса обчислюється за формулою А=Mf(Me)×2. Отже, атомна маса металу дорівнює 68,7×2=137.
Таким чином, шуканий метал - барій.
10. Визначити молярну масу речовини, якщо 600 мл її пари при 87°С і тиску 83,2 кПа дорівнює 1,30 г.
Розв’язання
Із рівняння Менделєєва-Клапейрона можна виразити молярну масу речовини:
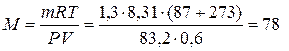 г/моль.
г/моль.
Таким чином, молярна маса речовини дорівнює 78 г/моль.
11. Написати рівняння реакцій, що характеризують такі перетворення:
SO2®Na2SO3®NaHSO3®Na2SO3®Na2SO4.
Розв’язання
У ході пропускання SO2 через надлишок розчину натрій гідроксиду утворюється натрій сульфіт:
SO2 + 2NaOH ® Na2SO3 + H2O.
Під час пропускання надлишку SO2 через розчин натрій сульфіту утворюється натрій гідрогенсульфіт:
SO2 + Na2SO3 + H2O ® 2NaHSO3.
Натрій гідрогенсульфіт у процесі нагрівання розкладається:
2NaHSO3 ® SO2 + Na2SO3 + H2O.
Сульфатна кислота витісняє сульфітну кислоту із сульфітів:
Na2SO3 + H2SO4 ® Na2SO4 + SO2 + H2O.
Читайте також:
- I. Застосування похідної та інтеграла до роз’язування задач елементарної математики.
- А) Задачі, що розкривають зміст дій
- АВТОМАТИЗАЦІЯ РОЗВ’ЯЗУВАННЯ КОМПЛЕКСУ ЗАДАЧ З ОБЛІКУ ОСНОВНИХ ЗАСОБІВ ТА НЕМАТЕРІАЛЬНИХ АКТИВІВ
- Алгоритм розв’язання задачі
- Алгоритм розв’язання задачі
- Алгоритм розв’язання розподільної задачі
- Алгоритм розв’язування задачі
- Алгоритм розв’язування задачі
- Алгоритм розв’язування задачі
- Алгоритм розв’язування задачі
- Алгоритм розв’язування задачі
- Алгоритм розв’язування задачі
| <== попередня сторінка | | | наступна сторінка ==> |
| Класами неорганічних сполук | | | Задачі для самостійного розв’язування |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |