
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Будова атома. Постулати Бора.
Сучасна модель атома базується на планетарні моделі Бора, яка була запропонована після відкриття субатомних частинок та ряду інших досліджень таких як радіоактивність, створення квантової теорії світла. Атом - мікрочастинка, яка складається з ядра, що вміщує протони і нейтрони, і електронів, які утворюють зовнішню оболонку. Хімічний елемент - вид атомів з однаковим зарядом ядра. Ізотоп - вид атомів з однаковим масовим числом. Масове число - загальна кількість протонів і нейтронів, що входять до ядра.
Квантові числа - параметри, що визначають електронну структуру і властивості електронів атома.n - головне квантове число; визначає енергетичний рівень і енергію електрона
n = 1, 2, ...[1]... ¥; l - орбітальне квантове число; визначає енергетичний підрівень, форму орбіталі і енергію електрона l = 0, 1, ...[1]... n-1; 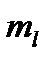 - магнітне квантове число; визначає просторову орієнтацію атомних орбіта лей.
- магнітне квантове число; визначає просторову орієнтацію атомних орбіта лей. 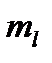 = -1... [1]...+1;
= -1... [1]...+1; 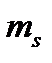 - спінове квантове число; визначає власний механічний і магнітний момент електрона.
- спінове квантове число; визначає власний механічний і магнітний момент електрона. 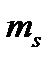 = -1/2 або +1/2. Кількість енергетичних підрівнів на енергетичному рівні дорівнює n. Електронна ємність енергетичного рівня дорівнює
= -1/2 або +1/2. Кількість енергетичних підрівнів на енергетичному рівні дорівнює n. Електронна ємність енергетичного рівня дорівнює 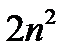 . Кількість орбіталей на енергетичному підрівні дорівнює 2l + 1.
. Кількість орбіталей на енергетичному підрівні дорівнює 2l + 1.
Електронна ємність енергетичного підрівня дорівнює 2·(2l + 1)
Нільс Бор спробував пояснити будову атома, сформулювавши два постулати:
1. Атом або система атомів може знаходитись не в усіх станах, що дозволяє класична механіка, а тільки в деяких певних (надалі - квантових) станах, що мають дискретні значення енергії Е1, Е2, Е3 тощо. В цих станах атом не випромінює. Усі можливі такі стани назвемо стаціонарними.
2. При переході зі стаціонарного стану з енергією Еn2 до стаціонарного стану з енергією En1, енергія атома змінюється на Еn2 - En1. Якщо такий перехід вввідбувається внаслідок випромінювання (поглинання), то при цьому випускається (поглинається) один фотон з енергією. hn = En2 – En1
| <== попередня сторінка | | | наступна сторінка ==> |
| Період, частота коливань. Зв’язок між ними. | | | Довжина хвилі, зв’язок з частотою коливань. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |