
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Теорія Бора для воднеподібних атомів
В теорії Бора вважається, що рух електрона по стаціонарній орбіті відбувається за законами класичної механіки. Оскільки маса m електрона значно менша від маси ядра атома, можна вважати ядро нерухомим. Розмістимо ядро в початку системи координат.
Запишемо другий закон Ньютона для електрона, який обертається навколо ядра по круговій орбіті радіуса r:
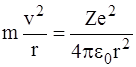 . (3)
. (3)
Потенціальну енергію електрона на відстані r будемо вважати рівною нулю. При таких умовах повна енергія Е електрона на відстані r від ядра буде дорівнювати
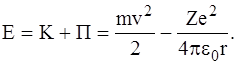 (4)
(4)
Рівняння (2), (3), (4) утворюють систему, розв’язавши яку відносно r та Е, можна знайти радіуси стаціонарних орбіт та значення енергії атома у відповідних стаціонарних станах. Для цього, виключаючи швидкість v з (2) та (3), знайдемо радіуси орбіт:
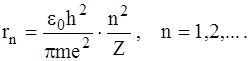 (5)
(5)
В формулі (5) кожному значенню числа n відповідає певне значення rn радіуса стаціонарної орбіти.
Для визначення енергії En стаціонарних станів атома виключимо v2 з рівнянь (3) та (4) і в одержане таким чином співвідношення:
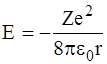 ,
,
підставимо замість r значення rn з формули (5). Після очевидних перетворень приходимо до виразу:
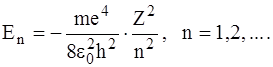 (6)
(6)
Ми одержали дискретний ряд значень енергії – набір енергетичних рівнів атома.
При Z = 1 та n = 1 формули (5) та (6) приводять до значень r1 та E1 – радіуса першої, найближчої до ядра, стаціонарної орбіти в атомі водню та енергії атома водню у найнижчому енергетичному стані, який називають основним станом. Величину r1 = 0,529· 10–10 м називаютьборівським радіусом,а Е1–енергієюосновного стану атома водню. Легко бачити, що, використовуючи значення r1 та E1, формули (5) та (6) можна подати у вигляді:
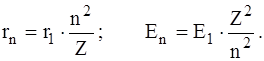
В атомній фізиці при вимірюваннях енергії користуються більш зручною, аніж джоуль, позасистемною одиницею – електрон-вольт (1 еВ = 1,6· 10–19 Дж). В цих одиницях Е1 = – 13,6 еВ.
Отже, радіуси стаціонарних орбіт, а такоженергетичні рівні атома водню та будь-якого воднеподібного атома легко розраховуються через борівський радіус та енергію основного стану атома водню.
Від’ємні значення енергії стаціонарних станів обумовлені вищезгаданим способом відліку потенціальної енергії електрона в полі ядра.
1.3 Спектри випромінювання воднеподібних атомів.
Формула Бальмера – Рідберга
Для визначення частот 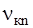 спектральних ліній випромінювання воднеподібних атомів звернімося до рівняння частот (див. другий постулат). Підставимо в (1) замість величин Ек та Еn їхні значення згідно (6). Одержимо:
спектральних ліній випромінювання воднеподібних атомів звернімося до рівняння частот (див. другий постулат). Підставимо в (1) замість величин Ек та Еn їхні значення згідно (6). Одержимо:
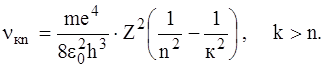
Скориставшись співвідношенням 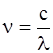 між частотою та довжиною хвилі (с – швидкість світла у вакуумі), останню формулу можна перетворити до вигляду:
між частотою та довжиною хвилі (с – швидкість світла у вакуумі), останню формулу можна перетворити до вигляду:
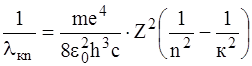
або
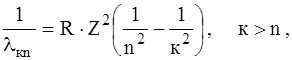 (7)
(7)
де
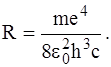 (8)
(8)
Величина R називається сталою Рідберга (R = 1,097· 107 м–1).
Формула (7), одержана Бором теоретично, була встановлена експериментально у 1885 р. за результатами спектральних вимірювань і відома як формула Бальмера – Рідберга.
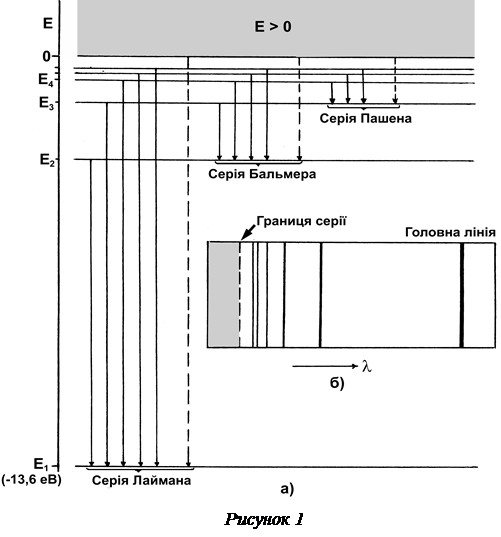
Для з’ясування деяких важливих понять, які використовуються при обговоренні атомних спектрів випромінювання, розглянемо діаграму енергетичних рівнів атома водню (рисунок 1, а). Дискретні значення енергії атома Е1, Е2, … показані на схемі горизонтальними лініями. Згідно (5) та (6), чим більше n, тим далі від ядра знаходиться електрон і тим вище лежить відповідний рівень енергії на діаграмі. Загалом в атомі існує нескінченна кількість можливих стаціонарних станів між основним рівнем Е1 = –13,6 еВ і рівнем Е∞ = 0, який відповідає стану іонізації атома водню (при n радіус rn ). Енергію іонізації водню Еі, тобто мінімальну енергію, потрібну для вилучення електрона з атома водню, який перебував в основному стані, легко знайти:
 Еі = Е – Е1; Еі = – Е1 = 13,6 еВ.
Еі = Е – Е1; Еі = – Е1 = 13,6 еВ.
Область енергій Е < 0 на діаграмі відповідає електрону, який знаходиться на одній з стаціонарних орбіт в атомі, тобто перебуває у зв’язаному стані. В цій області енергія електрона змінюється дискретно. В області енергій Е > 0 електрон втрачає зв’язок з ядром атома, стає вільним електроном, і його енергія може набувати довільних значень.
При відсутності зовнішніх впливіватом перебуває в основному стані. Всі енергетичні рівні атома, крім основного, називаються збудженими, оскільки для переходу на них атому необхідно надати певну енергію = Еn – Е1 – енергію збудження. Таку енергію атом може одержати, поглинувши квант випромінювання відповідної частоти від зовнішнього джерела (радіаційне збудження), або внаслідок непружного зіткнення з іншим атомом або електроном (збудження ударом). Час існування атома в збуджених станах (час життя) t ~ 10–8 с, після чого атом сам собою (спонтанно) переходить на один з розташованих нижче енергетичних рівнів, висвітлюючи квант випромінювання, частота якого, згідно (7), залежить від номерів к та n верхнього та нижнього рівнів.
Спектр атома водню поділяється на відокремлені групи спектральних ліній, які мають схожий вигляд, але розташовані в різних областях довжин хвиль. Такі групи називають спектральними серіями. В спектрі випромінювання лінії даної спектральної серії виникають при всіх квантових переходах з різних початкових збуджених рівнів на один, спільний, кінцевий рівень і “сходяться” до границі серії, яка має мінімальну для даної серії довжину хвилі (рисунок 1, б). Кожна серія починається з головної лінії – першої і найбільш яскравої спектральної лінії в даній серії. Перші три серії спектра водню такі:
Серія Лаймана була відкрита у 1906 р. в ультрафіолетовій області спектра. Спектральні лінії серії Лаймана виникають при переходах атома з будь-яких збуджених станів у основний стан. У формулі (7) цим переходам відповідають значення n = 1 та к = 2, 3, …
Серія Бальмера відкрита першою у 1885 р. Утворена переходами атома на перший збуджений енергетичний рівень n = 2 з усіх розташованих вище рівнів (к = 3, 4, …). Серія Бальмера починається у видимій області і закінчується у ближній ультрафіолетовій області
Серія Пашена (n = 3, к = 4, 5, …) відкрита у 1908 р. і лежить у інфрачервоній області спектра.
| <== попередня сторінка | | | наступна сторінка ==> |
| Постулати Бора. Походження лінійчатих спектрів | | | ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |