
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Кислотно-основні індикатори
Індикаторами називаються речовини, які під час додавання у невеликих кількостях в аналізований розчин дозволяють встановити кінець титрування за зміною забарвлення, утворенням каламуті, флуоресценцією розчину тощо.
Індикатори поділяються на:
- внутрішні, які вводяться в розчин;
- зовнішні, які змішуються з краплею розчину за межами реакційної суміші;
- зворотні, які здатні змінювати забарвлення в обох напрямках;
- незворотні, які змінюють забарвлення тільки один раз, оскільки їх молекули руйнуються.
За типом реакцій, які використовуються для аналізу, індикатори поділяються на:
- кислотно-основні;
- окисно-відновні;
- комплексонометричні (металохромні);
- адсорбційні.
Кислотно-основнi iндикатори змiнюють свiй колiр залежно вiд зміни рН розчину. За хiмiчною природою кислотно-основні індикатори є слабкими органічними кислотами або основами, якi частково дисоцiюють в розчинi, наприклад
HInd « H+ + Ind–,
де HInd - недисоцiйована молекула; Ind– - анiон iндикатора.
До кислотно-основних індикаторів ставляться такі вимоги:
- забарвлення обох форм індикатора повинно різко відрізнятися;
- забарвлення індикатора повинно бути інтенсивним;
- зміна забарвлення індикатора має відбуватися у вузькому інтервалі рН;
- кількість реагента, яка приводить до зміни кольору індикатора, повинна бути мінімальною;
- бажано, щоб індикатор був зворотним.
Інтервал pH, у якому індикатор змінює свій колір, називають інтервалом переходу індикатора.
Важливою характеристикою iндикатора є показник титрування pT - значення рН, за якого спостерiгається найбільш чітка змiна забарвлення і за якого закiнчують титрування:
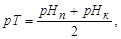 (5.1)
(5.1)
де рНп і рНк - початкове та кінцеве значення інтервалу зміни забарвлення індикатора.
Переглядів: 342