
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Добуток розчинності та розчинність малорозчинних сполук
Рiвновагу для малорозчинної сполуки MpXq з її насиченим розчином, в якому сполука дисоцiює повністю, можна виразити стехiометричним рiвнянням мiжфазної рiвноваги:
MpXq (тв.) « pMq+ (р.) + qXp– (р.).
В насиченому розчині малорозчинної речовини добуток активностей йонів у степені їх стехіометричних коефіцієнтів є величиною постійною при даній температурі і називається добутком розчинності ДР.
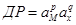 . (8.1)
. (8.1)
Добуток розчинностi малорозчинної сполуки MpXq, яка дисоцiює повнiстю, зв'язаний з її розчинністю (S) простим спiввiдношенням:
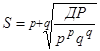 , (8.2)
, (8.2)
Підвищення розчинності малорозчинних сполук у присутності сильних електролітів, які не мають спільних йонів з осадом і не вступають з ним в реакції, називають солевим ефектом.
Переглядів: 394