
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Атом водню і його спектр за теорією Бора
Дослідження спектрів випромінювання розріджених газів, показали, що
кожному газу властивий певний лінійчастий спектр, який складається з окремих спектральних ліній. Найбільш вивченим є спектр атома водню.
Швейцарський вчений І. Бальмер у 1885 р. встановив, що довжини хвиль відомих на той час дев’яти ліній спектра атома водню можна обчислити за формулою:
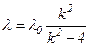 ,
,
де 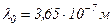 ,
, 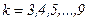 .
.
Цю формулу можна записати в іншому вигляді:
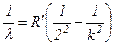 ,
, 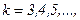
де 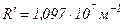 ,
, 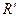 – стала Рідберга.
– стала Рідберга.
Оскільки 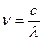 , то
, то
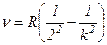 ,
,
де 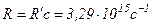 , яку також називають сталою Рідберга.
, яку також називають сталою Рідберга.
На початку ХХ ст. у спектрі водню було виявлено ще декілька серій спектра випромінювання, які знаходяться у невидимій області.
В ультрафіолетовій області – серія Лаймана:
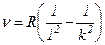 ,
, 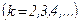 ;
;
в інфрачервоній області – серія Пашена:
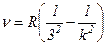 ,
, 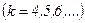 ;
;
серія Брекета:
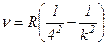 ,
, 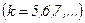 ;
;
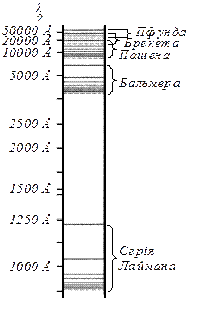 серія Пфунда:
серія Пфунда:
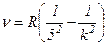 ,
, 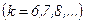 ;
;
серія Хемфрі:
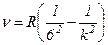 ,
, 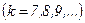 .
.
Всі серії у спектрі водню можуть бути описані однією формулою, яка називається узагальненою формулою Бальмера:
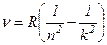 ,
,
де n=1, 2, 3, 4, 5, 6, і визначає серію, а k=n+1, n+2, n+3,… і визначає окремі лінії серії.
Теорія Бора застосовна до атома
водню і воднеподібної системи, яка складається з ядра з зарядом 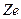 і одного електрона, що обертається навколо ядра:
і одного електрона, що обертається навколо ядра: 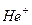 ,
, 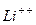 ,….
,….
В основу своєї теорії Бор поклав три постулати.
Перший постулат Бора (постулат стаціонарних станів): існують деякі стаціонарні стани атома з відповідними значеннями енергії 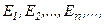 перебуваючи в яких, він не випромінює енергії.
перебуваючи в яких, він не випромінює енергії.
Цим стаціонарним станам відповідають цілком визначені (стаціонарні) орбіти, по яких рухаються електрони, які, незважаючи на наявність у них прискорення, електромагнітних хвиль не випромінюють.
Другий постулат Бора (правило квантування орбіт): в стаціонарному стані атома електрон, рухаючись по коловій орбіті, повинен мати квантові значення моменту імпульсу, які задовольняють умову
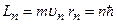 ,
, 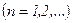 ,
, 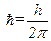 ,
,
де m – маса електрона, 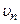 – його швидкість,
– його швидкість, 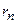 – радіус орбіти електрона.
– радіус орбіти електрона.
Третій постулат Бора (правило частот): при переході атома з одного стаціонарного стану в інший випромінюється або поглинається один фотон з
енергією 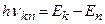 , яка дорівнює різниці енергій відповідних стаціонарних станів.
, яка дорівнює різниці енергій відповідних стаціонарних станів.
Враховуючи припущення Резерфорда, що електрон у воднеподібній системі рухається по коловій орбіті радіусом r під дією кулонівської сили притягання електрона до ядра, яка створює доцентрове
прискорення, запишемо:
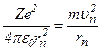 .
.
Звідси
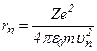 .
.
Підставивши сюди величину 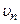 з виразу
з виразу 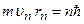 , отримаємо:
, отримаємо:
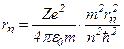 і
і 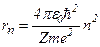 ,
,
де n=1, 2, 3,…
Радіуси орбіт зростають пропорційно квадратам цілих чисел.
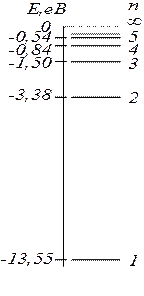 Для атома водню (Z=1) радіус першої орбіти електрона при n=1 називається першим борівським радіусом
Для атома водню (Z=1) радіус першої орбіти електрона при n=1 називається першим борівським радіусом 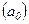 і дорівнює
і дорівнює
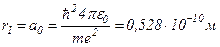
Тоді
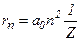 .
.
Оскільки експериментально виміряти радіуси орбіт неможливо, то для перевірки правильності теорії потрібно знайти такі величини, які можна виміряти експериментально. Такою величиною може бути, зокрема, енергія, яку випромінюють або поглинають атоми.
Енергія електрона у воднеподібній системі дорівнює сумі його кінетичної і потенціальної енергій в електростатичному полі ядра:
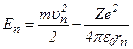 .
.
Врахувавши, що 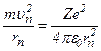 ,
,
отримаємо:
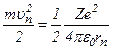 .
.
Тоді
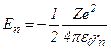 .
.
Підставимо в цей вираз значення 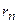 . Тоді
. Тоді
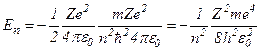 .
.
Знак „–“ означає, що електрон знаходиться у зв’язаному стані.
Енергетичні стани атома утворюють сукупність енергетичних рівнів, що змінюються залежно від значення n, яке виражає номер енергетичного рівня атома і називається головним квантовим числом. Енергетичний стан з n=1 є основним станом, а стани з n>1 – збуджені.
Надаючи n різні цілочислові значення, отримаємо для атома водню (Z=1) можливі рівні енергії (рис. 285). Енергія атома водню із збільшенням n зростає (зменшується її від’ємна величина), і енергетичні рівні наближаються до границі, що відповідає значенню 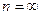 . Атом водню має мінімальну енергію
. Атом водню має мінімальну енергію 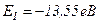 при n=1 і максимальну
при n=1 і максимальну 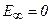 при
при 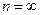 . Отже, значення
. Отже, значення 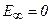 відповідає енергії іонізації атома (відриву від нього електрона). Енергія іонізації з певного стану дорівнює за абсолютною величиною енергії зв’язку електрона в атомі в цьому стані
відповідає енергії іонізації атома (відриву від нього електрона). Енергія іонізації з певного стану дорівнює за абсолютною величиною енергії зв’язку електрона в атомі в цьому стані 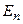 .
.
Згідно з третім постулатом Бора при переході електрона з k-ї орбіти на n-у випромінюється фотон з енергією
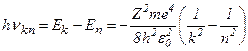 ,
,
звідки частота випромінювання
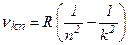 ,
,
де 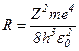 - стала Рідберга. Числове значення
- стала Рідберга. Числове значення 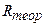 добре узгоджується з експериментально отриманим
добре узгоджується з експериментально отриманим 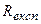 в емпіричних формулах для атома водню. Це підтверджує правильність отриманої Бором формули для енергетичних рівнів водневоподібної системи.
в емпіричних формулах для атома водню. Це підтверджує правильність отриманої Бором формули для енергетичних рівнів водневоподібної системи.
Переглядів: 5397