
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Крива рівноваги на трикутній діаграмі
Процеси змішування в трикутній діаграмі, правило важіля
При змішуванні двох трикомпонентних розчинів складів R і Е (рис. 10.4.1,б) утворюється потрійна суміш, склад котрої характеризується точкою N, яка лежить на прямій RE, яка з'єднує вихідні склади. Положення точки N на прямій знаходять по правилу ричага, якщо відомо кількості взятих розчинів R і Е
(кількість R)/( кількість E) = EN/RN (11.5.1)
Звідки випливає, що якщо суміш N будь-яким методом розкласти на дві фракції R і Е, то точки R, Е і N, які відповідають цим трьом сумішам, повинні лежать на прямій RNE. Якщо відомо кількість суміші N, її склад і склади фракцій після розділення суміші, то легко знайти кількість цих фракцій по виразам:
(кількість R)/(кількість N) = EN/(RN+EN) = EN/RE (11.5.2)
(кількість Е)/( кількість N) = RN/(RN+EN) = RN/RE (11.5.3)
Трикутна діаграма (рис.10.6.1) може бути використана для зображення рівноваги в потрійних системах координат рідина - речовини, що розподіляється - рідина. Аби отримати уявлення про рівновагу в потрійних системах, розглянемо процес додавання речовини М, що розподіляється, до гетерогенної суміші двох розчинників L і G. Нехай речовина М, що розглядається, необмежено розчиняється в обох розчинниках L і G, а самі розчинники L і G мають обмежену взаємну розчинність.
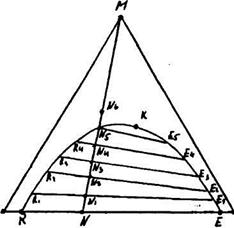
Рис. 11.6.1. Крива рівноваги на трикутній діаграмі.
З трикутної діаграми, яку представлено на рис.11.6.1, видно, що якщо М і L а також М і G утворюють однорідні двокомпонентні розчини, склад котрих характеризується точками на сторонах діаграм LМ і GM, то розчинним L і G утворюють однорідні розчини лише на невеликих ділянках LR і EG. Будь-яка суміш розчинників на ділянці RE розшаровується на два однорідних двокомпонентних насичених розчина R (насичений розчин G в L) і Е (насичений розчин L в G). Кількість насичених розчинів в кожному з двох шарів, що утворилися, залежить від положення точки N , яка виражає середній склад двофазної системи, і може бути визначена по правилу ричага з виразів (11.5.1) - (11.5.3).
При додаванні речовини М, що розподіляється, в суміш склaду N отримуємо потрійну суміш, склад котрої характеризується точкою N1, яка лежить на прямій змішyвання NM. Суміш складу N1 розшаровується на дві фази з рівноважними складами R1 (фаза розчинника L) і Е1 (фаза розчинника G) в кількісному співвідношенні E1N1:R1N1.
При додаванні в суміш наступних порцій М2, М3,... отримаємо ряд потрійних сумішей
складу N2, N3, .... котрі, як видно в попередньому випадку, розшаровуються на рівноважні
потрійні суміші складу R2 і Е2, R3 і Е3 і т.д. Як видно з діаграми, змінюються і вагові
співвідношення рівноважних розчинів до моменту, коли одна з фаз щезає (в нашому випадку при N5). При ще більшому розвeденні компонентом, що розподіляється, маємо лише однорідні потрійні розчини складу N6 і інші.
З'єднавши R1 і Е1, R2 і E2, ... лініями, отримаємо хорди рівноваги R1 E1, R2 Е2 які з'єднують на діаграмі рівноважні склади. Хорди рівноваги, зменшуючись, сходяться в точці К, яка зветься критичною.
З'єднавши точки, які відповідають рівноважним складам, плавною кривою RR1R2 ... К ... Е2Е1Е, отримаємо криву рівноваги , або так звану бінодальну криву, одна гілка RK котрої характеризує рівноважні склади фази розчинника L, а друга ЕК - рівноважні склади фази розчинника G.
Бінодальна крива на трикутній діаграмі обмежує площу, яка відповідає двофазним сумішам; площа діаграми поза кривою відповідає однофазним розчинам. Для процесу екстракції цікавість являє лише зона двофазних розчинів.
По трикутній діаграмі легко знайти коефіцієнт розподілення ψ для будь-якої пари рівноважних розчинів. Так як для двох розчинів R і Ε (рис. 11.6.2) коефіцієнт розподілення ψ дорівнює:
ψ = (концентрація М в фазі F)/( концентрація М в фазі R) (11.6.1)
причому величина ψ може бути більше одиниці (рис. 11.6.2,а), менше одиниці (рис. 11.6.2,б) або рівна одиниці (рис. 11.6.2,в).
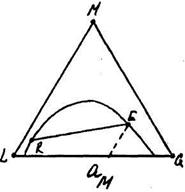
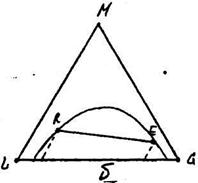
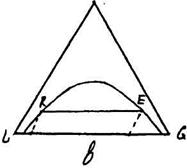
ψ>1 ψ<1 ψ=1
Рис. 11.6.2. До розрахунку коефіцієнта розподілення.
Нахил хорди рівноваги визначається природою компонентів і складом фаз.
Читайте також:
- Альтернативні уявлення щодо макроекономічного регулювання: теорії раціональних сподівань та економіка пропозиції. Крива Лафера.
- Аналіз загальної рівноваги
- Аналіз часткової рівноваги Крива виробничих можливостей
- Аналіз часткової та загальної рівноваги
- Аналіз часткової та загальної рівноваги
- Будь – які зміни популяції є результатом порушення рівноваги між її біотичним потенціалом та опором довкілля.
- Видатки та заощадження як функції доходу. Автономні величини та їх чинники. Крива планових видатків.
- Визначати ступінь відповідності обраної регресії відображуваним на діаграмі даним.
- Визначення стрілок на контекстній діаграмі
- Вплив держави на встановлення ринкової рівноваги
- Вплив тиску на положення рівноваги
- Вплив тиску на положення рівноваги
| <== попередня сторінка | | | наступна сторінка ==> |
| Зображення процесів розведення на трикутній діаграмі | | | Находження хорд рівноваги і критичної точки |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |