
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Кінетична класифікація гомогенних хімічних реакцій
З точки зору хімічної кінетики усі елементарні реакції можна класифікувати на реакції нульового, першого, другого та третього порядків. На відміну від молекулярності порядок реакції – величина формальна і дорівнює сумі показників степенів у кінетичному рівнянні. Із співвідношення (9.5) загальний порядок n даної реакції дорівнює
n = nA + nB + nD.
При цьому величини nA, nB, nD називаються приватними порядками реакціїза речовинамиА, В і D. Отже, загальний порядок реакції n дорівнює сумі приватних порядків.
Для елементарних реакцій nA = a , nB = b, nD = d.
Можливі такі типи кінетичних рівнянь елементарних реакцій:
n = 1 A  продукти W = kCA;
продукти W = kCA;
n = 2 2A  продукти W = kCA2;
продукти W = kCA2;
A1 + A2  продукти W = k×C(A1)×C(A2);
продукти W = k×C(A1)×C(A2);
n = 3 3A  продукти W = kCA3;
продукти W = kCA3;
2A1 + A2  продукти W = k×C2(A1)×C(A2);
продукти W = k×C2(A1)×C(A2);
A1 + A2 + A3  продукти W= k×C(A1)×C(A2)×C(A3);
продукти W= k×C(A1)×C(A2)×C(A3);
n = 0 A  продукти W = k.
продукти W = k.
Реакції нульового порядку – це реакції, які проходять при надлишку реагентів так, що змінювання концентрації не впливає на швидкість реакції.
Знайдемо основні кінетичні характеристики і рівняння для гомогенних хімічних реакцій різного порядку у закритих системах при постійності об¢єму та температури.
1 Реакції нульового порядку.Такі реакції трапляються рідко. Прикладом реакції нульового порядку є реакція розкладання N2O5 у газовій фазі за наявності твердого N2O5, коли постійна концентрація реагенту у газовій фазі підтримується сталою за рахунок випарювання твердого оксиду. Для реакцій нульового порядку
W = 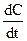 = k. (9.6)
= k. (9.6)
Розв¢яжемо це рівняння, розділивши змінні
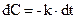
Після інтегрування 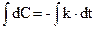 отримаємо
отримаємо
С = - k∙t + B,
де В – константа інтегрування. Знайдемо її, ураховуючи початкову умову у момент t = 0 концентрація дорівнює початковій С = С0, звідси С0 = В і
С = С0 – k∙t. (9.7)
Отже, у реакціях нульового порядку концентрація лінійно зменшується з часом (рис. 9.2,а).
Константу швидкості реакції нульового порядку можна обчислити за рівнянням
k =  (C0 – C). (9.8)
(C0 – C). (9.8)
Iї розмірність (моль/л)×с-1).
Поряд з константою швидкості для характеристики реакцій часто використовують величину, що називається часом напівперетворення t1/2 .
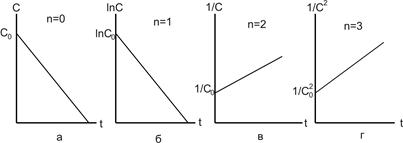
Рисунок 9.2 – Змінювання концентрації з часом у реакціях нульового (а), першого (б), другого (в) і третього (г) порядків
Час напівперетворення- проміжок часу, за який реагує половина вихідної кількості речовини, тобто при t = t1/2
C = C0/2 звідси
С0/2 = С0 - kt1/2 i
t1/2 = 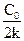 . (9.9)
. (9.9)
Отже, для реакції нульового порядку час напівперетворення пропорційний початковій концентрації вихідної речовини.
2 Реакції першого порядку.До елементарних реакцій першого порядку належать реакції, які можна подати у вигляді
А  продукти.
продукти.
Частіше всього це реакції розкладання. Наприклад, реакція розкладання ацетону
СН3СОСН3  CH4 + CO + H2.
CH4 + CO + H2.
Кінетичне рівняння для реакцій першого порядку має вигляд

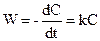 . (9.10)
. (9.10)
Проінтегруємо його, розділивши змінні:
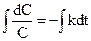 ,
,
ln C = - kt + B.
Для визначення постійної інтегрування припустимо, що у початковий момент реакції t = 0 концентрація вихідної речовини була С0, тоді
ln C0 = B,
отже, ln C = - kt + lnC0 , або
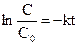 ,
,
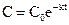 . (9.11)
. (9.11)
Це інтегральна форма кінетичного рівняння реакції 1-го порядку. Константа швидкості реакції першого порядку має розмірність (с)-1. Величина, зворотна константі швидкості реакції першого порядку, має розмірність часу і називається середньою тривалістю життя окремої частинки.
Для реакції першого порідку характерна лінійна залежність lnC від t (рис. 9.2,б).
Знайдемо час напівперетворення для реакції першого порядку. Для t = t1/2 C = C0 /2.
Тому

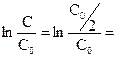 - kt1/2
- kt1/2
kt1/2 = ln 2.
Звідси
t1/2 = 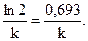 (9.12)
(9.12)
Бачимо, що час напівперетворення визначається виключно значенням константи швидкості. Так, для наведеної реакції розкладання ацетону k = 4,27 × 10-4 c-1. Отже,
t1/2 = 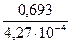 = 1580 с = 26 хв. 20 с.
= 1580 с = 26 хв. 20 с.
До істинно молекулярних або, краще сказати, моноатомних процесів першого порядку відносять усі численні перетворення радіоактивних речовин. У табл. 9.1 наведені деякі дані для таких реакцій.
Таблиця 9.1 – Кінетичні характеристики радіоактивного роз-
паду деяких ізотопів
| Ізотоп | k, c-1 | t1/2 |
| 222Ra 226Ra 238U 214Po | 2,1×10-6 1,35×10-11 4,88×10-18 4,62×103 | 3,8 доби 1620 років 4,5×109 років 1,5×10-4 с |
Класичним прикладом реакції першого порядку є реакція інверсії тростинного цукру (сахарози)
С12Н22О11 + Н2О 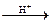 C6H12O6 + C6H12O6.
C6H12O6 + C6H12O6.
сахароза глюкоза фруктоза
Кінетичне рівняння цієї реакції має вигляд
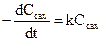
У реакції беруть участь ще вода та кислота (іони Н+), однак концентрація кислоти є постійною (іони Н+ - каталізатор), а концентрація води, що міститься у дуже великому надлишку, теж практично постійна. Реакція інверсії зручна для вивчення тим, що у ході її змінюється кут обертання площини поляризації. Сахароза обертає площину поляризації управо, а суміш глюкози та фруктози – уліво. Поміщаючи розчин сахарози у трубку поляриметра, можна стежити за проходженням реакції, не перериваючи її. При кінетичних розрахунках використовується пропорційний зв¢язок між кутом обертання та концентрацією обертальної речовини.
3 Реакції другого порядку. Реакції другого порядку проходять з участю двох частинок (молекул, атомів). Якщо у елементарній реакції беруть участь дві однакові частинки
2А  продукти,
продукти,
то кінетичне рівняння має вигляд
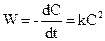 (9.13)
(9.13)
де С – концентрація речовини А. Інтегрування цього рівняння приводить до
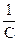 = kt + B.
= kt + B.
При t = 0 C = C0. Звідси В =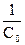 , отже,
, отже,
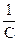 -
- 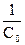 = kt (9.14)
= kt (9.14)
або
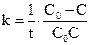 (9.15)
(9.15)
Для реакції другого порядку спостерігається лінійна залежність 1/с від t (рис. 10.2, в).
Розмірність константи швидкості реакції другого порядку (моль/л)-1×с-1, тобто на відміну від реакцій першого порядку у розмірності є не тільки час, але й концентрація. Тому для реакцій другого порядку ( та вище) не можна при розрахунках замінювати концентрацію на пропорційні неї їй величини.
Для реакції другого порядку
t1/2 = 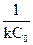 , (9.16)
, (9.16)
тобто чим більша початкова концентрація, тим менший час напівперетворення.
Якщо в елементарній реакції другого порядку реагують дві різні частинки
А1 + А2  продукти,
продукти,
причому концентрації речовин А1 та А2 різні, то
W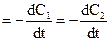 = kC1C2. (9.17)
= kC1C2. (9.17)
Враховуючи, що С1 = С10 – х та С2 = С20 – х, маємо
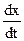 = k(C10 – x)(C20 – x),
= k(C10 – x)(C20 – x),
де С10 та С20 – початкові концентрації речовин А1 та А2,
х – зменшення їх концентрації у момент часу t.
Розв¢язок останнього рівняння дає
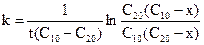 . (9.18)
. (9.18)
Реакцій другого порядку багато. Наприклад:
Н2 + І2(пар)  2HI,
2HI,
2HI  H2 + I2 (пар),
H2 + I2 (пар),

 О О
О О

 СН3С + NaOH
СН3С + NaOH  CH3C + C2H5OH та ін.
CH3C + C2H5OH та ін.
ОС2Н5 ОNa
4 Реакції третього порядку.Елементарні реакції третього порядку можна подати у вигляді:
3А  продукти,
продукти,
2A1+ A2  продукти,
продукти,
A1 + A2 + A3  продукти.
продукти.
Оскільки реакції третього порядку спостерігаються дуже рідко та не становлять значного практичного інтересу, розглянемо їх кінетику тільки для випадку рівності концентрацій усіх реагуючих речовин.
Тоді
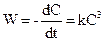 (9.19)
(9.19)
Та після інтегрування
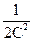 = kt + B.
= kt + B.
При t = 0 C = C0 та В =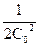 . Отже,
. Отже,
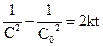 , (9.20)
, (9.20)
або
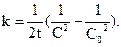 (9.21)
(9.21)
Константа швидкості реакції третього порядку має розмірність (моль/л)-2×с-1.
Для реакцій третього порядку лінійна залежність 1/С2=f(t) (рис. 10.2, г). Час напівперетворення для реакцій третього порядку обернено пропорційний квадрату концентрації
t1/2 = 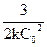 (9.22)
(9.22)
Прикладами реакцій третього порядку є
2NO + O2  2NO2,
2NO2,
2NO + Cl2  2NOCl.
2NOCl.
Слід зазначити, що реакції першого, другого та третього порядків є у той самий час моно-, бі- та тримолекулярними відповідно.
Для моделювання хіміко-технологічних процесів корисно ввести поняття формально простихреакцій. До формально простих реакцій відносять будь-які реакції, для яких кінетичне рівняння може бути подане наближено у вигляді степеневої залежності
W = kC1n(1) × C2n(2) × C3n(3) …
Наприклад, такою є складна реакція
3СН3ОН + 2Н2CrO4 + 6HCl  3CH2O + 2CrCl3 + 8H2O.
3CH2O + 2CrCl3 + 8H2O.
Для цієї реакції
W = kC(CH3OH) × C(H2CrO4) × C2(HCl).
Як бачимо, степенів для формально простої реакції не збігаються зі стехіометричними коефіцієнтами. У загальному випадку для таких реакцій показники степенів можуть бути дробовими і набувати значень, більших від трьох.
При рівності концентрацій реагуючих речовин кінетичне рівняння має вигляд
 (9.23)
(9.23)
Розв¢язання цього рівняння аналогічне попереднім і приводить до таких результатів:
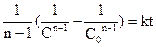 , (9.24)
, (9.24)
t1/2= 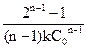 . (9.25)
. (9.25)
Константа швидкості має розмірність (моль/л)-(n-1) × (с)-1.
Читайте також:
- II. Класифікація видатків та кредитування бюджету.
- V. Класифікація і внесення поправок
- V. Класифікація рахунків
- А. Структурно-функціональна класифікація нирок залежно від ступеню злиття окремих нирочок у компактний орган.
- Адміністративні провадження: поняття, класифікація, стадії
- Аналітичні процедури внутрішнього аудиту та їх класифікація.
- Аналогія величин і рівнянь поступального і обертального руху. Кінетична енергія обертання тіла
- Банківська платіжна картка як засіб розрахунків. Класифікація платіжних карток
- Банківський кредит та його класифікація.
- Банківські ресурси, їх види та класифікація
- Будівельна класифікація ґрунтів
- Будівельні домкрати, їх призначення, класифікація та конструкція.
| <== попередня сторінка | | | наступна сторінка ==> |
| Речовин, піднесених до деяких ступенів. | | | Способи визначення порядку реакції |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |