
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
ЯВИЩА ПЕРЕНОСУ
ТЕМА: СТАТИСТИЧНИЙ РОЗПОДІЛ.
Лекція VIIІ
ПЛАН
1. Розподіл Максвелла.
2. Розподіл Больцмана.
3. Середнє число зіткнень і середня довжина вільного пробігу молекул.
4. Явища переносу.
1. В ідеальному газові швидкості молекул мають різні напрямки, а величини цих швидкостей безперервно змінюються. Тому неможливо визначити кількість молекул, які мають конкретну швидкість, але можна підрахувати кількість молекул, які володіють швидкістю в інтервалі від v1 до v2.
Це зробив англійський фізик Максвелл у 1859 році:
він розглянув газ як сукупність великої кількості однакових молекул, котрі знаходяться у стані термодинамічної рівноваги за відсутності зовнішнього силового поля.
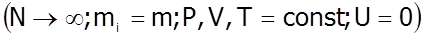
Застосувавши теорію ймовірності, він установив такий закон:
 (1)
(1)
- розподіл молекул за швидкостями Максвелла.
 - імовірність того, що швидкості молекул розташовані в інтервалі від v до v + dv при даній температурі Т.
- імовірність того, що швидкості молекул розташовані в інтервалі від v до v + dv при даній температурі Т.
 Т1
Т1









 | |||||
 |  | ||||
 | |||||
 | |||||
 | |||||
 | |||||
 | |||||




 v
v
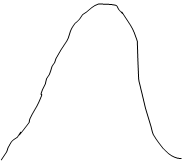
Із статистичного характеру розподілу молекул за швидкостями виходить:
1.Який би не був початковий розподіл молекул у термодинамічній рівноважній системі, завжди встановлюється розподіл Максвелла.
2. Якщо у системі вже встановився розподіл Максвелла, то він буде існувати нескінченно довго.
Заштрихована площа вказує на кількість молекул dN, які знаходяться в інтервалі швидкостей від v до v + dv.
Дослідивши на екстремум функцію (1), можна одержати ті значення швидкостей, при яких функція має максимум. Вони відповідають найбільш імовірній швидкості.
 (2)
(2)
Крива розподілу дає можливість знайти також середнюарифметичну швидкість для кожної молекули.
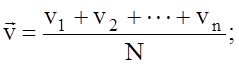
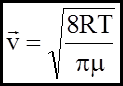 (3)
(3)
- середня арифметична швидкість.

2. Розглянемо газ, який знаходиться у полі сили тяжіння. Для подальшого розгляду введемо такі припущення:
розглянемо дуже тонкий шар газу (g=const), тоді 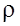 =const, T=const.
=const, T=const.

h
 |
mg
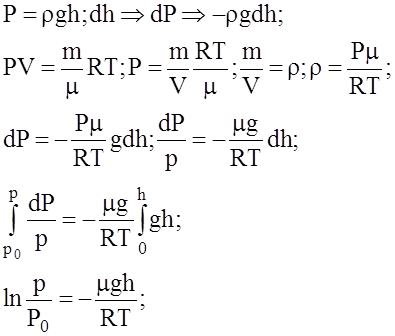
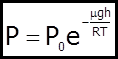 (4)
(4)
- барометрична формула.
Вона дає залежність атмосферного тиску від висоти h.
Оскільки P = nkT, тоді (4) можна представити так:
 (5)
(5)
- розподіл Больцмана.
Цей вираз описує найзагальніший закон Больцмана і дає розподіл кількості частинок у будь-якому потенціальному полі.
Ці теоретичні викладки були підтверджені в дослідах французького фізика Перрена (1908 рік), який вивчав розподіл по висоті посудини дуже маленьких частинок емульсії смоли гумігуту у воді і одержав такий закон :
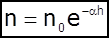
3. Раніше ми розглядали властивості тіл та систем, які знаходились у стані рівнодинамічної рівноваги. Але в більшості випадків на практиці мають справу з неврівноваженими системами.
Процес установлення стану термодинамічної рівноваги називається кінетичним процесом, або релаксаційним процесом , або просто релаксацією. Кількісною мірою встановлення стану термодинамічної рівноваги є величина, що називається час релаксації ( ).
).
Молекули ідеального газу здійснюють хаотичний рух унаслідок зіткнення та внаслідок співударів змінюють величину і напрямок своїх швидкостей, тому виникає необхідність увести середнє число зіткнень за 1 секунду 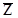 .
.
Відстань, яку проходять молекули між двома послідовними зіткненнями, називається середньою довжиною вільного пробігу молекул 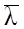 .
.
Ці величини пов`язані наступним співвідношенням :
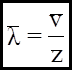 (6)
(6)
Якщо вважати, що молекули газу можна уявити, як маленькі кульки, то нескладні розрахунки можуть привести до такого результату :
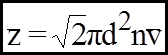 (7)
(7)
d - ефективний діаметр молекули.
Ефективний діаметр молекули - це відстань між центрами двох молекул при їх зіткненні.
Підстановка (7) в (6) дає:
 (8)
(8)
- формула довжини середнього вільного пробігу молекул газу.
Якщо врахувати, що  ,
, , то
, то
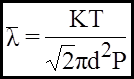 (8а)
(8а)
4. Розглянемо встановлення стану термодинамічної рівноваги у термодинамічно не врівноваженій системі.
Молекули володіють масою, імпульсом та енергією. Тому в термодинамічно не врівноваженій системі при встановленні стану термодинамічної рівноваги буде відбуватися просторовий перенос маси, імпульсу та енергії, що зумовлює явища дифузії, внутрішнього тертя й теплопровідності відповідно.
Ці явища зумовленi порушенням хаотичностi у русi молекул i описуються дослiдними законами.
а) Дифузiя - це явище проникнення молекул однiєї речовини у мiжмолекулярний простiр другої.
Це явище описується дослiдним законом Фiка :
 (9)
(9)
Закон Фiка :маса речовини М, яка переноситься за час t через поверхню площею S перпендикулярно до напрямку змiнення густини  , прямо пропорцiйна градiєнту густини
, прямо пропорцiйна градiєнту густини 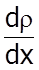 , площi S та часу t.
, площi S та часу t.
D - коефiцiєнт дифузiї.
Фiзичний змiст D : вiн чисельно дорiвнює масі речовини, яка переноситься через одиничну поверхню за одиницю часу при одиничному градiєнті густини.
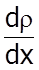 указує на змiну густини
указує на змiну густини  при одиничнiй змiнi
при одиничнiй змiнi
вiдстанi Х.
б) Внутрiшнє тертя (в`язкiсть) - це явище, що виникає мiж шарами рiдини (газу), якi рухаються з рiзними швидкостями. Тертя зумовлене обмiном імпульсу молекул цих шарiв унаслiдок хаотичностi їх руху. Воно описується дослiдним законом Ньютона :
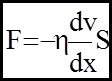 (10)
(10)
Сила тертя прямо пропорцiйна градiєнту швидкостi 
та площi шарiв, мiж якими виникає тертя.
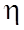 - коефiцiєнт в`язкостi (динамiчна в`язкiсть).
- коефiцiєнт в`язкостi (динамiчна в`язкiсть).
Фiзичний змiст 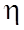 :
:
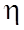 чисельно дорiвнює силi F мiж шарами одиничної площi S при одиничному градiєнтi швидкостi
чисельно дорiвнює силi F мiж шарами одиничної площi S при одиничному градiєнтi швидкостi 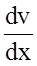 .
.
в) Теплопровiднiсть - це явище переносу теплоти вiд бiльш "гарячого" шару з температурою Т1 до бiльш "холодного" з температурою Т2. (Т2 < Т1). Воно описується
дослiдним законом Фур`є:
 (11)
(11)
Теплота, що переноситься за час t через поверхню площею S прямо пропорцiйна градiєнту температури  , площi S та часу t.
, площi S та часу t.
К - коефiцiєнт теплопровiдностi.
Фiзичний змiст К:
К чисельно дорiвнює кiлькостi теплоти Q, яка переноситься за одиницю часу через одиничну поверхню при одиничному градiєнтi температури  .
.
Знак "- " указує на:
1). математично: перенос маси, iмпульсу та енергiї вiдбувається у напрямку зменшення градiєнтiв густини, швидкості та температури;
2). фiзично: термодинамічна система переходить iз неврiвноваженого стану в рiвноважний тiльки таким чином, а не iнакше.
Одна iз головних задач молекулярної теорiї - встановлення зв`язку мiж макропараметрами D,  , К i мiкрохарактеристиками теплового руху молекул:
, К i мiкрохарактеристиками теплового руху молекул:
У припущеннi, що молекули є кульки, можна показати :
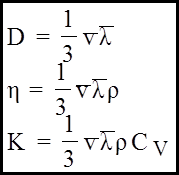 (12)
(12)
CV - питома теплоємнiсть речовини при сталому об'ємі.
Із (12) випливає:

Читайте також:
- Аналіз фінансово-господарської діяльності підприємства як методична основа діагностики його спроможності протидіяти кризовим явищам та ліквідувати їх наслідки
- Аналогія - спосіб отримання знань про предмети та явища на основі їхньої подібності з іншими.
- Біоелектричні явища в тканинах: будова мембран клітини, транспорт речовин через мембрану, потенціал дії та його розповсюдження.
- Біоелектричні явища і збудження в тканинах.
- Будова оптоволокна та основні фізичні явища в оптоволокні.
- Вивчення взаємозв’язків правопорушень з іншими соціальними явищами
- Види взаємозв'язків між явищами
- Визначення числа одиниць переносу
- Вплив рослин та тваринних організмів на процеси переносу
- Геологічні небезпечні явища
- Геологічні небезпечні явища
- Геологічні небезпечні явища.
| <== попередня сторінка | | | наступна сторінка ==> |
| ТЕМА: МАКРОСКОПІЧНИЙ СТАН | | | ТЕМА: ОСНОВИ ТЕРМОДИНАМІКИ |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |