
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Хімічні властивості.
1. Солі реагують з лугами або амоній гідроксидом. Унаслідок цього утворюються нові солі (середні, кислі, основні) та гідроксид або основна сіль (залежно від молярних співвідношень реагентів):
MgCl2 + NaOH ® Mg(OH)Cl + NaCl;
MgCl2 + 2NaOH ® Mg(OH)2+ 2NaCl;
NaH2PO4 + NaOH ® Na2HPO4 + H2O.
2. Солі реагують із кислотами. Такі реакції можливі, якщо утворюється осад чи слабкий електроліт. Продуктами цієї взаємодії можуть бути (залежно від молярних співвідношень реагентів) різні сполуки:
а) нова кислота і нова сіль:
FeS + 2HCl ® FeCl2 + H2S;
б) кисла та середня солі:
Ca3(PO4)2 + 2H2SO4 ® Ca(H2PO4)2 + 2CaSO4;
в) кисла сіль:
CaCO3 + CO2 + H2O ® Ca(HCO3)2;
г) одна або дві середні солі, основна сіль:
Fe(OH)2Cl + HCl ® Fe(OH)C12 + H2O.
3. Солі взаємодіють між собою. Така реакція можлива, якщо утворюється осад. Її продуктами будуть нові солі:
CaCl2 + Na2CO3 ® CaCO3¯ + 2NaCl.
Середня сіль може реагувати з кислою або основною сіллю одного й того ж металу, якщо між реагентами існує проміжна за складом кисла чи основна сіль, що й буде продуктом реакції:
Na3PO4 + NaH2PO4 ® 2Na2HPO4;
FeCl3 + Fe(OH)2Cl ® 2FeOHCl2.
4. Солі взаємодіють з металами з утворенням нової солі та металу:
CuSO4 + Fе ® FeSO4 + Сu.
Кожен метал може витіснити з розчинів солей метали, які знаходяться в ряді стандартних електродних потенціалів після нього, і не витісняє метали, що стоять перед ним:
FeSO4 + Сu (реакція не відбувається).
Метали, розташовані ліворуч від магнію (К, Ва, Са, Na та ін.), не використовують для витіснення металів із розчинів їх солей, оскільки вони реагують із водою з утворенням водню та лугу. Останній, у свою чергу, взаємодіє із сіллю з утворенням нерозчинного гідроксиду:
CuSO4 + 2Na + 2Н2O ® Сu(ОН)2¯ + Na2SO4 + H2.
5. Солі взаємодіють з оксидами (кислотними або амфотерними) під час нагрівання з утворенням солі та кислотного оксиду, більш леткого, ніж вихідний:
Na2CO3 + SiO2 ® Na2SiO3 +CO2;
4LiNO3 + 2А12О3 ® 4LiA1O2 + 4NO2 + О2.
6. Солі розкладаються під час нагрівання. Залежно від природи металу та кислоти утворюються різні продукти:
СаСО3 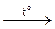 СаО + СO2;
СаО + СO2;
2NaNO3 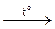 2NaNO2 + O2.
2NaNO2 + O2.
Читайте також:
- А) Товар і його властивості.
- Алкани (насичені вуглеводні). Хімічні властивості алканів
- Алкани, їх хімічні властивості.
- Алкени. Хімічні властивості
- Алкіни. Хімічні властивості
- Аміни. Фізичні та хімічні властивості аліфатичних амінів.
- Аналізатори людини та їхні властивості.
- Аналізатори людини та їхні властивості.
- Біохімічні зміни в організмі при розтренуванні і перетренуванні
- Біохімічні зміни компонентів молока при приготуванні кисло-молочних продуктів
- Біохімічні зміни при приготуванні сирів
- Біохімічні основи розвитку витривалості
| <== попередня сторінка | | | наступна сторінка ==> |
| Кислоти | | | Генетичний зв’язок між класами неорганічних сполук |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |