
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Порядку
Кінетика паралельних реакцій першого
Якщо одна і та сама речовина може реагувати за двома або більше напрямками, даючи різні продукти, то мають місце паралельні або конкуруючі розчини.
Наприклад,
 NH3 + N2 + H2O
NH3 + N2 + H2O
 N2OH
N2OH
NH3 + N2O + H2O ,
 |
.
Розглянемо найбільш простий випадок паралельних реакцій, коли обидві реакції проходять за першим порядком:
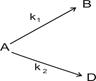
У цьому випадку
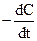 = k1C + k2C = (k1 + k2)C, (10.8)
= k1C + k2C = (k1 + k2)C, (10.8)
де С – змінна концентрація речовини А.
Звідси
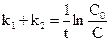 , (10.9)
, (10.9)
або
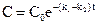 . (10.10)
. (10.10)
Ці рівняння аналогічні до рівнянь необоротної реакції першого порядку.
Для визначення кожної константи окремо врахуємо, що концентрації речовин, які утворилися у першій та другій реакціях, пропорційні константам відповідних швидкостей СВ/СD = =k1/k2.
На рис. 10.2 подане змінювання концентрацій у паралельних реакціях першого порядку.

Рисунок 10.2 – Змінювання концентрацій у паралельних реакціях першого порядку
Читайте також:
- RLC-фільтр четвертого порядку
- Аспекти організаційного порядку
- Афінний шифр k-ro порядку.
- Бінарне відношення порядку.
- Вестфальский мир як основа європейського правопорядку 1648-1815 рр.
- Визначення порядку черги фаз трифазної системи
- Визначники n-го порядку
- Відбулися кардинальні зміни у світовому порядку. На авансцену виходить Європа1.
- Відношення еквівалентності та порядку, їх властивості. Впорядковані множини. Зв'язок відношення еквівалентності з розбиттям множини на класи, що попарно не перетинаються.
- Відношення порядку на множині дійсних чисел.
- Відношення порядку на множині невід’ємних раціональних чисел.
- Відношення порядку на множині цілих невід’ємних чисел.
| <== попередня сторінка | | | наступна сторінка ==> |
| Кінетика зворотних реакцій першого порядку | | | Порядку |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |