
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
При підвищенні температури на 100 швидкість
реакції збільшується у 2-4 рази.
Використовуючи поняття температурного коефіцієнта швидкості реакції g, можна розрахувати зміну швидкості зaбудь-якої зміни температури:
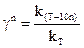 , (10.21)
, (10.21)
де n - кількість десятків градусів, на яку змінилася температура. n може бути цілим або дробовим, позитивним або негативним.
Більш точно позначає залежність константи швидкості реакції від температури рівняння, яке запропоноване у 1889 р. шведським вченим С.Арреніусом (рівняння Арреніуса):
k = k0exp(- Ea/RT), (10.22)
де k0 - передекспоненціальний множник, а Еa - енергія активації реакції (див. лекцію 9). Згідно з теорією Арреніуса (теорії активних зіткнень) для проходження реакції необхідно:
1) щоб відбулися зіткнення частинок системи;
Читайте також:
- Vу -швидкість ударника
- Алгоритм розрахунку температури поверхні чипу ІМС процесора
- Вертикальний градієнт температури
- Видаток і середня швидкість ламінарного потоку.
- Визначення температури на поверхні ізоляції принадземномупрокладанні та при прокладанні трубопроводів в приміщенні.
- Вимірювання інформації та швидкість її передачі
- Вимірювання температури
- Вимірювання температури контактним методом.
- Вплив всесторонннього стиску і температури на механічні властивості гірських порід
- Вплив параметрів режиму буріння на механічну швидкість проходки
- Вплив температури на рівновагу
- Вплив температури на форму та розмір наночастинок
| <== попередня сторінка | | | наступна сторінка ==> |
| Реакції | | | СТИСЛИЙ конспект лекцІй |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |