
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Добування толуолу
1 – реакція Фріделя – Крафтса:
 СН3
СН3
 |  | ||

 AlCl3
AlCl3
+ CH3Cl → + HCl
2 – реакція Вюрца – Фіттіга:

 Cl СН3
Cl СН3
 |  | ||


+2Na + Cl – CH3 → + 2NaCl
 |

 Розпізнавання бензолу, толуолу, стиролу
Розпізнавання бензолу, толуолу, стиролу
| Арен Реактив | бензол | толуол | стирол |
| нітруючa суміш HNO3 / H2SO4 | жовта речовина з запахом гіркого мигдалю | – | – |
| перманганат калію KMnO4 | – | знебарвлення | знебарвлення |
| бромна вода Br2 / H2O | – | – | знебарвлення |
Використання аренів у медицині
Бензидин –використовують в лабораторії для виявлення скритої крові у калі при внутрішніх кровотечах.
 |  |


 H2N – –NH2
H2N – –NH2
Брильянтовий зелений –антисептичний засіб.


 H5C2 C2H5
H5C2 C2H5


 N – – CH – – N
N – – CH – – N
H5C2 C2H5
Порівняльна характеристика вуглеводнів
| Характеристика | алкани | алкени | алкіни | арени |
| Зв’язки | С – С | С = С | С ≡ С |  
|
| Загальні формули | СnH2n+2 | СnH2n | СnH2n–2 | СnH2n–6 |
| Закінчення в назвах | – ан | – ен (єн) | – ин (ін) | – ен (єн) |
| Гібридизація | sp3 | sp2 | sp | sp2 |
| Валентні кути | 109°28′ | 120° | 180° | 120° |
| Форма молекули | тетраедрична | площинна | лінійна | площинна |
| Хімічні зв’язки | σ С – С | σ С = С π | σ С ≡ С 2π |  
 πσ πσ
|
| Довжина зв’язків | 0,154 нм | 0,134 нм | 0,120 нм | 0,140 нм |
| Енергія зв’язків | 347кДж/моль | 615кДж/моль | 812кДж/моль | 412кДж/моль |
| Характерні реакції | заміщення | приєднання | 1–приєднання 2–заміщення | 1– заміщення 2– приєднання |
| Якісні реакції |
 Знебарвлення бромної води та розчину KMnO4 Знебарвлення бромної води та розчину KMnO4
|
 Знебарвлення бромної води та розчину KMnO4
Реакції з Знебарвлення бромної води та розчину KMnO4
Реакції з
 Ag(NH3)2OH
(білий осад) та
Сu(NH3)2OH
(червоний осад) Ag(NH3)2OH
(білий осад) та
Сu(NH3)2OH
(червоний осад)
| Бензол – нітрування. Толуол – знебарвлення KMnO4 Стирол – Знебарвлення бромної води та розчину KMnO4 |
Галогенопохідні вуглеводнів
· це продукти заміщення в молекулах вуглеводнів одного або декількох атомів Гідрогену атомами галогенів.
Класифікація галогенопохідних
1 – за видом галогену:
–фторопохідні;
– хлоропохідні;
– бромопохідні;
– йодопохідні.
2 – за кількістю атомів галогенів:
– моногалогенопохідні;
– дигалогенопохідні тощо.
3 – за будовою вуглеводнів:
– насичені СН3 – СН2 СН2 – СН2
׀ ׀ ׀
Cl Cl Cl
– ненасичені СН2 = СН СН2 – СН = СН2
׀ ׀
Cl Cl
 – ароматичні Cl
– ароматичні Cl

 |
4 – за розташуванням двох атомів галогенів:
–гемінальні – два галогени розташовані біля одного атома С
Cl Cl
׀ ׀
СН3 – СН СН3 – С – СН3
׀ ׀
Cl Cl
– віцинальні – два галогени розташовані біля сусідніх атомів С
СН2 – СН2 СН3 – СН – СН2
׀ ׀ ׀ ׀
Cl Cl Cl Cl
– ізольовані – два галогени розташовані через один або більше атомів С
СН2 – СН2 – СН2
׀ ׀
С1 С1
Хімічні властивості галогенопохідних
1 – заміщення:
Ø лужний гідроліз
СН3 – Cl + NaOH → CH3 – OH + NaCl добування спиртів
Cl OH

 ׀ ׀ O
׀ ׀ O
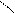 CH3 – CH + 2NaOH → CH3 – CH → CH3 – C + Н2О добування альдегідів
CH3 – CH + 2NaOH → CH3 – CH → CH3 – C + Н2О добування альдегідів
׀ ׀ H
Cl OH
|
Cl ОН

 ׀ ׀
׀ ׀
 |  |
+ NaOH → + NaCl добування фенолів
Ø амоноліз
СН3 – Cl + NH3 → CH3 – NH2 + HCl добування амінів
2 – відщеплення:
Читайте також:
- Добування ацетилену
- Добування карбонільних сполук
- ДОБУВАННЯ КАРБОНОВИХ КИСЛОТ
- ДОБУВАННЯ КОРИСНИХ КОПАЛИН ВІДКРИТИМ СПОСОБОМ
- ДОБУВАННЯ КОРИСНИХ КОПАЛИН ВІДКРИТИМ СПОСОБОМ
- Добування фенолу
- Добування чистих металів.
- Добування.
- Загальні способи добування металів.
- Класифікація методів практичного видобування знань
- Піднесення до степеня і добування кореня
| <== попередня сторінка | | | наступна сторінка ==> |
| Гомологи бензолу | | | R R R R |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |