
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Відновлення металів може проводитись різними методами, які зручно об'єднати в такі групи: пірометалургійні, гідрометалургійні та електрометалургійні.
Найбільш розповсюджені пірометалургійні методи, тобто відновлення металів за високих температур. Як відновник найчастіше використовують вугілля (кокс), оксид карбону(ІІ) та водень, наприклад:
+2 0 0 +2
ZnО + С = Zn + СО;
+3 +2 0 +4
Fe2O3+ 3CO = 2Fe + 3CO2;
+6 0 0 +1
WO3+3H2= W + 3H2O
Найдешевшим з них є кокс. Вказані відновники можуть бути використані для порівняно неактивних металів. Точна оцінка можливості перебігу процесу відновлення заснована на розрахунку зміни вільної енергії Гіббса ∆G.
Іноді для одержання деяких металів, використовують як відновники інші (більш активні) метали. Цей метод називають металотермічним.Найчастіше відновниками є алюміній, магній, кальцій, наприклад:
0 +3 0 +3
2Al + Cr2O3= 2Cr+Al2O3
0 +4 +2 0
2Mg + TiCl4= 2MgCl2+Ti
0 +5 0 +2
5Са + V2О5 = 2V + 5СаО.
Гідрометалургійні методи — це відновлення металів з водних розчинів солей та комплексних сполук. Прикладом може бути процес добування кадмію:
+2 0 0 +2
СdSО4 + Zn = Cd + ZnSО4.
Електрометалургійні методигрунтуються на процесах добування металів за допомогою електролізу. їх можна розділити на гідроелектрометалургійні, коли метали відновлюють на катоді з водних розчинів, якщо потенціал, що відповідає процесу відновлення (Меn+ + +п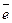 =Ме), не нижче приблизно -1,1В, та електротермічні – добування найбільш активних металів електролізом розплавів їх сполук. Електролізом водних розчинів солей добувають хром, марганець, кобальт, нікель, мідь, цинк, електролізом розплавів – лужні, лужноземельні метали, алюміній та ін.
=Ме), не нижче приблизно -1,1В, та електротермічні – добування найбільш активних металів електролізом розплавів їх сполук. Електролізом водних розчинів солей добувають хром, марганець, кобальт, нікель, мідь, цинк, електролізом розплавів – лужні, лужноземельні метали, алюміній та ін.
У вільному стані у природі зустрічаються метали з низькою хіміч-ною активністю — срібло, золото, платинові метали та ртуть. Інші — у вигляді сполук. Таким чином, добування вільних металів зводиться до їх відновлення.
Меt+n + пе– = Меt
Відновлення здійснюють хімічним або електрохімічним шляхом.
Як відновники зазвичай використовують вуглець, оксид карбону (II), водень, метан, кремній, алюміній, магній.
1. Відновлення металів з оксидів вуглецем або оксидом (II):
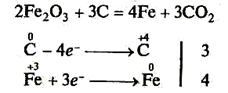 |
Відновник — вуглець, окисник — оксид феруму (III).
 |
Відновник — вуглець, окисник — оксид цинку.
2. Відновлення металів із їх оксидів більш активними металами (зазвичай використовують відновлення алюмінієм — алюмотермію):
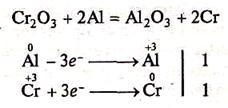 |
Відновник — алюміній, окисник — оксид хрому (III).
3. Відновлення металів із їх оксидів воднем:
 |
Відновник — водень, окисник — оксид феруму (III).
4. Електроліз розчинів солей металів:
 |
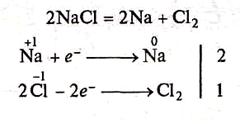 5. Електроліз розплавів солей металів використовують для добування найбільш активних металів, які неможливо добути переліченими вище методами:
5. Електроліз розплавів солей металів використовують для добування найбільш активних металів, які неможливо добути переліченими вище методами:
| <== попередня сторінка | | | наступна сторінка ==> |
| Загальні способи добування металів. | | | Добування чистих металів. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |