
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Умова нерозривності потоку
VS=const
36.
Гідростати́чний тиск (рос.гидростатическое давление, англ. hydrostatic pressure, нім.Hydrostatischer Druck m, Wasserdruck m) —
1) Тиск рідини в будь-якій точці об'єму цієї рідини. Тиск у рідині, що перебуває у стані спокою, створений сумою тиску газу на її вільній поверхні і зумовленого силою тяжіння тиску стовпа рідини, розташованого над точкою вимірювання. Гідростатичний тиск залежить від глибини занурення. Вимірюється в одиницях висоти стовпа рідини або в одиницях тиску.
Динамі́чний тиск (рос. динамическое давление; англ. dynamic pressure; нім. dynamischer Druck m) — частина тиску всередині рухомоїрідини або газу, зумовлена їх рухом; характеризує їх кінетичну енергію.
 ,
,
де  — густина, v — швидкість потоку рідини або газу.
— густина, v — швидкість потоку рідини або газу.
Рівня́ння Берну́ллі — рівняння гідродинаміки, яке визначає зв'язок між швидкістю течії v, тиском p та висотою h певної точки в ідеальній рідині. Встановив його у 1738році Даніель Бернуллі.
Для ламінарної течії ідеальної нестисливої рідини рівняння Бернуллі має вигляд:
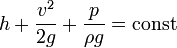
або
 ,
,
де ρ — густина рідини; g — прискорення вільного падіння.
В останньому рівнянні всі члени мають розмірність тиску, p — статичний тиск; 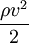 — динамічний тиск; hρg — ваговий тиск.
— динамічний тиск; hρg — ваговий тиск.
Тема 2
Молекулярно-кінетична теорія виходить із того, що речовина, зокрема газ складається з великої кількості мікроскопічних частинок (молекул), які рухаються хаотично. Частинки стикаються між собою та зі стінками посудини, створюючи на ці стінки тиск. Усі зіткнення вважаються пружними, тобто проходять без втрати енергії. Середнякінетична енергія руху частинок залежить від температури.
Середня кінетична енергія руху молекули:
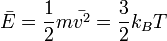 ,
,
де m — маса частинки, v — її швидкість,  — стала Больцмана, T — температура.
— стала Больцмана, T — температура.
Дифу́зія (лат. diffusio — поширення, розтікання, розсіювання, взаємодія) — процес взаємного проникнення молекул або атомів однієї речовини поміж молекул або атомів іншої, що зазвичай приводить до вирівнювання їхніх концентрацій по всьому займаному об'ємі.
Теплопрові́дність — здатність речовини переносити теплову енергію, а також кількісна оцінка цієї здатності: фізична величина, що характеризує інтенсивністьтеплообміну в речовині, яка дорівнює відношенню густини теплового потоку до градієнта температури
В'я́зкість або внутрішнє тертя — властивість рідких речовин (рідин і газів) чинити опір переміщенню однієї їх частини відносно іншої. Одиниця вимірювання динамічного коефіцієнта в'язкості — Пуаз.
Згідно із законом Ньютона для внутрішнього тертя в'язкість характеризується коефіцієнтом пропорційності  міжнапруженням зсуву
міжнапруженням зсуву  і градієнтом швидкості руху шарів
і градієнтом швидкості руху шарів  у перпендикулярному до деформації зсуву напрямку (поверхні шарів):
у перпендикулярному до деформації зсуву напрямку (поверхні шарів):
 .
.
Коефіцієнт  називають динамічний коефіцієнт в’язкості або абсолютною в'язкістю. Одиниця вимірювання динамічного коефіцієнта в'язкості — Па
називають динамічний коефіцієнт в’язкості або абсолютною в'язкістю. Одиниця вимірювання динамічного коефіцієнта в'язкості — Па  c, Пуаз (0,1Па·с).
c, Пуаз (0,1Па·с).
Ізобаричний процес
Нехай в циліндрі (рис. 31.1) знаходиться газ, об’єм якого дорівнює  при температурі
при температурі  і тиску
і тиску  . Площа поршня
. Площа поршня 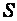 . Під дією сили
. Під дією сили 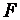 поршень переміщується з положення 1 у положення 2. Будемо вважати, що тиск газу не змінюється. Тоді робота газу буде:
поршень переміщується з положення 1 у положення 2. Будемо вважати, що тиск газу не змінюється. Тоді робота газу буде:
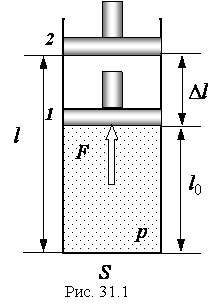
 .
.
Так як  ,
,
де 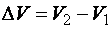 – зміна об’єму газу; то:
– зміна об’єму газу; то:
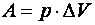 .
.
Отже, робота газу при ізобаричному процесі ( 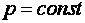 ) дорівнює добутку тиску газу на зміну об’єму.
) дорівнює добутку тиску газу на зміну об’єму.
Згідно з першим началом термодинаміки для ізобаричного процесу маємо:
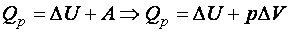 .
.
Ізохоричний процес
Оскільки при ізохоричному процесі (  )
) 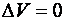 , то робота, виконана газом, дорівнює нулю і перше начало термодинаміки має вигляд:
, то робота, виконана газом, дорівнює нулю і перше начало термодинаміки має вигляд:
 .
.
Отже, все тепло при ізохоричному процесі використовується тільки для збільшення внутрішньої енергії газу.
Ізотермічний процес
Для ізотермічного процесу (  )
)  . Так як внутрішня енергія:
. Так як внутрішня енергія:
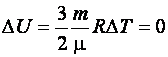 ,
,
то звідси випливає, що перше начало термодинаміки можна записати так :
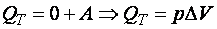 .
.
Вся теплота, надана тілу, при ізотермічному процесі йде на виконання роботи газу.
Адіабатичний процес
Адіабатичний процес – це процес, який проходить без теплообміну із зовнішнім середовищем (  = 0).
= 0).
Тоді перше начало термодинаміки має вигляд:
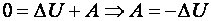 .
.
Робота при адіабатичному процесі виконується за рахунок зменшення внутрішньої енергії газу.
 Конкретні формули розрахунку роботи при всіх процесах, крім ізобаричного, мають складну форму і в даному курсі фізики не розглядаються. На практиці роботу газу можна визначити як площу фігури в координатах
Конкретні формули розрахунку роботи при всіх процесах, крім ізобаричного, мають складну форму і в даному курсі фізики не розглядаються. На практиці роботу газу можна визначити як площу фігури в координатах 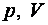 (на рис. 31.2 – це площа заштрихованої фігури).
(на рис. 31.2 – це площа заштрихованої фігури).
 31.2. Теплові двигуни
31.2. Теплові двигуни
Нехай газ знаходиться стані 1 ( 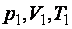 ) (рис. 31.3). Переведемо газ у стан 2 (
) (рис. 31.3). Переведемо газ у стан 2 (  ). Шлях такого переходу буде 1–3–2. Повернемо газ знову в стан 1. Повернення здійснимо шляхом 2–4–1. Такий процес називається коловим процесом, або циклом.
). Шлях такого переходу буде 1–3–2. Повернемо газ знову в стан 1. Повернення здійснимо шляхом 2–4–1. Такий процес називається коловим процесом, або циклом.
При переході 1–3–2 газ отримує кількість теплоти  , а при переході 2–4–1 він віддає кількість теплоти
, а при переході 2–4–1 він віддає кількість теплоти  . Тоді робота, яка виконується за цикл:
. Тоді робота, яка виконується за цикл:
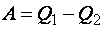 ,
,
а ККД цього циклу:

Теплові двигуни – це машини, які перетворюють теплову енергію в механічну. Існує три умови, необхідні для роботи теплового двигуна (рис. 31.4):
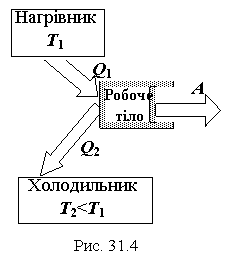 а) наявність робочого тіла (пари, газу), яке, розширюючись, здатне виконати роботу;
а) наявність робочого тіла (пари, газу), яке, розширюючись, здатне виконати роботу;
б) наявність нагрівника і холодильника;
в) використання в роботі теплового двигуна колового процесу (циклу).
ККД машин визначається за формулою:
 ,
,
де  – кількість теплоти, отримана від нагрівника;
– кількість теплоти, отримана від нагрівника;  – кількість теплоти, що передана холодильнику.
– кількість теплоти, що передана холодильнику.
Ідеальна теплова машина, яка працює по циклу Карно (С. Карно – французький фізик, автор даного циклу), має ККД, що визначається як (рис. 31.4):
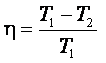 ,
,
де Т1 – температура нагрівника; Т2 – температура холодильника.
Це максимально можливий ККД для теплових машин.
Вн́утрішня ене́ргія тіла (позначається як E або U) — повна енергія термодинамічної системи за винятком її кінетичної енергії як цілого і потенціальної енергії тіла в полі зовнішніх сил. Внутрішня енергія складається з кінетичної енергії хаотичного руху молекул, потенціальної енергії взаємодії між ними і внутрішньомолекулярної енергії.
Внутрішня енергія є однозначною функцією рівноважного стану системи. Це означає, що кожний раз, коли система опиняється в даному рівноважному стані, її внутрішня енергія приймає властиве цьому стану значення, незалежно від передісторії системи. Отже, зміна внутрішньої енергії при переході з одного стану в інший буде завжди дорівнювати різниці значень в цих станах, незалежно від шляху, по якому здійснювався перехід. Внутрішню енергію тіла не можна виміряти напряму. Можна визначити тільки зміну внутрішньої енергії:
 ,
,
де  — кількість теплоти, передана термодинамічній системі,
— кількість теплоти, передана термодинамічній системі, 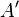 — робота, виконана над термодинамічною системою[1] або:
— робота, виконана над термодинамічною системою[1] або:
 ,
,
де 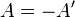 , робота виконана термодинамічною системою.(Приклад)
, робота виконана термодинамічною системою.(Приклад)
Термодинамічні властивості ідеального газу можна описати такими двома рівняннями:
Стан класичного ідеального газу описується рівнянням стану ідеального газу:

Внутрішня енергія ідеального газу описується наступним рівнянням:

де 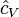 є константою (рівною, наприклад, 3/2 для одноатомного газу) і
є константою (рівною, наприклад, 3/2 для одноатомного газу) і
· U — внутрішня енергія (вим. у джоулях)
· P — тиск (паскаль)
· V — об'єм (метр кубічний)
· n — кількість речовини (моль)
· R — газова стала (джоуль на моль на градус Кельвіна)
· T — абсолютна температура (градуси Кельвіна)
· N — кількість молекул
· kB — стала Больцмана (джоуль на градус Кельвіна на молекулу)
Теплоє́мність — фізична величина, яка визначається кількістю теплоти, яку потрібно надати тілу для зміни його температури на один градус.
Позначається здебільшого великою латинською літерою C. Питома теплоємність — теплоємність одиничної маси тіла, позначається малою латинською літерою c. Часто визначається також молярна теплоємність — теплоємність одного моля газу.
Кількість теплоти  в термодинаміці визначається величиною
в термодинаміці визначається величиною
 ,
,
де T — температура, S — ентропія.
| <== попередня сторінка | | | наступна сторінка ==> |
| Дане явище описує закон Ньютона | | | Модуль 2 |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |