
МАРК РЕГНЕРУС ДОСЛІДЖЕННЯ: Наскільки відрізняються діти, які виросли в одностатевих союзах
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
Контакти
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Електрогравіметричний метод
Електрогравіметричний аналіз (електрогравіметрія) є різновидом гравіметричного (вагового) методу. Він ґрунтується на кількісному виділенні речовини на електродах внаслідок проведення електролізу досліджуваного розчину та визначенні маси одержаного на електроді осаду. Осаджувачем є електричний струм: на катоді проходить процес відновлення, а на аноді – окиснення. Метод є простим, точним, дозволяє визначати малі кількості речовини.
В процесі електролізу на катоді проходить відновлення позитивно заряджених іонів:
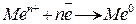 ,
,
а на аноді – окиснення аніонів:
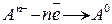 .
.
Наприклад, при електролізі розчину ZnCl2 на катоді виділяється цинк, а на аноді – хлор:
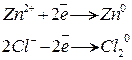 .
.
В інших випадках електроліз перебігає більш складно. Наприклад, при електролізі розчинів сульфатів лужних і лужноземельних металів на катоді виділяється водень:
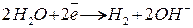 ,
,
а на аноді окиснюється вода з виділенням кисню:
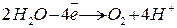 .
.
Електрогравіметрія використовується для:
1) для визначення катіонів, що відновлюються на катоді – Cu2+, Ni2+, Zn2+, Cd2+, тощо;
2) для визначення катіонів, що окислюються на аноді – Pb2+ ( 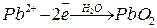 ) і Mn2+;
) і Mn2+;
3) для визначення аніонів – Cl– (для цього використовують розчинний срібний анод);
4) визначення неметалічних включень в сталях – зразок, що аналізується підключається у вигляді аноду, метали розчиняються і переходять в розчин, а зважують неметалічний залишок каркасу;
5) електроліз є основою полярографічного методу, амперометрії та кулонометрії;
6) електроліз широко використовується для покриття різноманітних виробів захисним шаром металу.
| <== попередня сторінка | | | наступна сторінка ==> |
| Визначення хлорид- і йодид-іонів при спільній присутності їх у розчині | | | Закони електролізу |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |