
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Електронна хмара. Хвильова функція
Точне положення електрона в атомі в певний момент часу встановити неможливо внаслідок існування співвідношення невизначеностей Гейзенберга (для координати і імпульсу, енергії і часу) в силу його хвильових властивостей
Електрон у атомі можна уявити як хмару з певною густиною від’ємного електричного заряду в певному об’ємі простору навколо ядра. Оскільки рух електрона має хвильовий характер, то він описується за допомогою хвильового рівняння подібно тому як описуються акустичні, світлові хвилі. Таке рівняння було запропоноване у 1926р. австрійским вченим Ервіном Шредінгером. Це диферненціальне рівняння II порядку в частинних похідних для 1-го електрона у трьохмірному просторі. Стаціонарне хвильове рівняння (коли ϕ не залежить від часу)
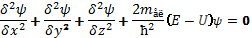
Величину Ψ, що кількісно характеризує амплітуду трьохмірної хвилі, зв’язаної з рухом електрона, називають хвильовою функцією або „псі”-функцією.
Е - повна енергія електрона (частинки);
U - потенціальна енергія електрона в полі потенціальних сил ядра;
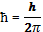 , h =6,63*10-34 Дж с; måë - маса електрона.
, h =6,63*10-34 Дж с; måë - маса електрона.
Ψ - приймає комплексні значення. Фізичний зміст має не сама ϕ-функція, а квадрат її модуля
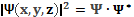 - характеризує густину ймовірності знаходження електрона
- характеризує густину ймовірності знаходження електрона
і 12
у деякій точці простору. Величина 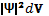 - є ймовірністю знаходження електрона в
- є ймовірністю знаходження електрона в
елементі об’єму dVв „окрестности” певної точки атомного простору. Визначаючи значення хвильової функції, що задовольняють рівняння Шредінгера, ми знаходимо той простір біля ядра, в якому з найбільшою ймовірністю перебуває електрон (його називають атомною орбіталлю, АО).
Слід вказати, що розв’язки хвильового ріняння (просторові хвильові функції електрона) можливі тільки при певних дискретних значеннях енергії Е1, Е2, ... , Еn. Таким чином, на відміну постулатам Бора існування квантованих станів, які характеризуються квантованими значеннями енергії мікросистеми строго безпосередньо витікає із розв’язку хвильового рівняння.
| <== попередня сторінка | | | наступна сторінка ==> |
| Електронна структура атомів | | | Квантовані стани атома |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |