
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Константа електролітичної дисоціації слабкого електроліту
Слабкi кислоти та основи дисоцiюють у водi лише частково з утворенням гiдратованих катiона та анiона, наприклад:
HAn + (k+1) H2O « H3O+ + An–∙k H2O
aбо без врахування гідратації:
НАn « Н+ + An–.
Рiвновага цiєї реакцiї характеризується константою, яку називають константою дисоціації KHAn:
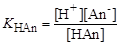 .
.
Вона характеризує здатність електроліту до дисоціації на йони. Чим більшим є значення константи, тим більш дисоційованим є електроліт.
Константа дисоцiацiї пов’язана зі ступенем дисоціацiї законом розведення В.Оствальда (1888 р.):
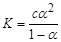 . (3.10)
. (3.10)
Якщо електроліт слабкий і розчин не дуже розведений, то ступінь дисоціації α є малим і значення 1-α мало відрізняється від одиниці. Тоді
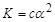 і
і 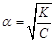 .
.
З цієї формули випливає, що ступінь дисоціації електроліту зростає під час його розведення.
Переглядів: 194