
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
R R R R
Br
Сl
Спирт
Спирт
СН3 – СН2 + КОН → СН2 = СН2 + КCl + H2O добування алкенів
׀
Cl
СН2 – СН2 + 2КОН → СН ≡ СН + 2КCl + 2H2O добування алкінів
׀ ׀
Cl Cl
Cl
׀спирт
СН3 – СН + 2 КОН → СН ≡ СН + 2КCl + 2H2O добування алкінів
׀
Cl
CH2 – CH2 + Zn → CH2 = CH2 + ZnCl2 добування алкенів
׀ ׀
Cl Cl
 |
СН2 – СН2 – СН2 + Zn → + ZnCl2 добування циклоалканів
׀ ׀
С1 С1
3 – реакція Вюрца:
CH3Cl + 2Na + ClCH3 → СН3 – СН3 + 2NaCl добування алканів
4 – реакція Вюрца – Фіттіга:

 Cl СН3
Cl СН3
 |  |


+2Na + Cl – CH3 → + 2NaCl
Добування галогенопохідних
· Моногалогенопохідні
а) первинні:
СН3 – СН2 – СН2ОН + НСl → СН3 – СН2 – СН2Сl + Н2О
б) вторинні:
СН3 – СН – СН3 + НСl → СН3 – СН – СН3 + Н2О
׀׀
ОН Сl
hυ
СН3 – СН2 – СН3 + Сl2 → СН3 – СН – СН3 + НСl
׀
Сl
СН3 – СН = СН2 + НCl → СН3 – СН – СН3
׀
Cl
 в) ароматичні:Cl
в) ароматичні:Cl



 FeCl3
FeCl3
+ Cl2 → + HCl
· Дигалогенопохідні
а) гемінальні первинні:Cl
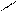
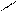 О ׀
О ׀
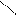 СН3 – С + РCl5 → СН3 – СН + РОCl3
СН3 – С + РCl5 → СН3 – СН + РОCl3
Н ׀
Cl
б) гемінальні вторинні:Cl
׀
СН3 – С ≡ СН + 2НCl → СН3 – С – СН3
׀
Cl
Cl
׀
СН3 – СН2 – СН3 + 2Cl2 → СН3 – С – СН3 + 2НCl
׀
Cl
в) віцинальні:
СН3 – СН = СН2 + Cl2 → СН3 – СН – СН2
׀ ׀
Cl Cl
Використання галогенопохідних у медицині
Хлороформ СНCl3 –інгаляційний наркоз.
Йодоформ СНІ3 –антисептичний засіб.
Хлоретан С2Н5Cl –місцевий знеболюючий засіб. Його дія зумовлена швидким випаровуванням, що викликає сильне охолодження шкіри і втрату чутливості.
׀
Фторотан F3C – CH –інгаляційний наркоз.
׀
Трихлоретилен ClHC = CCl2 –інгаляційний наркоз.
 |
Хлоксил Сl3C – – CCl3 –лікування гельмінтозів печінки.
 Спирти
Спирти
· це похідні вуглеводнів, що містять одну або декілька груп ОН.
Функціональна група ОН –гідроксильна.
Класифікація спиртів:
· за кількістю груп ОН:
– одноатомні спирти СН3 – ОН СН3 – СН2 – ОН
СН3 – СН2 – СН2 СН3 – СН – СН3
׀ ׀
ОН ОН
– багатоатомні спирти СН2 – ОН СН2 – ОН
׀ ׀
СН2 – ОН СН – ОН
׀
СН2 – ОН
· за будовою вуглеводневого радикалу:
– насичені спирти СН3 – СН2 – СН2 СН3 – СН – СН3
׀ ׀
ОН ОН
– ненасичені спирти СН2 = СН – СН2
׀
ОН

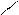 – ароматичні спирти СН2 – ОН
– ароматичні спирти СН2 – ОН

· за місцем гідроксильної групи:
– первинні спирти СН3 – СН2 – СН2
׀
ОН
– вторинні спирти СН3 – СН – СН3
׀
ОН
– третинні спирти СН3
׀
СН3 – С – СН3
׀
ОН
Одноатомні насичені спирти
Загальна формула СnH2n + 1 ОН
Гомологічний ряд:
СН3ОН метанол (метиловий спирт)
С2Н5ОН СН3 – СН2 етанол (етиловий спирт)
׀
ОН
С3Н7ОН СН3 – СН2 – СН2 пропанол–1 (пропіловий спирт)
׀
ОН
СН3 – СН – СН3 пропанол–2
׀
ОН
С4Н9ОН СН3 – СН2 – СН2 – СН2 СН3 – СН2 – СН – СН3
׀ ׀
бутанол – 1 ОН ОН бутанол – 2
Ізомерія:
–за вуглецевим скелетом СН3 – СН2 – СН – СН3 бутанол – 2
׀
ОН
СН3
׀
СН3 – С – СН3 2 – метилпропанол – 2
׀
ОН
– за положенням функціональної групи
СН3 – СН2 – СН2 – СН2 СН3 – СН2 – СН – СН3
׀ ׀
бутанол – 1 ОН ОН бутанол – 2
– міжкласова ізомерія (з простими ефірами) СН3 – СН2 – ОН етанол
СН3 – О – СН3 диметиловий ефір

 Електронна будова: Оδ–
Електронна будова: Оδ–
С Нδ+ Валентний кут 110°25′
Зв’язки С – О та О – Н полярні, тому легко розриваються під час хімічних реакцій. Отже, для спиртів характерні два види реакцій заміщення.
Фізичні властивості: С1 – С15 –рідини
С16 і більше –тверді
Нижчі спирти добре розчинні у воді, мають характерний запах.
Рідкий стан спиртів (відсутність газоподібних речовин) та розчинність у воді пояснюється наявністю водневих зв’язків між молекулами спирту та молекулами води і спирту:

 Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ–
Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ–


 Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ–
Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ– ··· Нδ+– Оδ–
| <== попередня сторінка | | | наступна сторінка ==> |
| Добування толуолу | | | R H R H |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |