
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Швидкістю найбільш повільної стадії.
Швидкостями окремих стадій визначається
Швидкість багатостадійного процесу з різними
Інших реакцій.
Закону кінетики і проходить незалежно від
То кожна з них підпорядковується основному
Повне змінювання системи є сумою цих незалежних змінювань. Принцип незалежності не є абсолютно загальним, оскільки відомий вплив реакцій.
Ще один постулат хімічної кінетики – принцип лімітуючої стадії:
Найчастіше хімічні реакції не проходять до кінця, тобто еквімолярна суміш вихідних речовин не повністю перетворюється у кінцеві продукти реакції. У таких випадках реакція наближується до якогось рівноважного стану , який може бути заздалегідь обчислений на основі термодинамічних даних. Прикладами таких реакцій є утворення аміаку, йодоводню, багатьох окисно-віднових реакцій. Оборотність реакцій особливо помітна у тих випадках, коли константа рівноваги близька до 1. Якщо необхідно довести реакцію до кінця, то слід видаляти продукти реакції з рівноважної суміші.
У випадку, коли реакції, що проходять у прямому та зворотному напрямках, мають перший порядок:
А 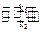 В.
В.
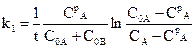 ,
,
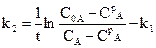 .
.
Якщо одна і та сама речовина може реагувати за двома або більше напрямками, даючи різні продукти, то мають місце паралельні або конкуруючі розчини.

У цьому випадку
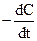 = k1C + k2C = (k1 + k2)C,
= k1C + k2C = (k1 + k2)C,
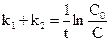
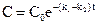
Ці рівняння аналогічні до рівнянь необоротної реакції першого порядку.
Послідовними реакціями називаються реакції з про міжними стадіями. У таких реакціях проміжний продукт, що утворюється на одній стадії, потім витрачається у наступній стадії. Схема найпростішої послідовної реакції першого порядку має вигляд
А 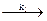 B
B 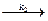 D .
D .
Швидкість змінювання концентрацій усіх речовин підпорядковуються таким рівнянням:
 ,
,
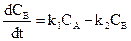 ,
,
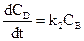 .
.
У результаті інтегрування цих рівнянь можна отримати часові залежності для концентрацій окремих компонентів:
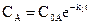 ,
,
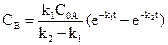 ,
,
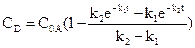 .
.
Більшість хімічних реакції складні, тобто вони проходять не так, як пишуться їх стехіометричні рівняння, а за механізмами, що складаються з декількох елементарних реакцій. Велику роль у деяких із цих механізмів відіграють активні частинки , що утворюються за сторонньою дії на систему - атоми або радикали. Таким чином, у результаті реакції спостерігається послідовність перетворення радикалів:
· · ·
R1  R2
R2  R3
R3  …
…
Читайте також:
- II. Критерій найбільших лінійних деформацій
- V. НАЙБІЛЬШ ВАЖЛИВІ ПОДІЇ І ДАТИ
- АТ – одна з найбільш зручних форм колективного підприємства в умовах ринкової економіки. Першим АТ вважають створену у 1602 році Голандсько –Ост - Індську компанію.
- В межах наукового підходу існує велика кількість концепцій, але найбільш переконлива – еволюційна теорія.
- ВЕЛИКОБРИТАНІЯ НАЙБІЛЬШ РОЗВИНЕНА НІЖ ІТАЛІЯ
- Випишіть 3 партії, що на вибораз 1994р. набрали найбільшу кількість голосів, зазначте прізвища їх лідеорів, яку ідеологію вони ісповідували?
- Відносно фронтальної площини проекцій модель треба розташувати так, щоб на цю площину вона спроекціювалась найбільш наочно – це зображення є головним виглядом.
- Відомості про найбільші озера Світу та України.
- Відомості про найбільші озера Світу та України.
- До найбільших морських портів України розташований межах Причорноморського економічного району належать
- Екологічні проблеми найбільших річок, Чорного і Азовського морів.
- Екологічні проблеми найбільших річок, Чорного й Азовського морів. Донецько-Придніпровський регіон
| <== попередня сторінка | | | наступна сторінка ==> |
| СТИСЛИЙ конспект лекцІй | | |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |