
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Організація дихального ланцюга
В процесі тканинного дихання від субстратів шляхом окиснення відщеплюються протони і електрони. Вони поступають на ферменти дегідрогенази, які відносяться до класу оксидоредуктаз і локалізовані у внутрішній мембрані мітохондрій. Пересуваючись від одного перенощика електронів до іншого, вони переходять на нижчі енергетичні рівні, віддаючи свою енергію порціями. В останній ланці дихального ланцюга електрони відновлюють молекулярний кисень з подальшим виділенням води. Звільнена енергія при перенесенні електронів у дихальному ланцюзі запасається в пірофосфатних зв’язках АТФ.
Окиснення органічних молекул в клітині, спряжене з вивільненням енергії, здійснюється дегідруванням – перенесенням електронів і протонів від атомів водню на молекулярний кисень (Рис. 3.1).

Рис. 3.1. Перенесення електронів і протонів від атомів водню
У клітинах тварин і людини спряження процесів окиснювапьно-відновних реакцій з синтезом АТФ проходить в клітинних органелах – мітохондріях. Ферменти дихального ланцюга розміщені на внутрішній мембрані цих органел і поділяються на три групи:.
1. Піридинзалежні дегідрогенази.
2. Флавінзалежні дегідрогенази.
3. Цитохроми.
3.3.1. Піридинзалежні дегідрогенази.Піридинзалежні дегідрогенази отримали таку назву в зв’язку з цим, що в структуру їх небілкового компонента входить похідне піридину – нікотинамід. Тому їх ще називають дегідрогеназами. Ці дегідрогенази як кофермент містять:
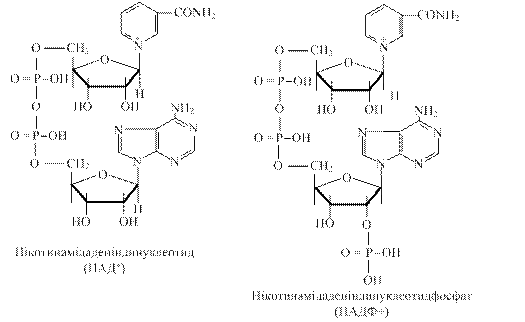
1) Нікотинамідаденіндинуклеотид (НАД+) складається з двох нуклеотидів: аденілової кислоти і нуклеотиду, в якого місце пуринової або піримідинової основи займає нікотинамід (вітамін РР). Ці нуклеотиди з’єднані через залишки фосфатів.
2) Нікотинамідаденіндинуклеотидфосфат (НАДФ+) - це НАД+, у якого в другому положенні рибози аденілової кислоти є додаткова фосфатна група.
Піридинзалежні дегідрогенази відносяться до складних ферментів, в яких НАД+ або НАДФ+ є коферментами, слабо зв’язаними з апоферментом і тому в клітині знаходяться окремо від білкової частини ферменту, виконуючи функцію носіїв атомів водню (протонів і електронів ). Ці дегідрогенази є універсальними акцепторами водню для багатьох субстратів: спиртів, альдегідів, кето- і гідроксикислот, дикарбонових кислот, амінів тощо. Специфічність дії цієї групи дегідрогеназ обумовлена білковою частиною ферменту, оскільки коферменти за своєю будовою подібні.
Дегідрування, як початкову стадію біологічного окиснення з участю піридинзалежних дегідрогеназ на прикладі молочної кислоти, можна представити так:
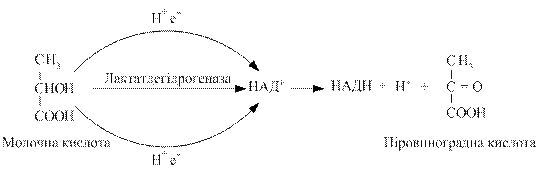
Здатність НАД+ і НАДФ+ виконувати функцію проміжного перенощика водню пов’язана з наявністю в його структурі аміду нікотинової кислоти.
3.3.2. Флавінзалежні дегідрогенази. Вони містять у своїй структурі небілковий компонент флавінове кільце – вітамін В2. Одні з них виконують функцію первинного дегідрування певних субстратів (янтарна кислота, похідні жирних кислот та інші). Вони здатні відщеплювати й приймати водневі від субстратів, при цьому виключається дія піридинзалежних дегідрогеназ. Інші оксидази можуть зразу при дегідруванні субстратів передавати протони й електрони на молекулярний кисень з утворенням пероксиду водню, забираючи від НАД·Н+ Н+.
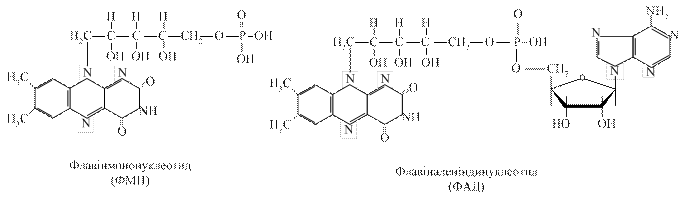
Флавінові ферменти є проміжними перенощиками водню від НАДН+Н+ на сполуку наступного етапу дихального ланцюга (убіхінон). Первинні дегідрогенази розміщуються на внутрішній поверхні внутрішньої мембрани мітохондрій.
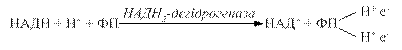
Відщепленні від НАДН+ Н+ електрони й протони (атоми водню) приєднуються до атомів азоту в 1-му і 10-му положеннях ізоалоксазинового кільця рибофлавіну, при цьому проходить переміщення подвійних спряжених зв’язків:

3.3.3. Убіхінон. Це жиророзчинний хінон, який має довгий ненасичений ланцюг. Він присутній практично у всіх клітинах. Його молекула здатна приєднувати атоми водню, що супроводжується переходом з окисленої форми у відновлену. Убіхінон може приймати участь в одно- і двоелектронному перенесенні. Молекула убіхінону має високу гідрофобність за рахунок бічного ланцюга. Це сприяє швидкій його дифузії в ліпідних фазах внутрішньої мітохондріальної мембрани. Убіхінон є похідним бензохінону з довгим бічним ланцюгом, який в більшості тканин ссавців складається з 10 ізопреноїдних залишків. На даний час встановлена коферментна роль убіхінону, який здійснює перенесення електронів і протонів, дифундуючи від внутрішньої поверхні мембрани до зовнішньої. Загальну реакцію третього етапу можна зобразити так:
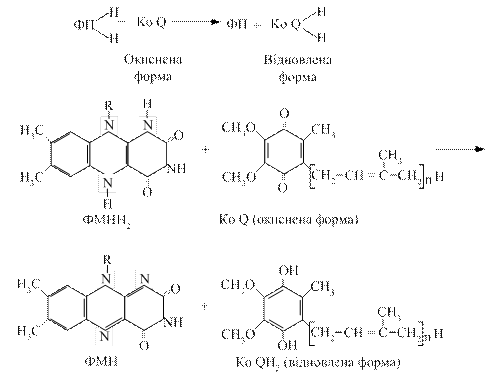
При цьому відновлена форма флавопротеїну окиснюється і може знову включатись у дихальний ланцюг.
3.3.4. Цитохроми. Цитохромна система складається з ряду ферментів, небілкова частина яких представлена залізопорфіринами, подібними до гему. Відомо чотири типи гемів, їх позначають латинськими буквами а,в,с. В процесах тканинного дихання велику роль відіграють цитохроми b, с1, с, а, а3. Цитохроми відрізняються будовою білкової частини, природою бічних ланцюгів і способом приєднання гему до білків. Атом заліза в гемі може змінювати валентність, приєднуючи або віддаючи електрон:
Fe3+ + e- ® Fe2+
Fe2+ - e- ® Fe3+
Установлено, що цитохроми розміщуються між КоQ і киснем. У дихальний ланцюг вони включаються в залежності від окиснювально-відновного потенціалу в основному в такій послідовності: b, с1, с, а, а3.
Комплекс цитохромів в і с1 переносить електрони від атомів водню відновленого КоQ·Н2 на цитохром c. Електрони послідовно проходять через атоми заліза цитохромів в і с1, потім поступають на цитохром с, протони при цьому вивільняються у внутрішнє середовище. Цитохром с – це залізовмісний білок з невеликою молекулярною масою (12000 Да), який складається з одного поліпептидного ланцюга і порфіринової групи з атомом заліза.

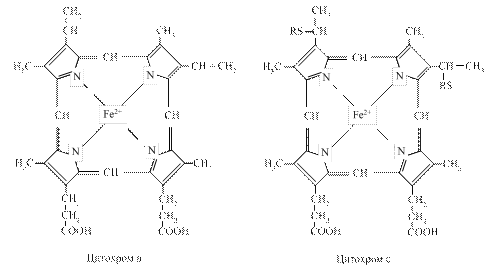
Цитохром с переносить електрони. Знаходиться поблизу внутрішньої мембрани і, очевидно, може виходити в міжмембранний простір. Він виконує як би човникові рухи між цитохромом b і комплексом цитохромів а і а3, дифундуючи вздовж поверхні мембрани.
3.3.5. Етапи тканинного дихання. Перший етап тканинного дихання починається з дегідрування, тобто відщеплення водню від відповідного субстрату. Ці реакції здійснюються піридинзалежними (для одних субстратів), а для інших флавінзалежними дегідрогеназами. Другий етап полягає в перенесенні в дихальному ланцюзі двох атомів водню від відновленої форми НАДН+ Н+ на флавопротеїни – проміжні переносники атомів водню. Третій етап– перенесення електронів і протонів від відновлених флавопротеїнів на убіхінон, який ще називають коферментом Q (КоQ). Потім в дихальному ланцюзі шляхи електронів і протонів розходяться (четвертий етап): електрони атомів водню від відновленої форми КоQ поступають на цитохромну систему, а протони звільняються у внутрішнє середовище. Комплекс цитохромів а і а3 переносить електрони на кисень. У результаті цього утворюється активний кисень, який взаємодіє з двома протонами з матриксу, утворюючи воду (рис. 3.2).
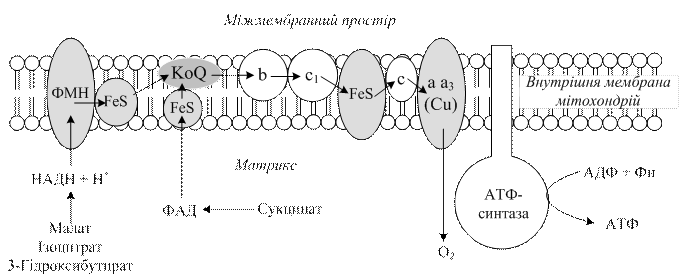 Рис.3.2. Схема організації компонентів дихального ланцюга мітохондрій
Рис.3.2. Схема організації компонентів дихального ланцюга мітохондрій
Перенесення протонів і електронів проходить завжди від меншого до більшого потенціалу (рис. 3.3). Різниця потенціалів між відновленим і окисненим субстратом називається редокс-потенціалом і вимірюється у вольтах.
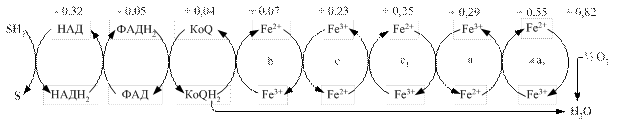
Рис. 3.3. Схема організації дихального ланцюга мітохондрій
Існують подовжені і скорочені шляхи тканинного дихання. Прикладом подовженого шляху є окиснення α-кетокислот.
Вони спочатку піддаються окиснювальному декарбоксилюванню (проходить втрата карбоксигрупи α -кетокислот з утворенням СО2), а два водні передаються на ліпоєву кислоту, потім діють нікотинамідні ферменти і вже НАДН2 включається в дихальний ланцюг. Скороченим шляхом окиснюється, наприклад (бурштинова) янтарна кислота:

При цьому процес дегідрування здійснюють флавінзалежні дегідрогенази, тобто виключається дія нікотинамідних дегідрогеназ. В живих організмах може відбуватися скорочений шлях аеробного окиснення органічних речовин без участі цитохромної системи. В цьому випадку водні окисненого субстрату зразу переносяться особливими металовмісними флавіновими ферментами (оксидазами) на молекулярний кисень з утворенням пероксиду водню. Утворений пероксид водню є сильною отрутою для клітини. Його знешкодження здійснюється за допомогою гемвмісних ферментів: каталази і пероксидази (рис. 3.4).
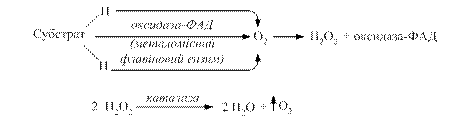
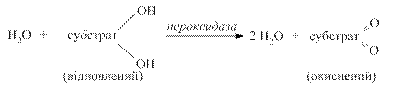
Рис. 3.4. Схема утворення пероксиду водню та механізм його знешкодження каталазою та пероксидазою
Каталаза – дуже активний фермент; одна її молекула розкладає до 4000 молекул Н2О2 за 1с. Пероксидаза в тканинах тварин малоактивна порівняно з каталазою. Рослинні клітини навпаки багаті на пероксидазу. Для каталази субстратом і донором електронів служать молекули пероксиду водню, а для пероксидази – органічний субстрат.
Читайте також:
- II. Організація і проведення спортивних походів
- II. Організація перевезень
- II. Організація перевезень
- А. Організація Острозького колегіуму – Академії
- Адміністративно-територіальна організація
- Бюджетний устрій в зарубіжних країнах. Організація бюджетного процесу
- Бюрократична організація
- Вентиляція. Види вентиляції. Організація повітрообміну в приміщеннях, повітряний баланс, кратність повітрообміну
- Взаємини з агентствами та організаціями
- Взаємодія органів публічної влади з трудовими колективами, підприємствами, установами, організаціями
- Вибір оптимального розкладу (режиму) роботи в наукових організаціях.
- Види податкових перевірок. Організація і здійснення перевірок.
Переглядів: 7087
| <== попередня сторінка | | | наступна сторінка ==> |
| Сучасні уявлення про тканинне дихання | | | Окиснювальне та субстратне фосфорилування |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |