
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
ЇХ ХАРАКТЕРИСТИКА
Розчинники – рідини, які застосовують для розчинення різних речовин, здебільшого твердих.
Всі розчинники поділяють на дві групи: неорганічні й органічні. Серед неорганічних розчинників найбільше практичне значення має вода, що є найуніверсальнішим розчинником, оскільки з усіх розчинників вона розчиняє найбільшу кількість речовин. Розчинювальна здатність води зумовлена будовою її молекул. Молекули води характеризуються сталим дипольним моментом: в процесі розчинення молекули води взаємодіють з іншими молекулами та іонами. Велике значення має здатність води утворювати водневий зв’язок з іншими сполуками, якщо в їхньому складі є атоми з великою електронегативність (Оксиген, Нітроген, Сульфур тощо).
У природі найбільш поширеними є саме водні розчини, й на Землі рідко зустрічаються розчини на неводній основі (нафта).
Органічні розчинники є менш універсальними. Кожний з них розчиняє лише обмежену кількість твердих або рідких речовин. Відомо дуже багато органічних сполук, які застосовуються як розчинники, з них найпоширенішими є:
1) вуглеводні – петролейний ефір, бензин, гас, бензол, толуол, ксилол, пропан і інші;
2) спирти – ізопропіловий, аміловий, метиловий, етиловий тощо;
3) аміни – диметиламін, етиламін, анілін;
4) кетони – ацетон, метилетилкетон тощо;
5) хлорорганічні сполуки – тетрахлорид карбону, дихлоретан, хлороформ та інші;
6) сполуки, що містять азот, - нітрометан, нітробензол тощо.
Часто застосовують суміші різних розчинників. Переважна більшість органічних розчинників є горючими і леткими (tокип. 30-200оС), тому з повітрям вони утворюють вибухові суміші. Майже всі вони є отруйними. Органічні розчинники широко застосовують у різних галузях промисловості – лакофарбовій, текстильній, пластичних мас, вибухових речовин та інших, а також у сільському господарстві, медицині тощо.
Вода як розчинник. (від лат. aguа) Вода (Н2О) – найпростіша хімічна сполука водню з киснем. Є ізотопна різновидність води – вода важка. При нормальних умовах вода – безколірна, блакитнувата рідина. Вода є головною складовою частиною гідросфери. Значна кількість води у вигляді пари міститься в атмосфері. Вода входить до складу ґрунту, багатьох мінералів і гірських порід; є складовою частиною всіх живих організмів. Для життя людини вода є дуже важливою, оскільки життя існує лише у водних розчинах, і будь-яка клітина живого організму являє собою водний колоїдний розчин. Вода становить до 75% загальної маси тіла людини. Особливо велика кількість її в плазмі крові, лімфі, травних соках. Основна функція води в організмі полягає в тому, що вона є розчинником більшості речовин. За участю води відбуваються важливі фізико-хімічні процеси у клітинах і тканинах. Вода має велику теплоємність, завдяки чому вона переносить тепло по всьому організмові і вирівнює температуру тіла. При випаровуванні з поверхні тіла вода забирає надлишок тепла.
Дистильована вода. (Aqua destillata). Розчини лікарських речовин для зовнішнього та внутрішнього застосування готують тільки на дистильованій воді. Дистильована вода найбільш широко використовується як розчинник для виготовлення ліків. Дистильована вода повинна бути безбарвною, прозорою, без запаху і смаку. рН дистильованої води повинен бути в межах 5,0-6,8. Вона не повинна містити хлоридів, сульфатів, нітратів, солей кальцію і важких металів.
Для одержання дистильованої води в аптечних умовах використовують водопровідну воду, в сільській місцевості, де немає централізованого водопостачання, воду безпосередньо, без будь-якої обробки, дистилюють. Принцип дистиляція води полягає в наступному. Воду нагрівають в перегінній посудині до кип’ятіння і пару, яка утворюється, конденсують шляхом охолодження. Конденсат дистильована вода – таким чином звільняється від не летючих домішок і стає придатна для виготовлення ліків.
Вода для ін’єкцій (Aqua pro ijectionibur). Для виготовлення лікарських форм і водорозчинних препаратів (а також для очних крапель, розчинів для зрошення і для промивання ран) використовують воду для ін’єкцій, яка незалежно від вимог до дистильованої води, повинна задовольняти вимогам на відсутність пірогенних речовин.
Воду для ін’єкцій зберігають в спеціальних умовах, які виключають можливість попадання в неї мікроорганізмів із навколишнього середовища (асептичні умови). Вода для ін’єкцій придатна для виготовлення відповідних лікарських форм протягом не більше 24 годин з моменту її одержання.
Демінералізована вода. (Aqua demineralisata). Одержується шляхом знесолення водопровідної води за допомогою спеціальних іоннообмінних смол. Демінералізована вода може використовуватися для миття аптечного посуду, різноманітних упаковок. Вода демінералізована не повинна використовуватися для парентерального застосування, але може використовуватись для виготовлення всіх рідких лікарських форм, розчинів, реактивів. У випадку використання демінералізованої води для виготовлення очних ліків вона повинна бути простерилізована безпосередньо перед виготовленням ліків.
Спирти. (від лат. Spiritus), алкоголі – органічні сполуки, гідроксильні похідні вуглеводнів, що містять гідроксильну (ОН) групу при насиченому атомі Карбону. Розрізняють спирти аліфатичні – насичені (наприклад: етиловий С2Н5ОН), та спирти циклічної будови: аліциклічні, ароматичні, гетероциклічні. Спирти поділяють на одноатомні, двоатомні (гліколі), триатомні (гліцерини) та багатоатомні. Найпростіші спирти – безбарвні рідини, розчинні у воді.
Широко застосовують спирти як розчинники, сировину для штучного каучуку та смол, лікарських та вибухових речовин, парфюмерних виробів тощо.
Етиловий спирт. (Spiritus aethyticis, Spiritus vini). Офіціальними є розчини етилового спирту 95%, 90%, 70%, 40%. Етиловий спирт одержують в результаті бродіння крохмаловмісної сировини, головним чином картоплі і зерна. Після очищення від різноманітних домішок і зміцнення шляхом застосування спеціальної технології (ректифікація) одержують спирт потрібної концентрації. Чистий етиловий спирт – це легко рухлива прозора рідина з характерним спиртовим запахом і пекучим смаком. Він леткий, легко загоряється. Етиловий спирт є гарним розчинником для великої групи лікарських речовин – ефірних олій, органічних кислот, смол, йоду і легко змішується з іншими розчинниками – водою, гліцерином, діетиловим ефіром, хлороформом. При змішуванні спирту з водою спостерігається розігрівання суміші і зменшенні її об’єму в порівнянні з сумою об’ємів, що складають суміш (явище контракції).
Як розчинник етиловий спирт має широке застосування в фармацевтичній технології, в основному для виготовлення розчинів для зовнішнього і внутрішнього використання, а в багатьох випадках для приготування ін’єкційних ліків. У зв’язку із значною залежністю розчинної здатності етилового спирту від його концентрації – процентного вмісту абсолютного (безводного) спирту в спиртовому розчині – при використанні водно-спиртових розчинів необхідно знати його концентрацію. В аптечній практиці застосовують тільки розчини спирту, переважно водні; в заводських умовах більш ширше використовують абсолютний, безводний етиловий спирт. Концентрація спиртового розчину зазвичай виражається в процентах по масі, що показують вміст безводного спирту (в грамах) в 100г спиртового розчину, або в процентах по об’єму, що показують вміст абсолютного спирту (в мілілітрах) в 100мл спиртового розчину. Переведення одних процентів в інші має місце в практичній діяльності фармацевтів і здійснюється за спеціальними формулами.
У фізіологічному відношенні спирт є далеко не індиферентною допоміжною речовиною, що слід мати на увазі при його використанні.
Спиртові розчини, починаючи з 15-20%, мають бактеріостатичні і бактерицидні властивості, що дозволяє застосовувати їх з метою дезинфекції аптечного посуду, хірургічних інструментів, рук. В фармакологічному відношенні спирт є представником групи речовин наркотичної дії.
Розчин етилового спирту будь-якої концентрації зберігають в добре закупорених скляних пляшках (для попередження випаровування), в прохолодному місці, далеко від вогню.
Ефір медичний – (Aethes medicinalis) – це безбарвна, легко рухлива летка рідина зі своєрідним запахом і смаком. Добре змішується з спиртом, жирними та ефірними маслами. Використання ефіру як розчинника вимагає дотримання низки запобіжних заходів внаслідок того, що цей препарат легко загоряється, а його пари вибухонебезпечні. Як допоміжну речовину ефір використовують в різних фармацевтичних процесах – при розчиненні, для полегшеного подрібнення твердих лікарських речовин, а також при виготовленні лікарських форм, головним чином для внутрішнього та зовнішнього застосування. Зберігають ефір в склянках оранжевого кольору, у прохолодному, захищеному від світла і відкритого полум’я місці.
Гліцерин. (Glycerinum). В медичній практиці зазвичай використовується гліцерин, що містить 12-16% води. Це прозора, безбарвна, без запаху в’язка рідина з солодкуватим смаком. Має виражену розчинну здатність по відношенню до значної кількості лікарських речовин. В гліцерині добре розчинні: танін, атропіну сульфат, калія йодид, гексаметилентетраамін, анестезин, борна кислота, ацетилсаліцилова кислота, натрію гідрокарбонат, цинку сульфат і інші. Гліцерин нерозчинний у жирних маслах, практично нерозчинний в ефірі, але змішується в усіх співвідношеннях з водою і етиловим спиртом. Препарат дуже гігроскопічний. Зазвичай розчинення лікарських речовин у гліцерині проводять на водяній бані (40-50оС). Гліцерин зберігають в широкогорлих щільно закритих штангласах.
J Тест на тему" Фазова рівновага та вчення про розчини"
| Питання | Варіанти відповіді |
| 1. 3 пониженням температури розчинність газів… | а) збільшується; б) зменшується; в) залишається сталою. |
| 2. Підвищення температури кипіння розчину… | а) прямо пропорційна його моляльності; б) прямо пропорційне його концентрації; в) обернено пропорційне його моляльності; г) обернено пропорційне його концентрації. |
| 3. Тиск насиченої пари розчинника над розчином… | а) завжди більший, ніж над чистим розчинником; б) завжди менший, ніж над чистим розчинником; в)залишається сталим, як і над чистим розчинником. |
| 4. 3акон Рауля : "Тиск насиченої пари розчинника над розчином дорівнює… | а) відношенню його тиску на молярну частку розчинника; б) відношенню молярної долі розчинника на його тиск над чистим розчинником; в) добутку його тиску над чистим розчинником на молярну частку розчинника |
| 5. Закону Рауля підкоряються розчини… | а) ідеальні; б) насичені; в) перенасичені; г) розбавлені. |
6. Відносне зниження тиску пари розчинника над розчином за законом Рауля справджується розчинів, коли… 
| а) розчинник леткий, а розчинена речовина нелетка; б) розчинник нелеткий, а розчинена речовина летка; в) і розчинник і розчинена речовина леткі речовини; г) і розчинник і розчинена речовина нелеткі речовини |
| 7. Тиск насиченої пари тим… | а) більший, чим більша концентрація розчину; б) менший, чим більша концентрація розчину; в) менший, чим менша концентрація розчину. |
| 8. Розчин замерзає при температурах… | а) більш низьких, ніж чистий розчинник; б) більш високих, ніж чистий розчинник; в) таких самих, як і чистий розчинник. |
| 9. Від чого залежить розчинність у воді твердих речовин і газів? | а) від температури, концентрації, об'єму; б) від природи розчинної речовини , температури , тиску; в) від тиску, маси розчинники, об'єму розчинної речовини ; г) від природи розчинної речовини , концентрації, об'єму розчинення, температури. |
| 10. На розчинність СО2 у воді не впливає… | а) тиск; б) температура; в) швидкість пропускання газу; г) хімічна взаємодія газу з водою. |
| 11. Закон Генрі: | а) "Розчинність газів при постійному тиску прямо пропорційна температурі газів над розчином"; б) "Розчинність газу при постійному тиску прямо пропорційна концентрації газу в розчині"; в) "Розчинність газу при постійній температурі прямо пропорційна тиску газу над розчином; г) "Розчинність газу при постійній температурі прямо пропорційна концентрації газу в розчині". |
| 12. Молярна концентрація - це відношення… | а) об'єму розчину до кількості розчиненої речовини; б) маси розчину до маси розчиненої речовини; в) кількості розчинної речовини до об'єму розчину; г) кількості розчиненої речовини до маси розчину; д) кількості розчинника до маси розчину. |
| 13. Молярна частка - це відношення… | а) кількості компонентів розчину до загальної кількості молей всіх компонентів; б) загального числа молей всіх компонентів до числа молей одного з компонентів розчину в) загального числа компонентів розчину до кількості молей одного з компонентів розчину; г) числа молей одного з компонентів розчину до загального числа компонентів розчину. |
| 14. Кріоскопічну сталу можна розрахувати по формулі… | а) Кзам = ΔТзам. m;
б) Кзам = ΔТзам .С ;
в) Кзам = 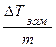 г) Кзам= ΔТзам
C
д) Кзам =
г) Кзам= ΔТзам
C
д) Кзам = 
|
| 15. Молярну масу розчиненої речовини можна розрахувати за формулою: | а) М = 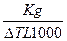 ; в) М = ; в) М = 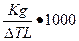 б) М =
б) М =  ; Г) М = ; Г) М = 
|
| 16. При наявності третього компонента розчинність газів… | а) збільшується; б) зменшується; в) залишається сталою. |
| 17. Концентрація насиченого розчину будь-якої речовини при даній температурі… | а) постійна; б) збільшується ; в) зменшується. |
| 18. Процес розчинення більшості твердих речовин… | а) ендотермічний; б) екзотермічний. |
| 19. Моляльність розчину розраховують за формулою: | а) m = g∙М∙L∙ 1000; б) m = М∙L/g∙ 1000; в) m = (М∙g)/(L∙1000); г) m = g/(M∙L)1000. |
| 20. Ебуліоскопічна стала залежить… | а) від природи розчиненої речовини і не залежить від природи розчинника; б) від природи розчинника і не залежить від природи розчиненої речовини; в) від природи розчинника і від природи розчиненої речовини . |
´ Контрольні запитання.
1. Які розчини називаються істинними?
2. Що називається розчином?
3. В яких випадках при розчиненні речовин процес має екзотермічний характер?
4. Що показує масова частка розчиненої речовини?
5. Чим відрізняється моляльна концентрація від молярної?
6. Від яких факторів залежить розчинність газів у рідинах?
7. Що таке дифузія?
8. Від яких факторів залежить швидкість дифузії?
9. Що таке осмос?
10. Як розрахувати осмотичний тиск ідеального розчину?
11. Що таке тургор і плазмоліз? Яке їх значення?
12. Які розчини називають ізотонічними, гіпотонічними, гіпертонічними?
13. Що таке кріоскопія та ебуліоскопія?
14. Для вирішення яких питань використовують кріоскопічний та ебуліоскопічний методи?
15. Дайте визначення і вкажіть розмірність кріоскопічної та ебуліоскопічної сталої розчинника.
16. Що називається фазою, компонентом, числом ступенів свободи?
17. Дайте визначення основних фазових переходів.
18. Як класифікують гетерогенні системи?
19. Чому дорівнює число незалежних компонентів системи?
20. Чому дорівнює число ступенів свободи системи?
21. Творче завдання: Підготувати повідомлення про вчених-хіміків: про Гіббса, про Вант-Гоффа, про Рауля.
ТЕМА 1.3. ЕЛЕКТРОХІМІЯ
Читайте також:
- I. Загальна характеристика політичної та правової думки античної Греції.
- II. ВИРОБНИЧА ХАРАКТЕРИСТИКА ПРОФЕСІЇ
- II. Морфофункціональна характеристика відділів головного мозку
- Аварії на хімічно-небезпечних об’єктах та характеристика зон хімічного зараження.
- Автобіографія. Резюме. Характеристика. Рекомендаційний лист
- Автокореляційна характеристика системи
- Амплітудно-частотна характеристика, смуга пропускання і загасання
- Аналіз розриву», його характеристика
- Анатомо-біомеханічна характеристика положень і рухів тіла
- Антична філософія як перший етап західної філософської традиції. Загальна характеристика
- Аплікація як вид образотворчої діяльності дошкільнят, його характеристика.
- Архітектура СЕП та характеристика АРМ-1, АРМ-2, АРМ-3
| <== попередня сторінка | | | наступна сторінка ==> |
| | | ЕЛЕКТРИЧНА ПРОВІДНІСТЬ РОЗЧИНІВ. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |