
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Гормони периферичних залоз
ПОМК
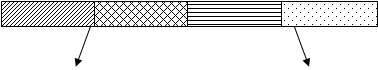 |
АКТГ (1-39) β-ЛПГ (42-134)
 |  | ||
α-МСГ (1-13) КТПП (18-39) γ-ЛПГ (42-101) β-ендорфін (104-134)
 |  |  |  | ||||
β-МСГ (84-101) γ-ендорфін (104-118)


 |
α-ендорфін (104-117)
 |
Рецептори для білково-пептидних гормонів (та інших біорегуляторів) поділяють на два класи:
1) рецептори І класу - іонотропні рецептори. При взаємодії біорегулятора з таким рецептором відбувається відкриття іонових каналів на плазматичній мембрані і генерація швидких іонових потоків. Результатом цього є відповідна клітинна відповідь;
2) рецептори ІІ класу - метаботропні рецептори. Результатом взаємодії біорегулятора з таким рецептором є зміна метаболічних процесів у клітині.
2 Гормони - похідні амінокислот - це низькомолекулярні водорозчинні сполуки, які мають у своєму складі аміногрупу. Вони утворюються в результаті метаболізму амінокислот. Прикладом гормонів цього класу є адреналін і тиреоїдні гормони, які утворюються з амінокислоти тирозину.
3 Стероїдні гормони - це жиророзчинні сполуки, похідні холестеролу. До них належать кортикостероїди, андрогени і естрогени.
4 Біорегулятори - похідні арахідонової кислоти - це гістогормони. До них належать простагландини, тромбоксани, лейкотрієни, простациклін.
Існують також інші типи класифікації гормонів. З біохімічної точки зору найбільш цікавою є класифікація залежно від клітинної локалізації рецептору і механізму реалізації гормонального сигналу. За цією класифікацією гормони поділяють на дві групи:
1) гормони, які не проникають в клітину і для них рецептор локалізований на поверхні плазматичної мембрани. До цієї групи належать білково-пептидні гормони та похідні амінокислот, будова і фізико-хімічні властивості яких не дозволяють проходити через біліпідний шар плазматичної мембрани. Ці гормони діють через сполуки, які утворюються в клітині у відповідь на дію гормону і є “представниками” гормону в клітині - це месенджери (або вторинні посередники);
2) гормони, які проникають крізь плазматичну мембрану і взаємодіють з рецепторами, які локалізовані в середині клітини (цитоплазмі, іноді в ядрі). До гормонів цієї групи належать ліпофільні сполуки - стероїдні та тиреоїдні гормони.
2 Регуляція секреції гормонів
Дія гормонів пропорційна їх концентрації в крові. Таким чином, концентрація гормонів в крові повинна змінюватися відповідно до потреб організму.
Частково кількість активного гормону в крові визначається швидкістю інактивації гормону і видаленням його з комплексу “білок сироватки крові - гормон”.
Другим, найбільш важливим фактором, який визначає розміри пулу любого гормону в крові, є швидкість його секреції
відповідною ендокринною залозою - тобто швидкість надходження гормону в кровоток.
Ендокринна система повинна постійно отримувати “інформацію” про концентрацію гормону в крові. Це забезпечується завдяки існуванню спеціального механізму регуляції секреції гормонів - механізму зворотного зв’язку.
Існує два види механізмів зворотного зв’язку регуляції секреції гормонів:
1) негативний зворотний зв’язок;
2) позитивний зворотний зв’язок.
1 Перший механізм бере участь в регуляції секреції практично всіх ендокринних органів. Другий механізм реалізується рідко, але також є важливим при певних ендокринних станах.
Розглянемо функціонування регуляції за принципом негативного зворотного зв’язку. Координуючим центром ендокринної системи є гіпоталамус, який отримує та інтегрує сигнали, що надходять з нервової системи. У відповідь на ці сигнали гіпоталамус секретує рілизинг гормони (ліберини), які транспортуються в аденогіпофіз. Кожний гіпоталамічний гормон регулює секрецію одного відповідного гормону гіпофіза - тропного гормону. Тропні гормони діють на відповідні ендокринні залози і стимулюють секрецію специфічних гормонів у кров. При підвищенні цих гормонів у крові, вони за принципом зворотного зв’язку інгібують секрецію і гормонів гіпофіза, і гормонів гіпоталамуса. Таким чином знижується секреція гормонів периферійних ендокринних залоз - реалізується принцип негативного зворотного зв’язку.
Прикладом може бути регуляція секреції тиреоїдних гормонів (Т3 і Т4).
Головні компоненти, які складають петлю негативного зворотного зв’язку - це Т3, Т4, ТТГ і тироліберин. Т4 і Т3 гальмують свій власний синтез за механізмом зворотного зв’язку. Медіатором цього процесу може служити Т3, оскільки Т4 у гіпофізі перетворюється в Т3, який подавляє секрецію ТТГ. У гіпоталамусі Т3 (або, можливо, Т4) гальмує утворення і секрецію тироліберина. Стимулом для підвищення секреції тироліберина і ТТГ є зниження концентрації тиреоїдних гормонів у крові.
|
 Гіпоталамус
Гіпоталамус
 | |||||
 | |||||
 | |||||
(-) (+) (-)
|
 Гіпофіз
Гіпофіз
 +
+
(+)
|

|

Існує цікава взаємодія петель зворотного зв’язку для щитоподібної залози і соматостатину, який також забезпечує регуляторні механізми секреції Т3 і Т4. А саме Т3 і Т4 підсилюють вивільнення соматостатину із гіпоталамуса, який також інгібує секрецію тиротропіна.
У маленьких дітей, які отримують терапію гормоном росту, іноді розвивається гіпотиреоз. Це пов’язано з тим, що СТГ стимулює секрецію соматостатина, який (за вище описаним механізмом) інгібує секрецію ТТГ і відповідно Т3 і Т4.
У реалізації другого механізму - за принципом позитивного зворотного зв’язку можуть приймати участь не лише гормони, а й деякі метаболіти. Першим прикладом може бути регуляція концентрації глюкози в крові під дією інсуліну.
Після прийому їжі в крові зростає концентрація глюкози, яка в свою чергу стимулює секрецію інсуліну. Підвищення концентрації інсуліну призводить до зниження рівня глюкози в крові. Після чого концентрація інсуліну знижується. Тобто реалізується механізм позитивного зворотного зв’язку - “чим більше, тим більше; чим менше, тим менше”.
Схематично це може бути подано таким чином:
(+)


 ↓ глюкоза крові → ↓ інсуліну ↓
↓ глюкоза крові → ↓ інсуліну ↓
(+)
 |
↓ глюкоза крові
Іншим прикладом може бути регуляція секреції естрогенів і прогестерона. Так естрогени і прогестерон стимулюють секрецію лютеїнізуючого гормону. Цей гормон сприяє процесу овуляції і формуванню жовтого тіла і відповідно підвищенню продукції естрогенів і прогестерона.
Транспорт гормонів
Транспорт гормонів у крові залежить від їх розчинності. Гідрофільні гормони (наприклад, білково-пептидні) транспорту-ються у вільному стані. Стероїдні і тиреоїдні гормони транспортуються в комплексі з білками плазми крові:
- специфічними транспортними білками (транспортні низькомолекулярні глобуліни, тироксинзв’язуючий білок, транскортин - білок для транспорту кортикостероїдів);
- неспецифічними транспортними білками - альбумінами.
3 Молекулярно-клітинні механізми дії гормонів
Існують два основні механізми дії гормонів:
1) мембранно-цитозольний;
2) цитозольний.
3.1 Мембранно-цитозольний механізм дії характерний для білково-пептидних гормонів і похідних амінокислот.
За фізико-хімічними властивостями це гормони, які не здатні проходити через біліпідний шар плазматичної мембрани в цитозоль. Саме тому для них рецептори знаходяться на поверхні клітини. Реалізацію дії цих гормонів у клітині забезпечують специфічні молекули, які утворюються в цитозолі у відповідь на дію гормону. Ці молекули називають месенджерами, або вторинними посередниками дії гормону. Месенджер є повноважним представником гормону в клітині. Вторинними посередниками дії гормонів можуть бути такі молекули, як цАМФ, цГМФ, ІТФ (інозитолтрифосфат), ДАГ (диацилгліце-рол), іони Са2+.
Першою молекулою, що була відкрита як месенджер, став цАМФ. У 1957 р. Сазерленд відкрив, що цАМФ є вторинним посередником дії адреналіну.
Нижче наведена таблиця, в якій подані гормони і відповідні вторинні посередники дії цих гормонів у клітині.
| Вторинний посередник | Приклади біорегуляторів | |
| цАМФ | Глюкагон, АКТГ, ТТГ, гонадотропіни, гона-доліберин, тироліберин, МСГ, вазопресин та інші | |
| цГМФ | α-передсердний Na уретичний пептид, аце-тилхолін, серотонін, NO, брадикінін | |
| ІТФ, ДАГ, Са2+ | Гастрин, тироліберин, вазопресин, ангіо-тензин ІІ, паратгормон, лейкотрієни |
цАМФ як вторинний посередник дії гормонів
Послідовність процесів, які відбуваються при активації синтезу цАМФ у клітині під дією гормону має такий вигляд.
Система, яка забезпечує синтез цАМФ - аденілатциклаза система - складається з трьох компонентів: рецептора, регуляторного білка - трансдуктора (G-білка) і каталітичної субодиниці - аденілатциклази.
Гормон зв’язується з рецептором, який знаходиться на поверхні плазматичної мембрани. У результаті цього процесу відбуваються конформаційні зміни в структурі рецептора, які передаються на спеціальний білок - трансдуктор (G-білок). Цей білок знаходиться у плазматичній мембрані і передає інформацію про зв’язування гормону з рецептором до ферменту аденілатциклази (АДЦ).
Сигнальні G-білки здатні зв’язувати ГТФ і ГДФ. У неактив-ному стані вони зв’язані з ГДФ. При активації ГДФ заміщується на ГТФ.
Існує декілька видів G-білків:
1) Gs - це G-білки, які стимулюють аденілатциклазу;
2) Gi - це G-білки, які інгібують аденілатциклазу;
3) Go - G-білок з невідомою функцією;
4) Gt - це трансдуцин, який бере участь в АДФ-рибозилювання при дії холерного токсину;
5) Gq - це G-білки, які активують фосфоліпазу С.
Аденілатциклаза - фермент, який є глікопротеїном.
Після активації цей фермент каталізує реакцію синтезу цАМФ із АТФ:
Mg2+
 АТФ цАМФ + ФФн
АТФ цАМФ + ФФн
Вважають, що цАМФ є найважливішим вторинним посередником дії біорегуляторів.
У результаті концентрація цАМФ у цитозолі швидко досягає максимальних значень (≈10-6М).
Далі цАМФ активує цАМФ-залежну протеїнкіназу (ПКА). ПКА містить 4 субодиниці: дві R-регуляторні і дві С - каталітичні. При активації 4 молекули цАМФ приєднуються до 2R-субодиниць і відбувається дисоціація ПКА - 2С субодиниці відділяються. У такому вигляді ПКА активна. Після активації цей фермент фосфорилює (за участі АТФ) біологічно активні білки - ферменти, рецептори, канальцеві білки, ядерні гістони, фактори транскрипції та інші.
Фосфорилювання відбувається, як правило, за сериновими, треоніновими або тирозиновими залишками цих білків. У результаті це призводить до активації або інактивації вказаних білків і виникає відповідна клітинна відповідь.
|
|



 ПКА 4цАМФ (не
ПКА 4цАМФ (не

 активна)
активна)


 цАМФ
цАМФ

 Г Р
Г Р
АТФ
|
|
цАМФ цАМФ
 |  |
Позначення: цАМФ цАМФ
 Г - гормон ПКА активна
Г - гормон ПКА активна
Р - рецептор
Gs - білок-трансдуктор
 АДЦ - аденілатциклаза
АДЦ - аденілатциклаза
 R - регуляторні субодиниці АДЦ АТФ
R - регуляторні субодиниці АДЦ АТФ
С - каталітичні
субодиниці АДЦ



 АДФ
АДФ
|
Після припинення дії біорегулятора для відновлення початкового стану метаболізму в клітинах існують ферменти, які забезпечують зниження концентрації цАМФ і дефосфорилювання білків:
1) фосфодиестераза - каталізує розщеплення цАМФ:
цАМФ → АМФ
Цей фермент активується під дією інсуліну.
Встановлений цікавий факт інгібування цього ферменту кофеїном, тобто кофеїн пролонгує дію гормонів, для яких цАМФ є вторинним посередником (наприклад, адреналіна).
2) фосфатази - каталізують дефосфорилювання білків.
Таким чином, функціонування фосфодіестерази і фосфатаз повністю знімає вплив, який викликаний дією гормону.
цГМФ як вторинний посередник дії гормонів
Синтез цГМФ каталізує гуанілатциклаза, яка в клітині знаходиться як в мембранно–зв’язаному, так і в розчинному станах. Так, наприклад, 90% активності гуанілатциклази клітин тонкого кишечника знаходиться у мембранах, 10% - в цитозолі. У легенях і печінці лише 20% гуанілатциклазної активності знаходиться в мембранах.
У результаті активації гуанілатциклази концентрація цГМФ в клітині підвищується (до 10-7М). цГМФ активує цГМФ-залежну протеїнкіназу (ПК-G). Ця протеїнкіназа складається з двох субодиниць, які при активації не дисоціюють (як у випадку з ПКА). ПК-G в активному стані фосфорилює клітинні білки, що призводить до певної клітинної відповіді.
У клітині цГМФ викликає ефекти протилежні цАМФ. цГМФ, наприклад, активує фосфодіестеразу, яка гідролізує цАМФ, стимулює проліферацію клітин (цАМФ пригнічує), регулює клітинний цикл.
Через цГМФ-залежний механізм діє такий важливий біорегулятор, як NO. Молекула NO має властивості класичного месенджера. Так в міоцитах гладеньких м’язів NO активує цитоплазматичну гуанілатциклазу. цГМФ, який утворюється, активує ПК-G, що призводить до зниження рівня Са2+, розслаблення м’язів і розширення судин (це реалізується лише в разі дії через гуанілатциклазу).
Інозитолтрифосфат (ІТФ), диацилгліцерол (ДАГ)
та іони Са2+ як вторинні посередники
(фосфоінозитидна система)
Дія деяких гормонів у клітині реалізується через утворення таких месенджерів як ІТФ, ДАГ та іони Са2+.
При взаємодії гормону з рецептором, через білок-трансдук-тор Gq відбувається активація мембранно-зв’язаного ферменту фосфоліпази С. Цей фермент гідролізує фосфотидилінозитол-4,5-дифосфат (ФІ-4,5ДФ). У результаті гідролізу ФІ-4,5ДФ утворюються ІТФ і ДАГ.
ІТФ спричиняє вихід іонів Са2+ з ендоплазматичного ретикулуму (або саркоплазматичного ретикулуму) в цитозоль через стимуляцію відкриття мембранних каналів для кальцію.
Далі іони Са2+ зв’язуються з кальцій-зв’язуючим білком - кальмодуліном, який присутній практично в усіх клітинах. Комплекс Са2+-кальмодулін здатний регулювати активність багатьох Са2+/кальмодулін-залежних ферментів (різних протеїнкіназ, аденілатциклазу, фосфодиестеразу та інші). Зміна активності цих ферментів призводить до певної клітинної відповіді.
ДАГ - це другий вторинний посередник фосфоінизитидної системи, який активує мембранно-зв’язану протеїнкіназу С. Ця протеїнкіназа фосфорилює білки і виникає відповідна клітинна відповідь.
Припинення передачі гормонального сигналу через ІТФ, ДАГ і Са2+ здійснюється через:
1) Інактивацію ІТФ і ДАГ.
Від ІТФ послідовно відщеплюються три фосфатні групи і він перетворюється в інозитол.
ДАГ розщеплюється до фосфатидної кислоти або гліцеролу і жирних кислот.
2) Дефосфорилювання білків клітини протеїнфосфата-зами.
Мембранно-цитозольний механізм дії гормонів реалізується дуже швидко. Це пояснюється каскадною організацією процесів - клітинна відповідь досягається через послідовність активації ферментів. На кожному новому етапі в геометричній прогресії зростає кількість активованих молекул - лавиноподібна активація. Такий каскад нагадує піраміду, на вершині якої одна молекула гормону, а у основи - велика кількість молекул активо-ваних ферментів. Саме тому, наприклад, ефект адреналіну підсилюється і досягається дуже швидко - зв’язування кількох молекул адреналіну призводить до миттєвого виходу в кров декількох грамів глюкози (підсилення ≈ 25 млн. разів).
Са2+-месенджерова система
Іонам Са2+ належить центральна роль в регуляції багатьох клітинних функцій. Як месенджер Са2+ може функціонувати самостійно (не лише у складі фосфоінозитидної системи).
Зміна концентрації внутрішньо-клітинного вільного Са2+ є сигналом для активації або інгібування ферментів, які в свою чергу регулюють метаболізм, скорочувальну і секреторну активність, адгезію, клітинний ріст.
Джерела Са2+ можуть бути внутрішньо- і позаклітинні. Вони постачають Са2+ у відповідь на нейрогормональні сигнали. Са2+ зв’язується з кальмодуліном і комплекс Са2+-кальмодулін акти-вує Са2+-кальмодулін-залежну протеїнкіназу. Ця протеїнкіназа фосфорилює внутрішньоклітинні ферменти - “мішені”, тим са-мим регулює їх активність, що призводить до певної біохімічної або фізіологічної відповіді.
3.2 Цитозольний механізм діївластивий для гормонів, які здатні проходити через ліпідний шар плазматичної мембрани. Цей внутрішньоклітинний механізм реалізується при дії стероїдних і тиреоїдних гормонів. Яким чином названі гормони транспортуються в клітину невідомо, вважається, що завдяки пасивній дифузії.
У цитозолі гормон зв’язується з рецептором - утворюється гормон-рецепторний (Г-Р) комплекс. Далі Г-Р комплекс акти-вується. Результатом такої активації є зміна конформації рецеп-тора, що дозволяє йому зв’язуватися з відповідними сайтами ядерного хроматину. Таке зв’язування призводить до зміни (активації / інгібування) синтезу мРНК і білків - реалізується специфічна біохімічна або фізіологічна відповідь.
Прикладом можуть бути дія кортизолу (глюкокортикоїд) і альдостерона (мінералокортикоїд). Дія кортизолу через цито-зольний механізм запускає в печінці синтез білків-ферментів глюконеогенезу; альдостерон стимулює синтез мембранних транспортних білків для Na+ і, таким чином активує реабсорбцію Na+ в нирках.
Схематично цитозольний механізм зображений нижче:








 |  |










 Ядро ДНК
Ядро ДНК
 |  |  |  | ||||||||||||||||||
 | |||||||||||||||||||||
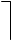 |  |  | |||||||||||||||||||
 |  | ||||||||||||||||||||
 | |||||||||||||||||||||





 Гормон Г мРНК
Гормон Г мРНК
 |  |  | |||||
 | |||||||
Рецептор Г-Р- Г-Р*
Комплекс (активний)


 мРНК
мРНК
 клітинна відповідь
клітинна відповідь
Білок
Тиреоїдні гормони в клітинах зв’язуються з рецепторами, які локалізовані в ядерному хроматині і їх наявність не залежить від наявності гормону. Взаємодія гормону з рецептором стимулює синтез мРНК, на якій синтезуються білки, що відповідають за клітинну реакцію на дію Т3 і Т4.
Таким чином, стероїдні і тиреоїдні гормони стимулюють транскрипцію генома (на відміну від білково-пептидних гормонів і похідних амінокислот, які діють на посттранскрип-ційні процеси). Саме тому клітинні реакції у відповідь на дію стероїдних і тиреоїдних гормонів розвиваються повільно і для гальмування їх дії також потрібен час.
4 Отримання і практичне використання гормонів
Для практичного використання гормони отримують:
1 Видаленням з біологічного матеріалу.
2 Шляхом хімічного синтезу.
3 За допомогою методів генної інженерії.
Першим способом отримують інсулін і глюкагон з підшлункової залози, кортикотропін і меланотропін з гіпофізів великої рогатої худоби.
Шляхом хімічного синтезу отримують всі стероїдні гормони і їх аналоги, гормони - похідні амінокислот, пептидні гормони (наприклад, окситоцин), білкові гормони.
З використанням методів генної інженерії отримані інсулін, соматостатин та інші.
У медичній практиці гормони використовують для замісного та патогенетичного лікування.
У першому випадку гормони використовуються в разі дефіциту їх в організмі (наприклад, СТГ, інсулін, тиреоїдні гормони та інші).
При другому підході використовують окремі властивості гормонів (наприклад, антизапальні - глюкокортикоїдів, анаболічні - анаболічних стероїдів - похідних тестостерону). У цьому випадку концентрація власних гормонів у організмі хворої людини знаходиться в межах норми.
5 Гормони гіпоталамуса і гіпофіза
5.1 Гіпоталамічні гормони
Однією з найважливіших ділянок ЦНС, яка координує і контролює функції ендокринних залоз є гіпоталамус. У ньому локалізовані нейросекреторні ядра і центри, що приймають участь в регуляції секреції і синтезу гормонів аденогіпофізу.
Гіпоталамус трансформує інформацію, яка надходить по нервових шляхах з вищих відділів нервової системи. Це досягається через зміну рівня нейромедіаторів, до яких належать різні моноаміни: адреналін, норадреналін, дофамін, серотонін, ацетилхолін, ГАМК. Стрес та інші фактори призводять до зміни вмісту, швидкості синтезу і секреції моноамінів у гіпоталамусі, які в свою чергу змінюють швидкість секреції гіпоталамічних гормонів. Таким чином, гіпоталамус - це ділянка безпосередньої взаємодії ЦНС і ендокринної системи.
У гіпоталамусі виділяються гормони (рилізинг-фактори), які впливають на ендокринну функцію гіпофізу:
1 Ліберини - стимулюють секрецію (а можливо і синтез) відповідних гіпофізарних гормонів.
2 Статини - пригнічують секрецію гормонів гіпофіза.
На теперішній час відомо 6 ліберинів і 3 статини.
Ліберини:
1) кортиколіберин - це пептид, який викликає підсилення секреції передньою часткою гіпофіза проопіомеланокортина (ПОМК) і відповідно тих гормонів, які утворюються з ПОМК:
- АКТГ;
- β-ендорфіну;
- ліпотропного гормону;
- меланоцитстимулюючого гормону.
Цей гормон також є нейропептидом, який бере участь в регуляції поведінкових (виникнення тривоги, страху, напруження, погіршення апетиту, сну, статевої активності) і імунопротекторних реакцій при стресі. Він також є фактором протизапального процесу. Кортиколіберин важливий в розвитку депресивних станів, зв’язаних з наркотичною залежністю. Тому його дія може бути розглянута як мішень терапевтичного впливу при відповідних патологіях;
2) тироліберин - трипептидний гормон, який стимулює секрецію тиреотропного гормону (ТТГ). Цей механізм реалізується через аденілатциклазу і фосфоліпазу С.
Крім того, тироліберин може брати участь у вивільненні пролактину, вазопресину, СТГ, кортикотропіну, соматостатину. Встановлено, що цей пептидний гормон може знижувати концентрацію Са2+ і гальмувати секрецію панкреатичних ферментів. Також він може діяти як антагоніст опіоїдної активності (без безпосереднього впливу на опіоїдні рецептори). Тироліберин також відносять до нейропептиду, який бере участь в регуляції деяких психічних функцій;
3) гонадоліберин (люліберин) - це пептидний гормон, який стимулює секрецію в кров гонадотропінів - лютеїнізуючого і фолікулостимулюючого гормонів (у більшій мірі впливає на секрецію першого).
Раніше існувала така точка зору, що гіпоталамус секретує люліберин, який вивільняє лютропін і фоліберин, який стимулює секрецію ФСГ. Ідентифікація структури цих ліберинів показало, що ці пептиди мають однакову послідовність. З точки зору сучасних уявлень про регуляцію секреції гонадотропінів існує єдиний ліберин - гонадоліберин.
Молекулярний механізм дії гонадоліберину - мембранно-цитозольний, через активацію фосфоліпази С. При довготри-валій дії гормону активація синтезу тропінів у гіпофізі відбувається при участі цАМФ.
Завдяки стимуляції секреції гонадотропінів цей гормон має важливе значення в регуляції репродуктивної функції людини, стимулює сперматогенез у чоловіків і дозрівання фолікулів у жінок, індукує овуляцію, бере участь в центральній регуляції репродуктивної поведінки.
Секреція гонадоліберину відбувається не постійно, а у вигляді коротких піків, послідовно один за одним через строго визначені інтервали часу.
Синтетичний препарат гонадоліберину використовується у медичній практиці для диференційної діагностики і лікування порушень репродуктивної функції, деяких форм гормонально залежних пухлин, наприклад, раку простати;
4) соматоліберин (соматокрінін) - пептидний гормон, який стимулює секрецію СТГ. У людини знайдені три структурні форми цього гормону, які відрізняються довжиною амінокислот-ної послідовності. Всі ці форми мають однакову біологічну активність.
Препарати соматоліберину та його біологічно активні фрагменти використовують у медицині з діагностичною та ліку-вальною метою як специфічні стимулятори секреції соматотро-піну;
5) пролактоліберин - гіпоталамічний гормон, який стимулює секрецію пролактину. Молекулярний механізм дії цього гормону полягає в активації аденілатциклази і фосфоліпази С;
6) меланоліберин - пентапептид, який стимулює секрецію меланоцитстимулюючого гормону.
Статини:
1) соматостатин - пептидний гормон, який інгібує секрецію значної кількості інших гормонів і моноамінів. Уперше цей гормон був виділений у мозку, пізніше показано наявність цього пептиду в периферичних тканинах. Гіпоталамічний соматоста-тин гальмує секрецію гормону росту в передній частині гіпофізу (а також тиротропіну і кортикотропіну).
У тканинах соматостатин існує в двох біологічно активних формах, які:
- гальмують секрецію інсуліну і глюкагону в підшлунковій залозі;
- гальмують секрецію гастрину і секретину в ШКТ;
- пригнічують секрецію реніну, (вазоактивного інцестинально-го пептиду) ВІП;
- інгібують секрецію соляної кислоти і пепсину шлунком;
- зменшують моторику кишечника;
- гальмують секрецію бікарбонатів і ферментів підшлункової залози;
- знижують процеси абсорбції в кишечнику, секреції і транспорту жовчі.
Широкий спектр та короткий час біологічної дії перешкод-жають використанню цього гормону в медицині.
2) пролактостатин - пептид, який пригнічує секрецію пролактину (існує точка зору, що роль пролактостатину в організмі виконує дофамін).
3) меланостатин - це пептидний гормон, який інгібує синтез і секрецію меланотропіну, має антиопіоїдну дію (існує точка зору, що оскільки за хімічною будовою цей гормон є С-кінцевою частиною окситоцину, то саме окситоцин задіяний в регуляції секреції меланотоніну).
Шляхи інактивації гіпоталамічних гормонів вивчені недостатньо. Одним з них є дія екзо- і ендопептидаз сироватки крові. У гіпоталамусі також знайдений специфічний фермент - піроглутамілпептидаза, яка також каталізує інактивацію тироліберину і гонадоліберину.
5.2 Гормони гіпофіза
5.2.1 Гормони передньої частки гіпофіза (аденогіпофіза) поділя-ють на три групи (сімейства):
І - група гормону росту (СТГ, пролактин, хоріонічний сомато-мамотропін);
ІІ - група тропних гормонів (тиреотропін, лютропін, фоліку-лостимулюючий гормон, хоріонічний гонадотропіни);
ІІІ - похідні ПОМК (АКТГ, ліпотропін, опіоїдні пептиди, меланоцитстимулюючий гормон).
І - група гормону росту
Соматотропний гормон (СТГ, соматотропін, гормон росту) -це пептидний гормон. За хімічною будовою і біологічними властивостями цей гормон схожий з пролактином плацентарним лактогеном і проліферином і тому з’єднаний з ними в одну родину.
СТГ утворюється в соматотропних клітинах аденогіпофіза. Синтез і секреція гормону контролюється двома гіпоталаміч-ними гормонами: соматоліберином (стимулює секрецію) і соматостатином (гальмує секрецію). На секрецію СТГ впливає ряд стимулів таких, як сон, стрес (біль, холод, хірургічне втручання), фізичні вправи, гостра гіпоглікемія або голодування, білкова їжа або амінокислота аргінін.
Протягом декількох хвилин рівень соматотропіну може змінюватися 10 разів. Один з найбільших піків концентрації спостерігається одразу після засинання, що підтверджує прислів’я: “хто не спить, той не росте”.
На вивільнення СТГ впливають такі агенти, як опіатні пептиди, глюкагон, гормони кишечника. Всі ці фактори діють на вентромедіальне ядро гіпоталамусу, який виробляє відповідні рилізинг-фактори.
Секреція СТГ поступово знижується з віком. Вона мінімальна у людей похилого віку, максимальна у підлітків у період інтенсивного лінійного росту та статевого дозрівання.
Соматотропін бере участь в регуляції ліпідного, білкового та вуглеводного обмінів, впливає на мінеральний обмін.
Вплив на обмін білків.
СТГ має потужну анаболічну і антикатаболічну дію - підсилює синтез білка і гальмує його розпад.
Цей ефект забезпечується за рахунок:
1) стимуляції транспорту амінокислот у м’язові клітини;
2) безпосередньої дії на трансляцію;
3) активації синтезу РНК і ДНК.
Для реалізації анаболічної дії СТГ на синтез білка наявність інсуліну є обов’язковою. У разі відсутності інсуліну або при зниженні його концентрації соматотропін не має анаболічного ефекту. СТГ і інсулін є синергістами у процесах регуляції білкового синтезу.
Вплив на обмін вуглеводів.
СТГ - це один з контрінсулярних гормонів, тобто його ефект зв’язаний з підвищенням концентрації глюкози в крові. Підвищення рівня глікемії зв’язане з тим, що соматотропін:
1) знижує утилізацію глюкози периферичними тканинами;
2) стимулює глюконеогенез у печінці (поряд з підсиленням синтезу глікогену).
Вплив на обмін ліпідів.
СТГ активує ліполіз, сприяє зниженню відкладання жиру в адипоцитах та підвищую співвідношення м’язової маси до жирової. У результаті стимуляції ліполізу під дією соматотро-піну в крові підвищується концентрація вільних жирних кислот і стимулюється їх окиснення у печінці. В умовах недостатності інсуліну (наприклад, при діабеті) саме це може сприяти синтезу кетонових тіл (кетогенезу) у печінці.
Вплив на мінеральний обмін.
СТГ активно бере участь у мінеральному обміні: сприяє позитивному балансу кальцію, магнію, фосфатів, викликає затримку Na, K, Cl.
Гормон росту може також зв’язуватися з лактогенними рецепторами і тому має деякі властивості пролактину, а саме здатність стимулювати лактогенез.
Соматомедини.Медіаторами деяких ефектів СТГ є ростові фактори - соматомедини.
Ріст-стимулюючий ефект СТГ опосередковується інсулінпо-дібними факторами росту (ІФР) - гормонами, які утворюються під впливом СТГ у печінці та інших тканинах. Виділені два ІФР: ІФР-1 і ІФР-2. СТГ реалізує свою дію в першу чергу через ІФР-1 - він стимулює синтез цього фактора у печінці, а також в жировій тканині, тимусі.
ІФР-1 регулює секрецію СТГ: він пригнічує секрецію соматоліберину і активує виділення соматостатину.
ІФР діють через рецептори 2 типів, які локалізовані на плазматичній мембрані: 1 тип - має тирозин-кіназну активність, 2-й тип - включає ефекторні системи через G-білки.
Крім того, доведена пряма дія СТГ на тканини, без участі ІФР-1.
Соматотропін має також деяку модулюючу дію на функції ЦНС і проявляє властивості нейропептиду. Відомо, що СТГ покращує пам’ять та пізнавальні функції, особливо у хворих гіпофізарним нанізмом (недостатністю соматотропної функції гіпофіза). Але довготривале використання СТГ як ноотропа неможливе у зв’язку з гормональною активністю цього пептиду. Тому вчені намагаються синтезувати поліпептид, який мав би спорідненість до соматотропних рецепторів ЦНС, але б не діяв на рецептори в периферичних тканинах.
Пролактин (мамотропін, лактогенний гормон)
За структурою (це пептидний гормон) і біологічними властивостями пролактин має загальні риси з гіпофізарним гормоном росту, плацентарним лактогеном і проліферіном та поєднується з ним в окрему родину - родину пролактоподібних білків (або групу гормону росту).
Пролактин синтезується лактотрофами передньої частки гіпофіза у вигляді препролактину. Кількість і розмір цих клітин зростає в період вагітності. Після низки етапів посттрансля-ційної модифікації, гормон в дуже низькій кількості секрету-ється в кров. У нормі концентрація пролактину в сироватці крові не перевищує 15 нг/мл.
Секреція пролактину постійно гальмується гіпоталамічним дофаміном. Підсилюють його секрецію естрогени, тироліберин і нервові імпульси від сосків. Під час вагітності рівень естрогенів постійно зростає і в ІІІ триместрі стає достатньо високим для стимуляції секреції пролактину. Підвищення концентрації пролактину в крові необхідно для підготовки молочних залоз до лактації.
Пролактин - це важливий поліфункціональний гормон, більшість ефектів якого пов’язані з репродуктивною функцією. Він бере участь в ініціації і підтримці лактації, підтримує активність жовтого тіла (подовжує лютеїнову фазу циклу), гальмує овуляцію, знижує секрецію естрогенів фолікулами яєчників та секрецію прогестерону жовтим тілом.
У чоловіків пролактин знижує секрецію тестостерону та пригнічує дозрівання сперматозоїдів.
Крім того відомо, що він впливає на водно-сольовий баланс в організмі та має анаболічну дію.
Також пролактин бере участь в імунологічних процесах - він синтезується не лише гіпофізом, а також лейкоцитами. Секреція пролактину цими клітинами підсилюється в разі активації імунітету, запаленнях, інфекціях.
Хоріонічний соматомамотропін (плацентарний лактоген) - це пептидний гормон, який продукується плацентою під час вагітності. За хімічною будовою він схожий до СТГ і пролактину. Він має соматотропні і пролактоподібні властивості. Встановлено, що лактогенна активність цього гормону вище ніж гіпофізарного пролактину.
Плацентарний лактоген має важливе значення у підготовці молочних залоз до лактації, підтримує роботу жовтого тіла яєчників під час вагітності, сприяє підвищенню секреції жовтим тілом прогестерона.
ІІ - група тропних гормонів
Тиреотропний гормон (ТТГ, тиреотропін).
ТТГ - це глікопротеїн з альфа-бета-димерною структурою, який утворюється в тиреотропних клітинах аденогіпофізу.
Синтез і секреція тиреотропіну контролюється тиролібери-ном. У регуляції цього процесу беруть участь гормони щитовидної залози Т3 (трийодтиронін), Т4 (тироксин). При підвищенні в крові концентрації Т3 і Т4, гальмується секреція ТТГ і тироліберину - реалізується принцип негативного зворотного за’язку регуляції синтезу гормонів.
Подібно до інших гормонів, ТТГ зв’язується з рецепторами плазматичної мембрани, активує аденілатциклазу і через цАМФ стимулює біосинтез тиреоїдних гормонів.
Ефекти, які зв’язані з дією ТТГ на щитовидну залозу, включають стимуляцію всіх стадій біосинтезу Т3 і Т4, у тому числі:
1) концентрування і органіфікацію йоду;
2) конденсацію йодотиронінів;
3) гідроліз тиреоглобуліну.
ТТГ також впливає на периферичні тканини через відповідні рецептори на плазматичних мембранах тканин, підвищує активність селен-залежної монодейодинази (металофермент, який перетворює Т4 в Т3) і чутливість рецепторів тканин до тиреоїдних гормонів. Таким чином тиротропін “готує” тканини до дії Т3 і Т4.
ТТГ викликає в щитовидній залозі більш пролонговані ефекти, для реалізації яких потрібно декілька днів. До них належать підвищення синтезу білків, фосфоліпідів і нуклеїнових кислот, збільшення розмірів і кількості тиреоїдних клітин.
При підвищених концентраціях та тривалій дії ТТГ викликає проліферацію тканини щитоподібної залози, збільшення її розмірів і маси, підвищення кількості колоїдного білка в ній, тобто її функціональну гіпертрофію.
Гонадотропіни
Лютеїнізуючий гормон (лютропін, ЛГ)
Лютропін - це глікопротеїн, який секретується гонадотроп-ними клітинами аденогіпофізу. Продукція цього гормону регулюється гонадоліберином. З початку пубертатного періоду ЛГ (разом з ФСГ) регулює синтез та секрецію статевих гормонів та гаметогенез.
ЛГ стимулює секрецію прогестерону клітинами жовтого тіла та тестостерону клітинами Лейдега.
Лютропін має специфічні рецептори на плазматичній мембрані клітин-“мішеней” і реалізує свою дію через цАМФ. цАМФ активує:
1) перетворення ацетату в сквален (попередник синтезу холестеролу);
2) утворення 2альфа-гідроксихолестеролу із холестеролу (це необхідний етап при синтезі прогестерону і тестостерону).
Синтез ЛГ регулюється за принципом зворотного зв’язку через дію естрогенів. Залежний від естрадіолу пік секреції лютропіну у середині менструального циклу індукує овуляцію у жінок. ЛГ необхідний для підтримки жовтого тіла, яке поряд з естрадіолом починає виробляти прогестерон. У чоловіків ЛГ підвищує утворення тестостерону, який разом з ФСГ стимулює сперматогенез.
Системні ефекти гормону включають розвиток вторинних статевих ознак, розвиток та підтримку простати сім’явиносних протоків та сім’яних міхурців.
У хворих полікістозом яєчників (синдром Штейна-Левен-таля) спостерігається підвищений рівень ЛГ, продукція андроге-нів, зниження фертильності, збільшення маси тіла та підвищений ріст волосся на тілі та лиці.
Фолікулостимулювальний гормон (ФСГ)-це один з трьох гонадотропінів (поряд з ЛГ і хоріонічним гонадотропіном). За хімічною будовою це глікопротеїн, молекула якого складається з двох субодиниць (α і β). Біологічні властивості ФСГ визначаються лише β-субодиницею.
У жінок фолітропін стимулює розвиток фолікулів до моменту овуляції і інтестинальної тканини яєчників, що призводить до підсилення секреції жіночих статевих гормонів - естрогенів.
У чоловіків ФСГ стимулює розвиток сім’яних канальців, підсилює сперматогенез і секрецію чоловічих статевих гормонів - андрогенів.
Свою дію ФСГ реалізує разом з ЛГ і поряд з цим підвищує чутливість статевих залоз до лютропіну. Регуляція синтезу і секреції ФСГ здійснюється під впливом відповідного рилізинг-гормону гіпоталамусу - фоліберину. Крім того концентрація ФСГ залежить від вмісту в крові андрогенів і естрогенів (при підвищенні їх концентрації секреція ФСГ знижується - реалізується принцип негативного зворотного зв’язку). Синтез ФСГ інгібується також специфічним білковим гормоном статевих залоз - інгібіном.
Хоріонічний гонадотропін (гонадотропний гормон плаценти) - це глікопротеїн, який складається з двох субодиниць. Він має активність як лютропіну, так і фолікулостимулювального гормону. Але ж перша його активність переважає над другою. Крім того лютеїнізуюча активність цього гормону набагато вища ніж у “звичайного” лютропіну гіпофіза.
У невагітних жінок хоріонічний гонадотропін відсутній. Але він може продукуватися різними злоякісними пухлинами.
Хоріонічний гонадотропін:
1) відповідає за функціонування жовтого тіла в період вагітності;
2) стимулює секрецію значної кількості прогестерона жовтим тілом;
3) стимулює продукцію естрогенів фолікулярним апаратом яєчників;
4) підвищує секрецію глюкокортикоїдів (що є важливим механізмом адаптації вагітних до стресу;
5) підтримує функціонування плаценти.
При введенні цього гормону, в організмі людини стимулюється овуляція у жінок і сперматогенез у чоловіків, підсилюється розвиток статевих органів і вторинних статевих ознак.
Фармацевтична промисловість випускає значну кількість препаратів, що містять хоріонічний гонадотропін; ці препарати використовують у медицині при зниженій функції статевих залоз у чоловіків і жінок, які обумовлені порушенням функціонування гіпоталамуса і гіпофіза. Але використання цих препаратів у значних дозах може призвести до порушень функціонування статевих органів у чоловіків і жінок.
В онкології визначення хор іонічного гонадотропіни в сироватці крові використовують для діагностики хоріокарціономії (наявний в 100% випадків), ембріональної карциономії (60%), злоякісних пухлинах товстого і прямого кишечника та деяких інших.
ІІІ - похідні ПОМК
АКТГ (адренокортикотропний гормон, кортикотропін)-гіпофізарний гормон, який утворюється в результаті процесингу білка попередника - ПОМК (проопіомеланокортину), який є попередником для деяких інших пептидних гормонів гіпофізу. Синтез АКТГ в кортикотропінових клітинах аденогіпофізу та секреція АКТГ контролюється кортиколіберином (кортикотро-пін-рилізинг фактором - CRF).
Кортикотропін стимулює синтез і секрецію гормонів кори наднирників - глюкокортикоїдів (кортизолу, кортизону, корти-костерону), при цьому спостерігається незначна стимуляція синтезу прогестерону, андрогенів і естрогенів. У деякій мірі кортикотропін стимулює секрецію мінералокортикоїдів і катехоламінів, але для названих гормонів цей механізм регуляції секреції не є основним.
Дія АКТГ на кору наднирників може носити довготривалий (хронічний) та короткотривалий характер.
При довготривалому впливі АКТГ на наднирники в них підсилюється кровоток, стимулюється синтез білків, робота ферментів стероїдогенезу, відбувається ріст залози. При великих концентраціях АКТГ відбувається ріст залози, при дефіциті - зменшення і атрофія.
Короткотривалий ефект АКТГ на кору наднирників зв’язаний з секрецією кортизолу, а саме гормон стимулює:
1 Захоплення ліпопротеїнів низької щільності.
2 Гідролізу ефірів холестеролу, які депонуються в корі наднирників, та підвищення кількості вільного холестеролу.
3 Транспорту холестеролу в мітохондрії.
4 Зв’язування холестеролу з ферментами та перетворення його в прегненолон.
Кортикотропін також діє на периферичні тканини.
1 Підвищує чутливість тканини до дії гормонів кори наднирників (глюкокортикоїдів та мінералокортикоїдів).
2 Активує ліполіз в жировій тканині шляхом дії безпосередньо на аденілатциклазу адипоцитів.
Встановлено, що АКТГ та його фрагменти впливають на мотивацію, пам’ять, процеси навчання.
Ліпотропін (β- та γ-)
Ліпотропні гормони утворюються в результаті розщеплення попередника - ПОМК (проопіомеланокортину).
β-Ліпотропін утворюється в кортикотропах передньої частки гіпофіза: при стимуляції кортикотропін-рилізинг-гормоном синтезуються ендопептидази, які розщеплюють ПОМК.
γ-Ліпотропін утворюється в меланотропах середньої частки гіпофізу: при стимуляції дофаміном активується синтез відповідних ендопептидаз, які гідролізують ПОМК.
Біологічна роль β- та γ-ліпотропінів полягає в тому, що вони підсилюють ліполіз в адипоцитах, зменшують синтез та відкладення триацилгліцеролів.
Меланоцитстимулювальний гормон (меланотропін, МСГ)
Виділяють три типи МСГ (α-, β-, γ-), які утворюються при частковому протеолізі ПОМК.
Гормон стимулює розмноження меланоцитів шкіри та підсилює синтез меланоцитами чорного пігменту - меланіну. Саме тому γ-МСГ підсилює пігментацію шкіри, підвищує стійкість шкіри до ультрафіолетового випромінювання.
α- і β-МСГ мають високу ліпотропну активність (стиму-люють ліполіз в жировій тканині). α-МСГ також бере участь в терморегуляції і має незначну стероїдогенну активність.
Опіоїдні пептиди
Це група природних пептидів, які за дією схожі до опіатів (морфін, кодеїн та інші) і зв’язуються з опіатними рецепторами організму. Існує декілька структурних родин цих сполук, які містять енкефаліни та ендорфіни, а також менш відомі - групи динорфіну.
Ці пептиди мають широкий спектр регуляторної активності та знайдені в різних тканинах - як в мозку, так і в периферичних тканинах (статевих залозах, кишечнику та інш.). Вони діють як нейротрансмітери та/або нейромедіатори.
Більшість опіоїдів утворюються з білкових попередників (проопіомеланокортину, продинорфіну та проенкефаліну) в результаті часткового протеолізу цих молекул.
Регуляторний вплив опіоїдних пептидів здійснюється, як правило, за участі інших пептидів і низькомолекулярних субстанцій (ГАМК, глютамат, ацетилхолін, дофамін).
Ці пептиди діють на клітини через систему фосфоліпази С.
Фізіологічні функції цих пептидів:
1) знеболювальна дія;
2) протишоковий ефект;
3) антистресова дія;
4) пригнічення функцій гіпоталамо-гіпофізарно-гонадної осі на всіх рівнях;
5) зниження апетиту;
6) зниження тонусу симпатичної нервової системи;
7) гальмування секреторної активності та перистальтики ШКТ;
8) мотивація задоволення.
Одним з найважливіших енкефалінів є мет-енкефалін, який утворюється тільки у жінок (в процесі шопінгу, сексу, поїдання шоколаду), має також анальгезивний ефект.
Менш відомі опіоїдні пептиди - це: динорфін та споріднені пептиди, які беруть участь в регуляції артеріального тиску, генералізованих та локальних нейрогенних процесах; визна-чають спадкову схильність до алкоголізму.
5.2.2 Гормони задньої частки гіпофіза (гормони нейрогіпофізу)
Нейрогіпофізарні гормони утворюються в гіпоталамусі, транспортуються по аксону в комплексі з специфічним білком - нейрофезіном у задню частку гіпофізу (нейрогіпофіз), де депонується та секретується у кров.
Нейрогіпофізарні гормони - це вазопресин і окситоцин.
Вазопресин (антидіуретичний гормон, АДГ) -це пептидний гормон, серед великої кількості ефектів якого виділяють два основні:
- контроль водного балансу в організмі (антидіуретична дія);
- підтримка артеріального тиску (сильна вазоконстрикторна дія).
Вазопресин (та його аналоги також) беруть участь у процесах навчання та пам’яті.
Антидіуретична дія - найважливіша функція АДГ. Основною “мішенню” АДГ є клітини дистальних канальців і збірних трубочок нирок. У мембрані цих клітин є рецептори, які спряжені з аденілатциклазою.
Приєднання АДГ до рецепторів активує аденілатциклазу і цАМФ, який утворюється, стимулює збільшення кількості каналів для води в мембранах канальців і трубочок. Це забезпечує пасивну реабсорбцію Н2О.
Основним стимулом для секреції АДГ є підвищення осмолярності позаклітинної рідини. Оскільки основним катіоном цієї рідини є Na, осмолярність позаклітинної рідини визначається головним чином його концентрацією.
Регуляція секреції АДГ зв’язана з функціонуванням ренін-ангіотензинової системи. При гіповолемії (зменшення об’єму крові в організмі, яке виникає внаслідок втрати Nа і Н2О) відбувається стимуляція ренін-ангіотензинової системи, утворення ангіотензину ІІ, який у свою чергу стимулює секрецію АДГ. Крім того стимуляторами секреції АДГ є простагландин Е2, нікотин, барбітурати, гістамін, ацетилхолін тощо. Інгібують секрецію АДГ передсердний натрійуретичний гормон, алкоголь тощо.
У разі відсутності АДГ кількість водневих каналів знижена і епітелій практично немає проникливості до Н2О, тому з організму виводиться велика кількість гіпотонічної сечі.
Порушення секреції або дії АДГ призводить до розвитку нецукрового діабету, який характеризується виділенням великого об’єму розведеної сечі - гіпотонічна поліурія. Діагностичні критерії нецукрового діабету:
- кількість сечі більш ніж 30 мл/кг/добу;
- осмолярність менш ніж 300 мосм/кг;
- питома вага менш ніж 1,010.
Окситоцин -це потужний гормон, який утворюється в передніх ядрах гіпоталамуса, депонується в нейрогіпофізі, куди траспортується за допомогою специфічного білка - переносника нейрофізину.
Цей гормон виконує в організмі функції, які зв’язані з пологами та лактацією. Він стимулює скорочення міометрію матки та міоепітеліальних клітин молочної залози. Окситоцин стимулює також секрецію пролактину. Цей пептид має відношення до фіксації пам’яті; разом з калікреїн-кініновою системою бере участь в регуляції натрійурезу (має слабкий вазопресиноподібний антидіуретичний ефект).
Знайдений вплив окситоцину на психоемоційну сферу чоловіків і жінок. Він викликає більш доброзичливе відношення з іншими людьми, дозволяє вірити словам конкретної людини. Крім того, він здатний заспокоювати чоловіків і жінок під час сварок (через зниження рівня гормону стресу кортизолу).
6.1 Гормони щитоподібної залози
У щитоподібній залозі синтезуються:
1) тиреоїдні гормони (Т4 - тироксин, Т3 - трийодтиронін)
2) кальцитонін (який буде розглянутий в розділі з регуляції кальцій-фосфорного обміну)
Тиреоїдні гормони - це похідні амінокислоти тирозину (Тир). Конденсація двох молекул Тир призводить до утворення L-тироніну, який є попередником в синтезі Т3 (трийодтироніну) і Т4 (тироксину):



Тиронін L-тироксин L-трийодтиронін
(3, 5, 3′, 5′ - (3, 5, 3′ - трийодтиронін),
тетрайодтиронін), Т4 Т3
Показано, що найбільшу біологічну активність має 3, 5, 3′ - трийодтиронін - Т3. Вважають, що Т3 - це не лише гормон, який секретується, але й є активною формою Т4 у периферичних тканинах.
Синтез тиреоїдних гормонів
Клітини фолікулярного епітелію постійно синтезують колоїдний білок - тиреоглобулін (глікопротеїн). Для синтезу Т3 і Т4 потрібен йод, який в формі І- всмоктується в шлунку і кишечнику. Тиреоцити захоплюють йод з плазми крові і концентрують його. За добу залоза поглинає ≈ 120 мкг йоду. Не менше як 80 мкг йоду використовується за добу на синтез тиреоїдних гормонів. На наступному етапі йод із іонної форми переводиться в зв’язану з тиреоглобуліном форму. Цей процес каталізує фермент тиреоїдна пероксидаза. Під дією цього ферменту йод зв’язується з залишками тирозину в тиреоглобуліні. Кожний четвертий залишок Тир йодується. Утворюються моно- і дийодтирозини (МИТ і ДИТ).
На наступному етапі відбувається конденсація йодтирозино-вих залишків - утворюються Т3 і Т4, які знаходяться в структурі колоїдного білка. Т4 є результатом конденсації двох залишків ДИТ, Т3 - МИТ і ДИТ.
Після секреції в кров, більша частина гормонів зв’язується з транспортним білком - тироксин-зв’язуючим глобуліном (фракція α-глобулінів). Він зв’язує 75% Т4 і 80% Т3. Приблизно 15% Т4 зв’язується з іншим транспортним білком крові - транстиретином (фракція преальбумінів). Біля 10% Т4 зв’язано з альбуміном.
У зв’язаному вигляді ці гормони неактивні.
Лише 0,02% Т4 і 0,3% Т3 залишаються вільними - це активна фракція гормонів. Вільні гормони Т3 і Т4 досягають клітин-“мішеней” і діють на рецептори. Т4 в клітинах повністю перетворюється в Т3.
Вважають, що деякі ефекти тиреоїдних гормонів зумовлені їх дією на рецептори плазматичної мембрани (стимуляція транспорту амінокислот, активація К+-Na+-АТФ-ази). Доведена наявність мітохондріальних рецепторів до Т3 і Т4. Але найбільш важливими є ядерні рецептори, які сприймають виключно Т3.
Рецептори до тиреоїдних гормонів присутні практично в усіх клітинах організму (найменша чутливість до тиреоїдних гормонів у спленоцитів і сім’яників.
Катаболізм тиреоїдних гормонів відбувається в основному в печінці. Т3 і Т4 перетворюються в МИТ і ДИТ, які потім дейодуються під дією дейодиназ. Йод, який вивільняється знову може використовуватися щитовидною залозою.
Біохімічні ефекти тиреоїдних гормонів
У фізіологічних дозах тиреоїдні гормони є анаболічними. У токсичних дозах - катаболічними.
Тиреоїдні гормони мають такі біохімічні ефекти:
1 Підсилюють поглинання амінокислот, глюкози, калію і виведення натрію, кальцію, фосфору.
2 Стимулюють синтез білка за рахунок активації аміноацил-тРНК-синтетазної, пептидилсинтетазної і транслоказної реакцій.
3 Підсилюють аеробне окиснення (в токсич
Читайте також:
- Аденогіпофіз, його гормони, механізм впливу
- Аденогіпофіз, його гормони, механізм впливу, прояви гіпер- та гіпофункцій.
- Біологічне значення залоз внутрішньої секреції
- Будова і функції ендокринних залоз
- ВИЛОЧКОВА ЗАЛОЗА
- Вилочкова залоза.
- Гормони статевих залоз
- Гормони шлунковокишкового тракту
- Досі фахівці не прийшли до загальної думки про те, чи вважати гіпертрофію передміхурової залози патологічним процесом або нормальним фізіологічним явищем.
- Ендокринна функція підшлункової залози
- ЕНДОКРИННА ЧАСТИНА ПІДШЛУНКОВОЇ ЗАЛОЗИ
| <== попередня сторінка | | | наступна сторінка ==> |
| Федеральне казначейство Російської федерації | | | Глюкагон |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |