
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
КЛАСИ НЕОРГАНІЧНИХ СПОЛУК
1.1 Перелічіть стійкі ступені окислення елементу:
01 – Нітроген; 02 – Магній; 03 – Натрій; 04 – Хлор; 05 – Сульфур; 06 – Титан; 07 –Карбон; 08 – Цинк; 09 – Купрум; 10 – Манган; 11 – Хром; 12 – Бром; 13 – Кальцій; 14 – Алюміній; 15 – Калій; 16 – Аргентум; 17 – Барій; 18 – Силіцій; 19 – Кадмій; 20 – Літій; 21 – Нікол;
22 - Гідроген; 23 – Літій; 24 – Станум; 25 – Фосфор; 26 – Стибій; 27 – Бор; 28 – Ферум;
29 - Меркурій ; 30 – Іод.

1.2. Складіть емпіричні та графічні формули можливих оксидів елементу, вказаного у розділі 1.1, і назвіть ці оксиди.
1.3. Визначте тип оксидів (солетворний, несолетворний, основний, кислотний або амфотерний), вказаних у розділі 1.2.
1.4. Напишіть рівняння реакцій солеутворення, що доводять характер оксидів (основний, кислотний або амфотерний), визначений у розділі 1.3.
1.5. Напишіть емпіричні, графічні формули та назву гідроксидів оксидів, складених за розділом 1.2.
1.6. Дайте назву сполук за міжнародною номенклатурою:
01-  ; 02-
; 02- 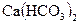 ; 03-
; 03- 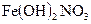 ; 04-
; 04-  ; 05 -
; 05 - 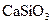 ; 06 -
; 06 -  ; 07 -
; 07 -  ; 08 -
; 08 -  ; 09 -
; 09 - 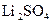 ; 10 -
; 10 -  ; 11 -
; 11 -  ; 12 -
; 12 -  ; 13 -
; 13 - 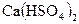 ; 14 -
; 14 - 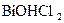 ; 15 -
; 15 -  ; 16 -
; 16 -  ; 17 -
; 17 - 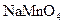 ; 18 -
; 18 -  ; 19 -
; 19 - 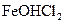 ; 20 -
; 20 -  ; 21 -
; 21 - 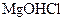 ; 22 -
; 22 - 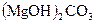 ; 23 -
; 23 - 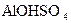 ; 24 -
; 24 -  ; 25 -
; 25 - 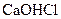 ; 26 -
; 26 - 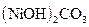 ; 27 -
; 27 -  ; 28 -
; 28 - 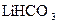 ; 29 -
; 29 - 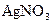 ; 30 -
; 30 - 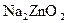 .
.
1.7. Визначте ступінь окислення елементів, утворюючих сполуки, зазначені у розділі 1.6.
1.8. Напишіть емпіричну та графічну формули кислоти:
01 – борної; 02 – карбонатної; 03 – нітритної; 04 – фосфатної; 05 – сульфатної; 06 – нітратної; 07 – сульфідної; 08 – оцтової; 09 – силікатної; 10 – сульфітної; 11 – хлоридної; 12 – нітратної; 13 – фосфатної; 14 – силікатної; 15 – карбонатної; 16 – бромводневої; 17 – фтороводневої; 18 – хромової; 19 – борної; 20 – манганової; 21 – сульфатної; 22 – фосфатної; 23 – бромоводневої; 24 – сульфітної; 25 – нітритної; 26 – йодоводневої; 27 – хромової; 28 – нітратної; 29 – оцтової; 30 – манганової.
1.9. Напишіть емпіричну та графічну формули основи:
01 – нікол (ІІІ) гідроксид; 02 – кальцій гідроксид; 03 – ферум (ІІІ) гідроксид; 04 – стронцій гідроксид; 05 – натрій гідроксид; 06 – ферум (ІІ) гідроксид; 07 – бісмут (ІІІ) гідроксид; 08 – купрум (І) гідроксид; 09 – нікол (ІІІ) гідроксид; 10 – кобальт (ІІІ) гідроксид; 11 – калій гідроксид; 12 – цезій гідроксид; 13 – барій гідроксид; 14 – кадмій гідроксид; 15 – магній гідроксид; 16 – манган (ІІ) гідроксид; 17 – францій гідроксид; 18 – купрум (ІІ) гідроксид; 19 – бісмут (ІІІ) гідроксид; 20 – нікол (ІІІ) гідроксид; 21- меркурій (ІІ) гідроксид; 22 – літій гідроксид; 23 – барій гідроксид; 24 – радій гідроксид; 25 – цирконій (ІІІ) гідроксид; 26 – купрум (ІІ) гідроксид; 27 – хром (ІІ) гідроксид; 28 – ітрій (ІІІ) гідроксид; 29 – рубідій гідроксид; 30 – талій (ІІІ) гідроксид.
1.10. Напишіть емпіричну та графічну формули солі:
01 – літій нітрат; 02 – кальцій карбонат; 03 – калій сульфат; 04 – натрій нітрат; 05 – цинк сульфіт; 06 – літій хлорид; 07 – натрій силікат; 08 – берилій фторид; 09 – барій сульфід;
10 – натрій дихромат; 11 – магній гідрогенсульфід; 12 – кальцій дигідрогенфосфат; 13 – ферум (ІІІ) гідрогенсульфат; 14 – алюміній гідроксосульфат; 15 – хром (ІІІ) дигідроксонітрат; 16 – калій цинкат; 17 – алюміній дигідрогенфосфат; 18 – стронцій дихромат; 19 – алюміній дигідроксосульфат; 20 - калій гідрогенкарбонат; 21 - ферум (ІІІ) гідроксохлорид; 22 - кальцій гідрогенфосфат; 23 – алюміній дигідроксохлорид; 24 - натрій гідрогенфосфат; 25 – кадмій карбонат; 26 - стронцій гідрогенсульфат; 27 - меркурій (ІІ) нітрат; 28 – барій хлорид; 29 – станум (ІІ) сульфат; 30 - аргентум хромат.
Читайте також:
- II. Класифікація видатків та кредитування бюджету.
- V. Класифікація і внесення поправок
- V. Класифікація рахунків
- VIII. Реакції, в результаті яких утворюються високомолекулярні сполуки
- А .Маршалл - основоположник неокласичної теорії.
- А. Структурно-функціональна класифікація нирок залежно від ступеню злиття окремих нирочок у компактний орган.
- Абстрактні класи
- Адміністративні провадження: поняття, класифікація, стадії
- Азоновмістні органічні сполуки.
- Азосполуки
- Азот, фосфор, біогенні елементи та їх сполуки, органічні речовини
- Аналітичні процедури внутрішнього аудиту та їх класифікація.
| <== попередня сторінка | | | наступна сторінка ==> |
| | | ОСНОВНІ ПОНЯТТЯ ТА ЗАКОНИ ХІМІЇ |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |