
МАРК РЕГНЕРУС ДОСЛІДЖЕННЯ: Наскільки відрізняються діти, які виросли в одностатевих союзах
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
Контакти
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Для виділення 1 кг речовини, потрібно пропустити через електроліт одну й ту ж кількість електрики, її позначають буквою F і називають числом Фарадея.
F = 9,65 × 104 Кл
Електрохімічний еквівалент визначають по формулі:
К = (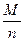 ) × (
) × (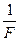 ) =
) = 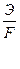
Гальванічний елемент є хімічне джерело постійного струму, його схема:
електрод ½½ р – р ½½ р – р ½½ ½ електрод ½½
Е1 Едиф Е2
Різниця потенціалів між електродом і розчином називається електродним потенціалом, а між двома різними розчинами – дифузійним потенціалом Е.Р.С. визначається різницею між електродним потенціалом.
Потенціал електрода в розчині солі того ж металу з активністю іонів від Ме+n, обчислюється по формулі:
для 25 оС ЕМе/Меn+ = EoMe/Меn+ + (0,095 / ne) × lg a Men+
при 25 оС Е = Е¢о - Е¢¢о = (0,059 / ne) lg (a1 / a2)
при 18 оС Е = Е¢о + Е¢¢о = (0,058 / ne) lg (a1 / a2)
де, Е¢о і Е¢¢о – нормальні потенціали електродів (знаходяться по таблиці ряду напруг);
a1 і a2 – активності іонів у розчинах, якщо ne1 = ne2 = ne.
При розрахунках ЕДС від більшого потенціалу розраховують менший, тобто у всіх випадках Е > 0.
Читайте також:
- I. Органи і системи, що забезпечують функцію виділення
- III. За виділенням або поглинанням енергії
- Ni - загальна кількість періодів, протягом яких діє процентна ставка ri.
- VII. Філо- та онтогенез органів виділення
- Адсорбція електролітів
- Адсорбція електролітів
- Акустичний контроль приміщень через засоби телефонного зв'язку
- Алкени – вуглеводні, в молекулах яких є один подвійний зв’язок між атомами вуглецю . Алкені називають також олефінами або етиленовими вуглеводнями.
- Алкіни – вуглеводні, в молекулах яких є два атоми вуглецю, сполучені потрійним зв’язком - -. Алкіни називають також ацетиленовими вуглеводнями.
- АЛЬТЕРНАТИВНІ ПІДХОДИ ДО ВИДІЛЕННЯ МЕТОДІВ УПРАВЛІННЯ
- Аналіз ризику через моделювання.
- Антропогенез – процес виділення людини з тваринного святу, олюднення мавпи під впливом суспільної практики.
| <== попередня сторінка | | | наступна сторінка ==> |
| Потенціометричні визначення концентрації водневих розчинів. | | | Вступ, загальна характеристика, класифікація. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |