
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Молекулярне - кінетичні властивості колоїдних систем
Лекція № 19
Тема:Молекулярно - кінетичні властивості дисперсних систем.
Мета:Знати: рівняння Ейнштейна-Смолуховського, яке пояснює основні молекулярно - кінетичні властивості, процеси дифузії і від яких факторів ці процеси залежать, закон Вант-Гоффа і вміти його порівнювати для істинних розчинів.
Молекулярне - кінетичні властивості зумовлені тепловим рухом частинок. До таких властивостей відносяться: дифузія, осмотичний тиск, розподіл частинок по висоті (гіпосиметричне розподілення).
В колоїдних системах молекулярне - кінетичні властивості визначаються рухом частинок дисперсної фази - броунівським рухом, яке було відкрите 1827 році англійським ботаніком Робертом Броуном .
Рівняння кількісної оцінки броунівського руху:
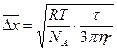
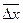 - середній квадратичний здвиг частинки за одиницю часу;
- середній квадратичний здвиг частинки за одиницю часу;
t - час;
NA – число Авогадро;
h - в’язкість дисперсного середовища;
r - радіус частинки дисперсної фази.
Рівняння Ейнштейна – Смолуховського неодноразово перевірялось і його правильність була доказана експериментально і підвердило реальне існування молекул.
Броунівський рух є причиною дифузії частинок в колоїдних системах. Дифузія - самодовільне вирівнювання концентрацій, спостерігається в будь-яких дисперсних системах, частинки яких знаходяться в русі. Швидкість дифузії пропорційна різності концентрацій і температури, обернено пропорційна в'язкості дисперсного середовища та розміру дифундуючи частинок. Колоїдні системи мають осмотичний тиск. За законом Вант-Гоффа осмотичний тиск розчинів неелектролітів визначається:
П = m0 / М∙ RT
де: m0 - вага речовини, розчиненої у 1 літрі розчину, яку можна уявити m0= mV
m - вага однієї частинки
М - вага одного моля розчиненої речовини
Вагу одного моля розчиненої речовини можливо виразити через постійну Авогадро: М = m × Na, тоді рівняння має вигляд:
П = n∙RT / Na
Відповідно осмотичний тиск залежить тільки від числа частинок в одиниці об'єму розчину та не залежить від природи та розміру частинок. При однаковій ваговій концентрації часткова концентрація колоїдних розчинів завжди менше, ніж у істинних розчинів, тому і осмотичний тиск колоїдних розчинів повинен бути дуже невеликим.
Для двухколоїдних розчинів з однаковою масовою концентрацією рівняння буде мати вигляд:
П1/П2 = n1/n2
Для колоїдних систем характерна агрегація (або дезагрегація) частинок, внаслідок чого розмір їх збільшується (або зменшується), відповідно змінюється осмотичний тиск. Можна зробити висновок, що осмотичний тиск в колоїдних системах завжди буде менше ніж в істинних розчинах.
Читайте також:
- Active-HDL як сучасна система автоматизованого проектування ВІС.
- I. Органи і системи, що забезпечують функцію виділення
- I. Особливості аферентних і еферентних шляхів вегетативного і соматичного відділів нервової системи
- II. Анатомічний склад лімфатичної системи
- II. Бреттон-Вудська система (створена в 1944 р.)
- III етап. Системний підхід
- IV. Розподіл нервової системи
- IV. Система зв’язків всередині центральної нервової системи
- IV. УЗАГАЛЬНЕННЯ І СИСТЕМАТИЗАЦІЯ ВИВЧЕНОГО
- IV. Філогенез кровоносної системи
- OSI - Базова Еталонна модель взаємодії відкритих систем
- POS-системи
| <== попередня сторінка | | | наступна сторінка ==> |
| Електрофорез та електроосмос, їх практичне застосування. | | | Лекція № 21 |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |