
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
ЗАГАЛЬНІ ВІДОМОСТІ
Амперометричне титрування є титриметричним методом аналізу, в якому для індикації точки еквівалентності використовують струм, що виникає в ланцюзі за рахунок розряду іонів, які беруть участь у титруванні (визначуваного компонента, надлишку титранта) або продуктів їх взаємодії. Амперометричне титрування являє собою модифікацію полярографічного методу аналізу, заснованого на пропорційності дифузійного граничного струму від концентрації речовини, що приймає участь в електродній реакції і що обумовлює зміни граничного дифузійного струму, який і є аналітичним сигналом у розглянутому методі аналізу.
Безпосередній зв'язок між амперометричним титруванням і полярографічним методом краще за все проілюструвати наступним прикладом. Для ряду розчинів солі Мору, (NH4)2Fe(SO4)2, з різною концентрацією зняті вольтамперні криві (рис. 1.1). Залізо (II) окиснюється на Pt мікроелектроді. На кривих фіксуються полярографічні хвилі. Чим більше концентрація Fe2+ у вихідному розчині, тим вище граничний дифузійний струм. Для амперометричних титрувань заліза (II) біхроматом калію:

на електроди накладається напруга, відповідна положенню цих площадок щодо осі абсцис (Е), наприклад +1 В (див. рис. 1.1) і відтитровують розчин з максимальним вмістом Fe2+ розчином біхромату калію. При додаванні титранту концентрація заліза (II) і сила дифузійного струму симбатно зменшуються (рис. 1.2). У кінцевій точці титрування встановлюється постійний залишковий струм, величина якого надалі практично не змінюється.
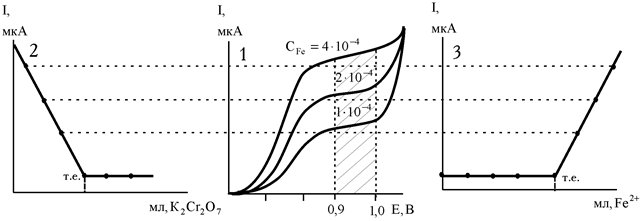
Рис. 1.1. Графічне зображення зв'язку між полярограмами (вольтамперними кривими) (1) і кривими амперометричного титрування (2, 3)
У випадку титрування K2Cr2O7 розчином солі Мору при такій же напрузі, титрант (Fe2+) витрачається на хімічну реакцію і сила струму, поки в розчині є біхромати-іони, не змінюється (рис. 1.3). Після точки еквівалентності з'явиться надлишок заліза і струм різко зросте. Підйом струму, що спостерігається після точки еквівалентності, пропорційний кількості надлишку титранту. За витраті стандартного розчину титранту (перетинанням двох прямих) знаходять графічним методом точку еквівалентності і розраховують масу визначуваної речовини або її масову частку, використовуючи знайомі для титриметрії розрахункові формули:

Можливості амперометричного титрування значно ширші, ніж полярографічного аналізу. У полярографії електродну реакцію повинний давати визначуваний іон. У той час як в амперометрії електрохімічно активними можуть бути не тільки визначуваний компонент, але і розчин, яким титрують, або продукт хімічної реакції, що виділяється. Ширше і діапазон визначаємих концентрацій.
Так само як і в полярографії при амперометричному титруванні використовують мікро- і макроелектроди. При анодній поляризації як мікроелектроди частіше застосовують Pt, рідше графіт, срібло або золото. У випадку катодної поляризації – ртутно-крапельний або амальгамований електроди. Макроелектродом слугує каломельний або хлоросрібний електрод. Робочі електролітичні комірки мають вигляд:
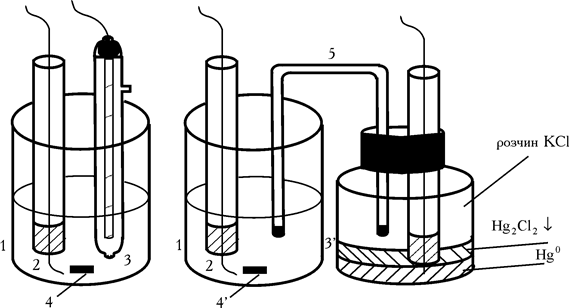
Рис. 1.2. Електролітичні комірки з одним індикаторним електродом: 1 – стаканчик для титрування; 2 – платиновий мікроелектрод; 3 і 3’ – макроелектроди хлоросрібний і каломельний відповідно; 4 – мішалка; 5 – електролітичний ключ
Для виконання аналізу амперометричним методом необхідне виконання наступних двох основних умов:
1. У розчині кількісно, швидко і селективно повинна проходити хімічна реакція. Запишемо її в загальному вигляді таким чином:

2. Один з компонентів (А, В або С) повинний бути електрохімічно активним. Тобто при напрузі, що накладається, іони (молекули) А, В або С повинні давати електродну реакцію. Вони повинні окиснюватися або відновлюватися на мікроелектроді.
Для проведення аналізу звичайно спочатку знімають вольтамперні криві А, В та С, якщо електрохімічні властивості їх невідомі або не дані в прописах. Для цього в розчини перерахованих речовин опускають електроди, і змінюючи напругу, що накладається, від 0 до +1,2 В (відн. НКЕ) або до – 1,0 В, записують виникаючу силу струму в ланцюзі. Вибирають напругу, що відповідає середині інтервалу значень Е, площадки граничного дифузійного струму (рис.1.1). Накладають цю напругу на електроди. Занурюють електроди в аналізований розчин і проводять титрування, записуючи силу струму після кожного додавання титранту (по 0,1–0,2 мл). Титрування закінчують після різкої зміни струму (рис.1.2) або, якщо ця зміна почалася з початку титрування, то після встановлення значень, що не змінюються. (рис. 1.3).
Амперометричне титрування проводять на приладах АУ-4М, БАН-УНІІЗ і звичайних полярографах. Іноді для аналізу застосовують установки, зібрані безпосередньо в лабораторіях. Схема такої установки надана на рис.3.
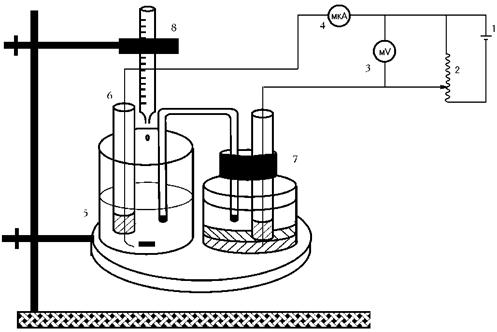
Рис. 3. Схема амперометричної установки: 1 – джерело постійного струму – батарейка;
2 – дільник напруги; 3 – мілівольтметр; 4 – мікроамперметр; 5 – електролітична комірка;
6 – обертовий платиновий мікроелектрод; 7 – каломельний електрод; 8 – мікробюретка для титрування
Для виготовлення платинового мікроелектрода Pt дріт впаюють у скляну трубку, в яку для контакту насипають графіт і занурюють звичайний дріт-провідник, який і підключають у ланцюг.
За допомогою амперометричного титрування можуть бути визначені практично всі елементи періодичної системи Д.І. Менделєєва. Останнє наочно проілюстроване складеними рядами катіонів і аніонів, що розташовані в порядку відповідним періодичним групам таблиці:
I. AuCl4– і AuCl2–, Ag+, Cu2+ і Cu+, K+, Na+, Li+;
II. Be2+, Ba2+, Ca2+, Mg2+ Cd2+, Zn2+, Hg2+ і Hg22+;
III. Al3+, In3+, Ga3+, Tl3+ і Tl+, Y3+, Sc3+, B(H3BO3), Ce4+ і ін. латаноїди, актиноїди – уран, торій, плутоній;
IV. Pb2+, SnCl62– і SnCl42–, германій, цирконій, гафній, Si (SiО32–, кремніймолібденові і кремнійвольфрамові кислоти);
V. V (VO3–, VO2+, V3+), Bi3+, Sb (SbCl6– і SbCl4–), As (AsО43– і AsО33–), Nb і Ta (Me(C2O4)n–m); P(PO43–), N2(NH3, NO2–, NO3–, H4N2 та ін.);
VI. Mo (MoО42–, MnО22+, MoIII), W (WO42–), Cr (Cr2O72–, Cr3+), O2 (OH–, озон, Н2О2); Se і Te (VI і IV); S (S2–, SO32–, S2O32–, CNS–, полісульфіди);
VII. F–, Cl–, Br–, I–, Mn (MnО4–, Mn2+, Mn3+Ln–, Mn2+), Tc і Re (MeО4–);
VIII. Fe3+ і Fe2+, Ni3+ і Ni2+, Co3+ і Co2+, PdCl42–, JrCl62–, PtCl42–, Os і Ru (VI, IV, III), Rh (III і V).
Згідно з наведеними даними за допомогою амперометричного титрування можливе і визначення елементів різного ступеня окиснювання.
Металоїди (неметали) при розкритті наважок в основному переводять у кисневмісні аніони.
Амперометричним титруванням можна також визначати багато органічних сполук. Вибір титранту носить індивідуальний характер. Часто зустрічаються нітрати срібла і ртуті, сульфати міді, кадмію і церію, біхромат калію, бромат-бромідна і йодат-йодидна суміші, K3Fe(CN)6, солі хрому (II), гідроксиламін та ін.
Дані за аналізом органічних сполук, амперометричним титруванням надані в табл.1.1
Як видно з наведених даних визначення можливе для сполук різних класів: альдегідів, кетонів, спиртів, кислот, амідів і амінів, насичених, ненасичених і ароматичних вуглеводнів, білків, алкалоїдів та інших сполук.
Таблиця 1.1
Читайте також:
- D - порушення стану свідомості (Disability).
- I. Загальні збори АТ
- I. ЗАГАЛЬНІ МЕТОДИЧНІ ВКАЗІВКИ
- I. Загальні положення
- I. Загальні положення
- I. ЗАГАЛЬНІ ПРАВИЛА.
- II. Загальні вимоги до розробки екскурсії
- II. ЗАГАЛЬНІ ПОЛОЖЕННЯ.
- IV. Загальні висновки
- IV. ЗАГАЛЬНІ ПОНЯТТЯ ПРО ПЕРШУ МЕДИЧНУ ДОПОМОГУ ПОТЕРПІЛИМ.
- IV. Загальні рекомендації щодо безаварійної та безпечної експлуатації сільськогосподарської техніки вітчизняного та зарубіжного виробництва
- IX. Відомості про військовий облік
| <== попередня сторінка | | | наступна сторінка ==> |
| | | Органічні сполуки, які визначають амперометричним титруванням |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |