
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Точність титрування.
Класифікація методів об’ємного аналізу за способом титрування
Окрім класифікації методів об’ємного аналізу за типом хімічної реакції, їх розрізняють за способом титрування. Розглянуті вище приклади відносяться до методів прямого титрування. Вони передбачають пряму взаємодію речовини робочого розчину з речовиною, що титрується.
Поряд з цим велике значення мають непрямі методи, з яких найважливішими є метод заміщення і метод залишків.
Метод заміщення застосовується тоді, коли неможливе пряме титрування (речовина не реагує з робочими розчинами, або реакція відбувається не в стехіометричних співвідношеннях, або, нарешті, неможливо підібрати індикатор). Так, наприклад, іони Ca2+ неможливо безросередньо титрувати ні кислотою або основою, ні окисниками або відновниками. Тому його спочатку зв’язують оксалат-іонами
Ca2+ + C2O42+ = CaC2O4¯
виділяють щавлеву кислоту з осаду
CaC2O4 + 2H+ = Ca2+ + H2C2O4
і титрують останню робочим розчином перманганату
5 H2C2O4 + 2MnO4- + 6H+ = 2 Mn2+ + 10CO2 +8 H2O
Очевидно, що в цих методах використовуються т. з. “спряжені” реакції. Із застосуванням методу заміщення ми стикнемось при подальшому вивченні курсу.
Метод залишків (зворотнє титрування) полягає в тому, що досліджувану речовину обробляють спочатку фіксованим надлишком першого робочого розчину, а потім залишок першого робочого розчину відтитровується другим робочим розчином. Приклад: карбонат кальцію може реагувати з соляною кислотою, тим не менш реакція йде повільно, особливо поблизу точки еквівалентності. Тому пряме титрування утруднене. Значно зручніше до наважки CaCO3 додати певний надлишок HCl, нагріти, розчинити весь карбонат кальцію
CaCO3 + 2HCl = CaCl2 + CO2 + H2O (HCl надлишок)
а надлишок відфільтрувати другим робочим розчином лугу
HClнадл + NaOH = NaCl + H2O
Метод залишків застосовують тоді, коли пряма реакція йде повільно, або тоді, коли неможливо підібрати для прямого титрування підходяще середовище чи індикатори.
Точність об’ємно-аналітичного визначення залежить від багатьох факторів. Одним із головних з них є точність виміру об’єму розчинів. Якщо користуватись звичайними бюретками, то точність виміру складає 0,05 мл і відносна похибка при затрачених на титрування 25 мл розчину складе
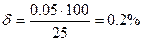
Якщо ж взяти 1 мл розчину, то похибка зросте в 25 раз
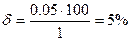
Легко підрахувати, що при користуванні мікробюретками з точністю відліку 0,01 мл відносна помилка визначення 0, 04% і 1%. Практичні висновки полягають в тому, щоб на титрування йшло не менше 10-20 мл титранта. При дефіциті матеріалу, що аналізується, слід користуватись бюретками з меншою ціною поділки (мікробюретки).
Інші джерела помилок полягають у тому, що точка еквівалентності не співпадає з точкою кінця титрування. Потрібно при виборі методу аналізу максимально зближати ці точки (приклад з титруванням оцтової кислоти NaOH рН=9, рТлакмусу= 7, рТф-ф=9).
Третя група помилок пов’язана з характером зміни концентрацій реагуючих компонентів поблизу точки еквівалентності. Це питання буде розглянуто при розгляді кривих титрування методу нейтралізації.
Читайте також:
- Довірчий інтервал характеризує точність вимірів даної вибірки, а довірча імовірність – достовірність виміру.
- ОСОБЛИВОСТІ РЕАКЦІЇ ОРГАНІЗМУ ДИТИНИ НА ФІЗИЧНІ НАВАНТАЖЕННЯ У РІЗНІ ВІКОВІ ПЕРІОДИ, ТОЧНІСТЬ ВИКОНАННЯ РУХІВ
- Перевірка на точність відображення
- Плани (карти) землеволодінь та землекористувань, що підлягають коригуванню. Точність і способи коригування
- Повнота і точність інформаційного обслуговування
- Продуктивність і точність обчислень.
- ТЕМА 11. ТОЧНІСТЬ І ДОРЕЧНІСТЬ МОВЛЕННЯ. СКЛАДНІ ВИПАДКИ СЛОВОВЖИВАННЯ. ПАРОНІМИ ТА ОМОНІМИ.
- ТЕМА: МЕТОДИ КІЛЬКІСНОГО АНАЛІЗУ. ТИТРИМЕТРИЧНИЙ МЕТОД АНАЛІЗУ. МЕТОД КИСЛОТНО-ОСНОВНОГО ТИТРУВАННЯ.
- Точність визначення площі планіметром
- Точність визначення площі району
- Точність і ефективність обчислень
- Точність мовлення
| <== попередня сторінка | | | наступна сторінка ==> |
| Точка еквівалентності. Індикатори. | | | Визначення нормальності робочих титрованих розчинів |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |