
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Принципіальні схеми абсорбції
В хімічній техніці використовують наступні принципові схеми абсорбційних процесів: прямоточні, протиточні, одноступінчаті з рециркуляцією і багатоступінчасті з рециркуляцією.
Прямоточна схема взаємодії речовин в процесі абсорбції показано на рис.9.5.1. В цьому випадку струми газу і абсорбенту рухаються паралельно один до одного; при цьому газ з з більшою концентрацією речовини, що розподіляється, приводиться в контакт з рідиною, що має меншу концентрацію речовини, що розподіляється, а газ з меншою концентрацією взаємодіє на виході з апарату з рідиною, яка має більшу концентрацію речовини, що розподіляється.
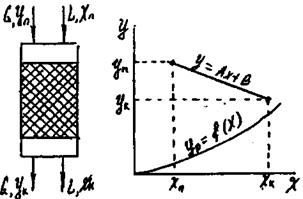
Рис.9.5.1 .Прямоточна схема абсорбції.
Протиточна схема показана на рис.9.5.2. За цією схемою в одному кінці апарату приводяться в контакт газ і рідина, які мають великі концентрації речовини, що розподіляються, а в протилежному кінці - менші.

Рис. 9.5.2 Протиточна схема абсорбції.
Схеми з рециркуляцією передбачають багатократне повернення в апаратуру або рідини, або газу. Схема з рециркуляцією рідини показана на рис.9.5.3.
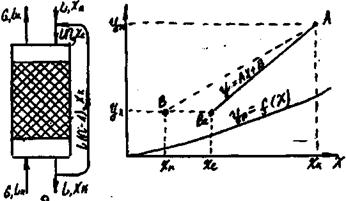
Рис.9.5.3 Схема абсорбції з рециркуляцією рідини.
Газ проходить через апарат знизу вгору, і концентрація речовини, що розподіляється в ньому змінюється від Уп до Ук. Рідина яка поглинає підводиться до верхньої частини апарата при концентрації речовини, що розподіляється Хn, потім змішується з рідиною яка виходить з апарату, як результат відбувається підвищення концентрації до Хс. Робоча лінія зображується на діаграмі відрізком прямої; крайні точки його мають координати Yп, YK і Хк , Хп відповідно. Величину Хс легко знайти з рівняння матеріального балансу.
Позначимо відношення кількості поглинаючої рідини на вході в апарат до кількості свіжої поглинаючої рідини через ni, тоді
G(Yп-Yк) = L(Хк-Хn) = L(Хк-Хc ), (9.5.1)
і
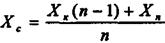 (9.5.2)
(9.5.2)
Схема абсорбції з рециркуляцією газу приведена на рис.8.5.4. Тут матеріальні співвідношення аналогічні попереднім. Положення робочих ліній визначають точки Ас (Yc, Хк ) і В (Yк, Хп); ордината Yс знаходиться з рівняння матеріального балансу:
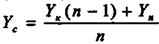 (9.5.3)
(9.5.3)
Одноступінчаті схеми з рециркуляцією можуть бути як протиточні, так і прямоточні.
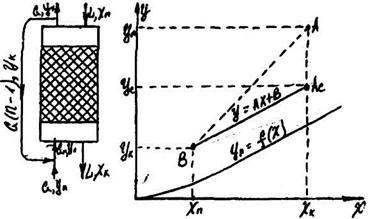
Рис. 9.5.4. схема абсорбції з рециркуляцією газу.
Багатоступінчасті схеми з рециркуляцією можуть мати прямоток, протиток, рециркуляцію рідини і рециркуляцію газу. Велике практичне значення має багатоступінчаста протиточна схема з рециркуляцією рідини в кожному ступені. Ця схема показана на рис. 9.5.5.
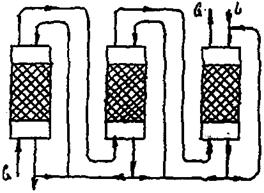
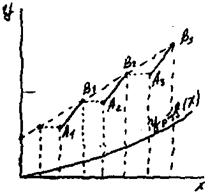
Рис. 9.5.5. Схема багатоступінчастої абсорбції з рециркуляцією рідини.
Робочі лінії наносяться на діаграму окремо для кожного ступеня, як і у випадку декількох окремих одноступінчатих апаратів. У розглянутому на рисунку прикладі робочі лінії складають відрізки А1В1, А2В2, A3B3.
Співставимо розглянуті схеми абсорбції, враховуючі наступні показники процесу: питому витрату абсорбенту, рушійну силу процесу і коефіцієнти масопередачі. На рис.9.5.6 показані прямоточні протиточні процеси при заданих їх параметрах: Уп, Ук і Xп.
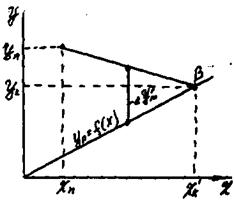

Рис.9.5.6. Рушійна сила прямоточного (а) і протиточного (б) процесів абсорбції.
На рисунках показані також граничні положення робочих ліній, коли концентрації Х`к для прямого току і Х"K для протитоку досягають рівноважних значень. З приведених графіків видно, що Х"K>Х'к а ΔY"m < ΔY'm.
Тому протиточний процес забезпечує більшу кінцеву концентрацію газу, що поглинається, в абсорбенті, а разом з цим і меншу витрату абсорбенту; рушійна сила при протитоці менша, а тому при інших рівних умовах необхідні більші розміри апарата. Вказане співвідношення носить загальний характер і його можна формувати як: зміна робочих концентрацій, яка призводить до зменшення витрати абсорбенту, потребує збільшення габаритів апарата, і навпаки.
Одноступінчаті з рециркуляцією абсорбенту або газу порівняно зі схемами без рециркуляції мають наступні особливості. При одній і тій же витраті свіжого абсорбенту кількість рідини, яка проходить через апарат, значно більше; як результат цього є збільшення коефіцієнта масопередачі і деяке зменшення рушійної сили. При певному співвідношенні між дифузійними опорами в рідкій і газовій фазах це може призвести до зменшення габаритів апарата.
Очевидно, що рециркуляція рідини доцільна у тому випадку, якщо основний опір масопередачі складає перехід речовини від поверхні розділу фаз в рідину, а рециркуляція газу - коли основним опором процесу є перехід речовини з газової фази до поверхні розділу фаз. Рециркуляції рідини завжди віддається перевага при необхідності супроводжувати процес абсорбції охолодженням, так як в цьому випадку включення холодильника в галузь рециркулюючого абсорбенту дозволяє досить легко відводити тепло від взаємодіючих речовин.
Багатоступінчасті схеми з рециркуляцією мають всі переваги одноступінчатих схем і разом з тим забезпечують більшу рушійну силу процесу. З цієї причини в більшості випадків вибирають варіант багатоступінчастих рециркуляційних схем.
10 Перегонка рідин
Вступ
Перегонка рідин являє собою процес, в якому рідка суміш, що розділяється, нагрівається до кипіння, а пар, що утворився відбирається і конденсується. В результаті отримуємо рідину, склад якої відрізняється від складу вихідної суміші.
Розділення перегонкою базується на різній летючості компонентів суміші при одній і тій же температурі. Тому при перегонці всі компоненти суміші переходять в пароподібний стан в кількостях, пропорційних їх фугітивності.
В багатьох випадках вихідна суміш є бінарною, тобто складається з двох компонентів. Пар, що отримується при її перегонці містить відносно кількість легколетючого, або низькокиплячого, компонента (НК), ніж вихідна суміш. Тому, в процесі перегонки рідка фаза збіднюється, а парова фаза збагачується НК. Рідина, що не випарувалася, має склад більш багатий важко летючим, або висококиплячим компонентом (ВК).
Ця рідина називається залишком, а рідина, отримана в результаті конденсації парів, -дистилятом, або ректифікатом.
Ступінь збагачення парової фази НК при інших рівних умовах залежить від виду перегонки. Існує два принципово різних вида перегонки:
1) проста перегонка (дистиляція);
2) ректифікація.
Дистиляція (проста перегонка) являє собою процес одноразового часткового випаровування рідкої суміші і конденсації парів, що утворюються.
Значно більш повніше розділення рідких сумішей на компоненти досягається шляхом ректифікації.
Ректифікація являє собою процес багатократного часткового випаровування рідини і конденсації парів. Процес здійснюється шляхом потоку пару і рідини, які мають різну температуру, і проводяться звичайно в колонних апаратах. При кожному контакті з рідини випаровується переважно НК, котрим збагачуються пари, а з парів конденсуються переважно ВК, які переходять в рідину. Такий двосторонній обмін компонентами, що повторюється багато раз, дозволяє отримати в кінцевому рахунку пари, які являють собою майже чистий НК. Ці пари після конденсації в окремому апараті дають дистилят (ректифікат) і флегму - рідину, яка повертається для зрошення колони і взаємодії з парами, що піднімаються. Пари отримують шляхом часткового випаровування знизу колони залишку, є майже чистим ВК.
Процеси перегонки здійснюються періодично або безперервно.
10.1 Характеристики двофазних систем рідина - пар
Якщо система складається з двох компонентів (К=2) і між ними не проходить хімічна реакція, то при наявності рідкої та парової фаз число фаз Ф=2. Згідно правилу фаз, число ступенів свободи такої системи складне:
С=К+2-Ф=2+2-2=2
Тому, з трьох незалежних параметрів, які повністю визначають стан системи: температури t, тиску Р і конденсації С - можна довільно вибрати будь - які два ; при цьому визначиться значення третього параметра, котре вже не може бути довільним.
У зв'язку з цим для фізико-хімічної характеристики бінарних систем рідина - пар користуються так званими фазовими діаграмами. Якщо позначити через X склад рідкої фази, а через У - склад парової фази, то, приймаючи t=const, можна побудувати графік залежності тиску пару від складу рідини (діаграма Р-х). Аналогічно, вважаючи постійним тиск парів (P=const), зображують на площині залежність температури кипіння рідини і конденсації парів від складу рідкої та парової фаз (діаграма t-x-y). При P=const t=const знаходять залежність між рівноважними складами фаз, котра зображується діаграмою рівноваги (діаграма у-х).
Вигляд цих залежностей визначається взаємною розчинністю компонентів рідкої суміші і іншими їх властивостями.
Класифікація бінарних сумішей
В залежності від взаємної розчинності компонентів розрізняють суміші рідин:
-з необмеженою взаємною розчинністю;
-взаємно нерозчинні;
-обмежено розчинні один в одному.
Суміші з необмеженою взаємною розчинністю компонентів в свою чергу поділяються на ідеальні суміші з позитивним або від'ємним відхиленням від закону Рауля.
Читайте також:
- VІ. Структурно-логічні схеми
- Алгоритми та блок-схеми
- Блоки схеми алгоритму
- Вибір схеми підключення абонентів залежно від режимів тиску.
- Вибір типу обмотки і складання схеми.
- Вибір типу обмотки і складання схеми.
- Види і схеми відбору одиниць
- Види недержавного пенсійного забезпечення та схеми фінансування пенсійних виплат.
- Визначення сумарної маси еквівалентної схеми V- подібного КШМ.
- ГЕНПЛАНИ ОЧИСНИХ СПОРУДЖЕНЬ І СХЕМИ ВИСОТНОГО РОЗТАШУВАННЯ ОЧИСНИХ СПОРУДЖЕНЬ .
- Гібридні системи, індексні схеми
- Головні завдання Регіональної схеми розселення на Україні.
| <== попередня сторінка | | | наступна сторінка ==> |
| Тепловий баланс і температура абсорбенту | | | Принцип ректифікації |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |