
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Білок р53 як чинник транскрипції
Серед великого кількості вже відкритих чинників транскрипцій найбільш відомий, мабуть, білок р53. Це пояснюється тим, що він контролює виключно важливі клітинні процеси і, завдяки цьому, залучений у велику кількість різних регуляторних ланцюгів.
а) Функціональна роль.
Білок р53 (чи його ген) активується у відповідь на різноманітні ушкодження клітинної структури :
- нерепаровані розриви і інші ушкодження ДНК
- порушення розбіжності хромосом в мітозі
- руйнування мікротрубочок і т. д.
Сам же білок р53 регулює активність, принаймні, трьох груп генів :
1) активує гени (Р21, GADD45 та ін.), що відповідають за зупинку клітинного поділу;
2) активує гени (ВАХ, KILLER/DR5, PIG та ін.), які запускають апоптоз - процес, що призводить, шляхом активації спеціальних ферментів, до загибелі клітини; а також репресує гени (BCL2, RELA), стримуючі апоптоз.
3) активує гени (ТSР1, ВАІ1 та ін.), що гальмують ангіогенез (утворення нових судин).
У результаті через посередництво білку р53 клітина у відповідь на ушкодження своєї структури
· або затримується на тій або іншій стадії мітотичного циклу і виправляє ці ушкодження;
· або (при неможливості виправлень) взагалі зупиняє поділ і вступає в процес клітинного старіння (фаза III по Хейфлику);
· або (при потенційній небезпеці пошкодженої клітини для її оточення) здійснює апоптоз, тобто, попросту кажучи, самогубство.
Зокрема, апоптозу, окрім інших, піддаються і клітини, в яких сталася пухлинна трансформація. В зв'язку з цим зрозуміло, чому одночасно гальмується ангіогенез: це ще один спосіб обмеження пухлинного зростання.
Тому білок р53 - один з найбільш важливих опухолевих супресорів. У більшості ж пухлин, що розвиваються, функції білку р53 опиняються в тому або іншому відношенні порушеними.
Така загальна біологічна роль білку р53.
Розглянемо деякі пов'язані з ним питання детальніше.
б) Структура білку р53.
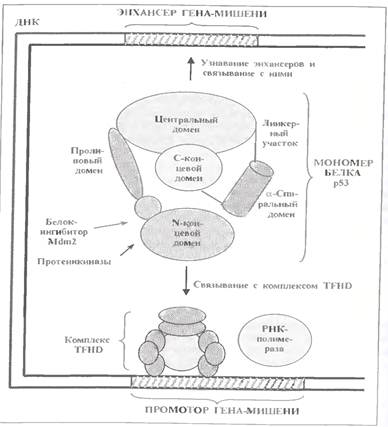
Білок р53 не входить ні в одну з тих родин ДНК-зв’язуючих білків, які були описані в вище. У його молекулі - 392 амінокислотні залишки, що утворюють шість різних за розміром і функціями доменів (див.мал.).
Центральний і найбільший домен (що включає близько 200 залишків) відповідає за впізнавання енхансерів генів-мішеней і зв'язування з ними.
А найперший від N-конца (N-кінцевої) домен бере участь у взаємодії із загальними чинниками транскрипції, тобто з комплексом TFIID. Іншими словами, саме два названі домени забезпечують правильне зв'язування білку р53 з його основними партнерами.
Але це зв'язування знаходиться під контролем багаточисленних чинників.
Так, в тому ж N-домені є локус зв'язування з білком-інгібітором Mdm2, який блокує взаємодію з комуплексом TFIID. І тут же присутні залишки серина і треоніна, які можуть фосфорилювати спеціальними протеінкіназами (ДНК протеінкіназою, білком ATM та ін.).
Ці кинази активуються при ушкодженнях ДНК і інших структур клітини. Їх дія на N-домен, а також, мабуть, на сам інгібітор Mdm2 вивільняє цей домен з-під блокуючого впливу: він набуває здатності взаємодіяти з комплексом TFIID.
Взаємодія центрального домена з енхансером теж знаходиться під контролем, який знову здійснюється шляхом модифікації. Але безпосереднім об'єктом модифікації є не центральний, а С-кінцевий (він же лужний) домен. Причому сама модифікація є різноманітнішою: це не лише фосфорилювання, але також ацетилювання і глікозілювання (що також здійснюється спеціальними ферментами).
Якщо С-кінцевий домен не модифікований, центральний домен не здатний взаємодіяти з ДНК-мішенню. Модифікація ж С-домена не лише надає білку р53 таку здатність, але і впливає на його специфічність. Річ у тому, що р53-залежні енхансери (що відносяться до різних генів) дещо відрізняються послідовністю нуклеотидних пар. І від виду модифікації С-домена залежить, з якими конкретно енхансерами зв'язуватиметься білок р53, а з якими - ні.
Таким чином, за допомогою модифікації двох кінцевих (N- і С -) доменів білок р53 отримує (від дуже численних "джерел") інформацію про стан клітини, переробляє її шляхом зміни своєї конфігурації і належним чином реагує як чинник транскрипції певних генів.
С-кінцевий домен виконує ще одну функцію. Як відмілось вище, деякі гени (ВСL2, RЕLА) білком р53 не активуються, а репресуються. Ця дія, як вважають, здійснюєтьсяся С-доменом. При цьому останній (замість N-домена) зв'язується з комплексом TFIID і пригнічує його активність.
Досить важлива функція і інших частин білку р53. Так, в клітині його молекули утворюються один з одним тетрамерні комплекси: це звичайний стан білку незалежно від рівня його активності. За утворення ж комплексів відповідає α-спіральний домен, що є попередником С-кінцевому домену. У мономірному стані білок р53 не здатний до активації.
Між центральним і α-спиральним доменами знаходиться функціонально важлива лінкерна (єднальна) ділянка. Вважають, що він потрібний для проникнення новосинтезованного білку р53 з цитоплазми в ядро.
Нарешті, між N- кінцевим і центральним доменами розташовані ще дві невеликі домени, один з яких багатий на залишок проліну. Обоє вони беруть участь в активації тих або інших мішеней.
Таким чином, структура білку р53 дуже складна, що цілком відповідає його украй важливій функціональній ролі.
в) Обмін білку р53.
У клітинах білок р53 постійно синтезується і так же постійно руйнується. Тому в клітинах більшості тканин середня тривалість життя молекул білку і їх стаціонарна концентрація виявляються дуже низькими.
Але при стресах і ушкодженнях клітини швидкість деградації білку р53 сповільнюється, що призводить до збільшення його концентрації. Іншими словами, використовуються два способи включення білку р53 в "роботу":
- підвищення його вмісту (шляхом зниження швидкості розпаду)
- підвищення активності (шляхом модифікації).
Відмітимо: у разі переважної більшості інших білків збільшення концентрації досягається іншим способом - шляхом активації гена і, отже, швидкості синтезу білку. Ген р53, як ми бачимо, досить активно функціонує практично завжди.
Відомі лише одиничні ситуації істотної його активації в порівнянні із звичайним рівнем. Це ранній ембріогенез, а також розвиток ембріональної тератокарціноми.
Читайте також:
- Адаптація організму до змін чинників зовнішнього середовища
- Біохімічні чинники виникнення втоми при виконанні короткочасних вправ максимальної і субмаксимальної потужності
- Видатки та заощадження як функції доходу. Автономні величини та їх чинники. Крива планових видатків.
- Види виробничої потужності, чинники, що її визначають, послідовність розрахунків
- Визначення та класифікація небезпечних і шкідливих виробничих чинників, характерних для офісів та фінансових.
- Виробництво. Головні чинники зростання ефективності виробництва.
- Виробниче середовище: сутність і основні чинники.
- Влада як суспільне відношення і як системоутворюючий чинник.
- Внутрішні чинники
- Внутрішні чинники ризику
- Вплив геохімічних та геофізичних чинників біосфери на здоров’я людини
| <== попередня сторінка | | | наступна сторінка ==> |
| Загальні чинники транскрипції | | | Загальний план будови РНК |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |