
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Характеристика компонентів системи
У чистому вигляді залізо зустрічається у формі метеоритного або у вкрапленнях гірських порід, що утворилися з магми
Залізо м'який, пластичний матеріал. Технічне залізо має наступні характеристики механічних властивостей:
sв=250МПа; sу=120МПа; d=50%; Y=85%; 80НВ.
Залізо — перехідний елемент VIII групи IV періоду, має порядковий номер 26. Атомна маса 55,85. Електрони по енергетичних рівнях розподілені в такий спосіб: 1S22 S 22р63 S 23р63d64 S 2.
Зовнішні електронні оболонки атома заліза мають конфігурацію З d 64 S 2. У конденсованих залізних фазах зовнішні електрони утворять енергетичний спектр із широких що перекриваються S - і d -полос. У зв'язку із цим переходи електронів на зовнішніх рівнях відбуваються порівняно легко, що легко, що обумовлює змінну валентність
Відповідно до діаграми фазової рівноваги (рис. 6.1) можливі шість станів заліза: газоподібний з дуже слабким вандерваальсовим міжатомним зв'язком і п'ять конденсованих станів з металевим зв'язком, енергія якої оцінюється в 320-340 Дж/кмоль. Конденсовані фази - рідке залізо й чотири кристалічні поліморфні модифікації: α- Fе; γ - Fе; δ - Fе; ε- Fе.

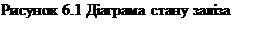
Залежно від зовнішніх умов кристалічне залізо може бути представлено одним із трьох типів кристалічних ґрат: кубічною об'ємноцентрованою (α- Fе і δ - Fе), кубічної гранецентрованою (γ-Fе ), гексагональною щільноупакованною (ε- Fе). Можливо ще один рівноважний стан. При дуже високих температурах газоподібне залізо іонізується й переходить у стан плазми. Залізна плазма, що складається з іонів і електронів, поєднуваних взаємодією кулонівського типу, не має яких-небудь принципових відмінностей від інших видів плазми й по ряду властивостей різко відрізняється від залізного газу.
При атмосферному тиску (штрихпунктирна лінія на рис. 6.1) модифікація α- Fе стійка від абсолютного нуля до точки Аз (1183° К). До точки А2 (1041° К, точка Кюрі) залізо феромагнітне. При температурі, близької до точки А2, тепловий рух атомів розбудовує одноманітну орієнтацію спинових магнітних моментів електронів і α- Fе стає парамагнітним. Раніше залізо в інтервалі А2-А3 позначали як самостійну поліморфну модифікацію β- Fе. Однак, оскільки втрата феромагнетизму не пов'язана зі зміною типу ґраток, цим позначенням зараз не користуються.
В інтервалі температур від А3 до А4 (1673 °К) стійке γ – Fе від А4 до точки плавлення (1812 °К) стійке δ - Fе. Таким чином, особливість поліморфізму заліза у найбільш важливій для сучасної техніки області тисків і температур полягає в тім, що температурний інтервал існування модифікації з об 'ємноцентрованими ґратами розчленований на дві ділянки з областю стабільності модифікації із гранєцентрованими ґратами. Серед перехідних металів перетворення α- Fе - γ – Fе унікальне, тому що у всіх інших випадках перехід низькотемпературної модифікації у високотемпературну пов'язаний зі зменшенням щільності впакування.
Вуглець — елемент IV групи II періоду, порядковий номер 6, електронна структура 1 S22 S22р2. Конфігурація зовнішніх електронних оболонок 2 S22р2. При втраті всіх чотирьох електронів зовнішньої оболонки атомний радіус суттєво зменшується(більш ніж в чотири рази). При розчиненні в залозі вуглець звичайно іонізується до С4+, малі розміри якого визначають відносно високу розчинність вуглецю в конденсованих залізних фазах (крім об 'ємноцентрированих упакувань), а також його високу дифузійної рухливість.
Вуглець поліморфний, на діаграмі стану показані області стійкості трьох модифікацій (рис. 6.2). В звичайних умовах стабільний графіт, що характеризується пошаровою будовою. Атомна структура одного шару гексагональна сітка, у вузлах якої розташовуються атоми вуглецю. Ковалентні зв'язки здійснюються спарюванням трьох валентних електронів кожного атома з електронами трьох навколишніх його сусідів . Четверті валентні електрони колективізуються, і це надає графіту металеві властивості: високу електричну провідність, непрозорість, блиск. Кожний шар графіту можна розглядати як плоску макромолекулу, поляризовану під дією сусідніх макромолекул. Дві інші модифікації вуглецю в залізовуглецевих сплавах не зустрічаються


Крім основних компонентів, технічні залізовуглецеві сплави містять ряд домішок. Їх можна розбити на три групи:
1) технологічні (звичайні) домішки (Мп, Р, S, Н, N. О);
2) легуючі й прим, якими модифікують і легують сплави
(елементи, що вводять спеціально в сплави , для регулювання, їхньої структури й властивостей; інколи ними можуть бути звичайні домішки в підвищених концентраціях);
3) випадкові або природні домішки, які попали у сплав пов'язане із природою та шихтовими матеріалами (мідь в уральських залізних рудах
залізних рудах, миш'як у керченській та т.і.).
Читайте також:
- I. Загальна характеристика політичної та правової думки античної Греції.
- I. Органи і системи, що забезпечують функцію виділення
- I. Особливості аферентних і еферентних шляхів вегетативного і соматичного відділів нервової системи
- II. Анатомічний склад лімфатичної системи
- II. ВИРОБНИЧА ХАРАКТЕРИСТИКА ПРОФЕСІЇ
- II. Морфофункціональна характеристика відділів головного мозку
- IV. Розподіл нервової системи
- IV. Система зв’язків всередині центральної нервової системи
- IV. Філогенез кровоносної системи
- POS-системи
- T. Сутність, етіологія та патогенез порушень опорно-рухової системи
- VI. Філогенез нервової системи
| <== попередня сторінка | | | наступна сторінка ==> |
| Діаграми стану залізовуглецевих сплавів | | | Характеристика фаз |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |