
МАРК РЕГНЕРУС ДОСЛІДЖЕННЯ: Наскільки відрізняються діти, які виросли в одностатевих союзах
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
Контакти
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
І. Теоретична частина
Реакція ацилювання спиртів карбоновими кислотами називається реакцією естерифікації. Ця реакція є оборотною, відбувається лише при нагріванні та присутності кислотного каталізатора (сірчана кислота, безводний хлороводень, сульфокислоти, іонообмінні смоли). Методом «мічених атомів» (використовували спирт, який містив важкий ізотоп кисню 18О) було встановлено, що в реакції естерифікації молекула води утворюється із гідроксилу карбонової кислоти та водню спирту («мічений» атом кисню після реакції входив до складу естеру).
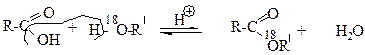
Швидкість утворення естеру залежить від будови кислот та спиртів. Реакційна здатність в реакціях естерифікації зменшується в наведених рядах спиртів та кислот ( М.О.Меншуткін):
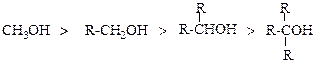
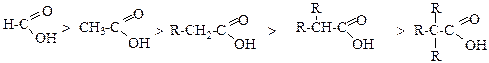
У ароматичному ряді зменшення швидкості естерифікації може бути викликане стеричними факторами. Відомо, що орто-заміщені ароматичні карбонові естерифікуються дуже важко.
За законом діючих мас вихід естеру підвищується зі збільшенням концентрації однієї з вихідних речовин ( чи то спирту, чи то карбонової кислоти). Найчастіше використовують п,яти-десятикратний надлишок найдешевшого реагенту. Збільшення виходу відбувається також при вилученні із реакційної сфери продуктів реакції: води або естеру. Слід зауважити, що каталізатор підвищуює одночасно швидкість реакції естерифікації і гідролізу, тому не впливає на стан рівноваги.
Реакція естерифікації при наявності каталітичних кількостей кислоти відбувається за таким механізмом:
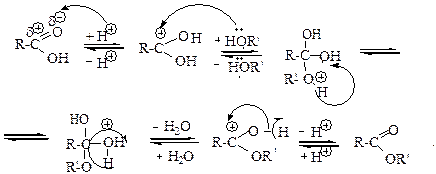
Для синтезу бензойноетилового естеру (етилбензоату) використовують сірчану (сульфатну) кислоту як каталізатор. Оскільки бензойна кислота – тверда речовина, то для зміщення рівноваги беруть у надлишку етиловий спирт.
Читайте також:
- I. Вступна частина
- II Основна частина
- II Основна частина
- II Основна частина
- II частина
- II частина.
- II. Основна частина
- II. Основна частина
- II. Основна частина ЗАНЯТТЯ
- III Заключна частина
- III Заключна частина
- III Заключна частина
| <== попередня сторінка | | | наступна сторінка ==> |
| Техніка безпеки | | | ІІ. Експериментальна частина |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |