
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Частина III. Масообмінні процеси
Розділ 6. Випарювання
Значна частина енергії, що споживається промисловістю затрачається на розділення та очистку речовин за допомогою масообмінних процесів. В цих процесах зміна складу сумішей виконується в основному дифузійним, а не механічним шляхом. Тому такі технологічні процеси, як фільтрація та відстоювання, в цьому розділі взагалі не розглядаються.
Так як основну увагу в цій книзі приділяють економії енергії, то як об'єкти вивчення вибрані найбільш енергомісткі масообмінні процеси. Основною метою всіх цих процесів є отримання кінцевих продуктів з більш впорядкованим станом речовини із сировини, що характеризується меншою впорядкованістю. Таке зниження ентропії2 системи досягається, зазвичай, шляхом підведення тепла. Оскільки кінцевий продукт містить не більше енергії, ніж сировина, то все тепло, що підводиться для їх виділення, в кінцевому результаті відводиться в навколишнє середовище. Тобто, маємо можливість значної економії енергії шляхом більш ефективного способу виконання цих процесів. Для визначення ефективності процесу розділення використовується метод ентропійного аналізу. Цей метод не є традиційним при оцінці масообмінних процесів, однак він може виявити нові шляхи збільшення економії енергії.
Процес випарювання вибраний для введення в об'єкт регулювання масообмінних процесів, тому що цей процес простий в математичному вираженні, але ще складний в регулюванні. Використання таких технологічних методів, як повторний стиск пари, дозволяє значно зекономити енергію. Однак ці методи описуються термодинамічними співвідношеннями, які необхідно зрозуміти до того, як ефективно використовувати в регулюванні.
6.1 Системи випарювання
Випарювання - це процес виділення леткої рідини із нелеткої твердої речовини шляхом підведення тепла. Протягом багатьох століть такий спосіб використовується для екстракції3 солі з морської води за допомогою сонячної енергії. На цукровому заводі в Новій Англії концентрування цукрового сиропу виконується шляхом кип'ятіння на вогні.
 Технологічний процес концентрування розчинів шляхом виділення розчинника і перетворення його на пару.
Технологічний процес концентрування розчинів шляхом виділення розчинника і перетворення його на пару.
Фізична величина, яка в спостережуваних явищах і процесах характеризує знецінювання(розсіювання) енергії, зумовлене перетворенням усіх її видів на теплову і рівномірним розподілом тепла між тілами.
Спосіб розділення суміші речовин на складові частини за допомогою розчинника, в якому вони розчиняються неоднаково.
В більшості процесів випарювання тверді матеріали являють собою більш цінний продукт, ніж видаляючий розчинник. Випарювання використовується також і для отримання прісної води із морської води, промислових розчинів і стоків, тверді продукти яких є менш цінними.
Випарювання відрізняється від сушіння тим, що воно здійснюється при відсутності повітря або інших газів, що не конденсуються. Рівняння рівноваги стану при сушінні ускладнюється через необхідність обліку ще одного додаткового параметру.
6.1.1 Багатокорпусне (багатоступеневе) випарювання
Використання підігріву для отримання цукрового сиропу надзвичайно неефективне. Процес все одно буде неефективним навіть в тому випадку, коли втрати тепла мінімальні і коефіцієнт надлишку повітря ретельно регулюється. На сучасних промислових підприємствах для концентрації цукрових розчинів і сиропів застосовується багатоступінчате (багатокорпусне) випарювання з багаторазовим використанням енергії, що підводиться.
На рис 6.1 показано трьохкорпусний випарний апарат для концентрації розведеного розчину. Якщо транспортування кінцевого продукту не викликає ускладнень через високу в'язкість або наявність в ньому плаваючих твердих частинок, і якщо він термостійкий, то можна використовувати випарні апарати значної ємності. Зазвичай в них розташований великий жмут теплообмінних труб, який називається трубчастим кип'ятильником випарного апарату. Парозбірник завантажений трубами, по яких під дією природної конвекції1 циркулює кипляча рідина.

Рис. 6.1. Трьохкорпусний випарний апарат з прямотечійним рухом пари і розчину
 1 Явище перенесення тепла в рідинах, газах або сипких середовищах потоками самої речовини(не важливо, вимушено чи мимоволі).
1 Явище перенесення тепла в рідинах, газах або сипких середовищах потоками самої речовини(не важливо, вимушено чи мимоволі).
Відведена з першого корпусу вторинна пара конденсується киплячою рідиною в другому корпусі, що має нижчий тиск тощо. В кожному корпусі кількість утвореної пари менша від кількості сконденсованої пари внаслідок збільшення прихованої теплоти пароутворення при зниженні тиску і температури. Для передачі потрібної кількості тепла кожна поверхня теплообміну повинна мати відповідний градієнт температури. Ця різниця температури врешті визначає тиск в різних корпусах і теплову економічність установки в цілому.
Випарювання таких нечутливих до впливу температури продуктів, як, наприклад, морська вода, може здійснюватись в тринадцятикорпусному випарному апараті. Внаслідок збільшення прихованої теплоти пароутворення і втрат тепла, кожний наступний корпус випарного апарату є менш ефективним, ніж попередній, що не стимулює додаткових капіталовкладень для їх побудови. Для випарювання таких термочутливих продуктів, як харчові продукти, необхідно обмежуватись двома або трьома корпусами. Температура в останньому корпусі обмежується як кількістю охолоджуючої води, так і в'язкістю кінцевого продукту, тоді як температура першого корпусу визначається лише термостійкістю твердої речовини.
Незважаючи на те, що розбавлені розчини можуть випарюватись в трьох-або чотирьохкорпусних апаратах, кінцеві продукти, що мають концентрацію 75-85%, зазвичай піддаються технологічній обробці в двохкорпусній установці.
Труднощі, пов'язані із транспортуванням в'язких розчинів, можна вирішити шляхом зміни напряму руху гріючої пари і випарюваного розчину. На рис. 6.2 зображені випарні апарати з протитечійним і змішаним напрямком руху пари і розчину. Необхідно зазначити, що корпуси завжди нумеруються в одному і тому ж порядку: від корпуса з найбільшим тиском до корпуса з найменшим тиском.
В промисловості використовуються найрізноманітніші схеми руху потоків. В деяких процесах два корпуси працюють по паралельній схемі підводу пари і по послідовний схемі подачі випарюваного розчину. Така система використовується при обробці відходів перегонки, коли корпуси 1а і 1б отримують гріючу пару з одного і того ж колектора і скидають його в корпус 2, а розчин рухається в зворотному напрямку з корпуса 2 послідовно в корпус 1а і після 1б.
З метою зниження до мінімуму часу перебування термочутливих матеріалів при підвищених температурах розроблені спеціальні конструкції випарних апаратів.
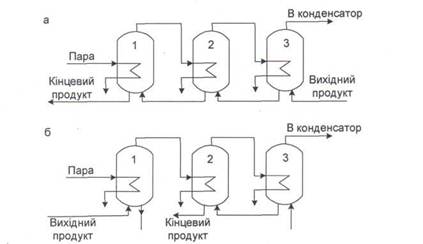
Рис. 6.2. Випарні апарати з протитечійним (а) і змішаним (б) напрямком руху
пари і розчину
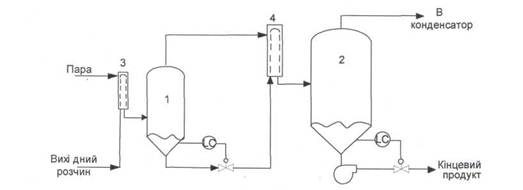
| Рис. 6.3. Випарний апарат з пропусканням невеликих кількостей рідини |
У випарній установці (рис. 6.3) інтенсивна подача тепла здійснюється через систему труб малого діаметра 3 і 4. Нагрітий розчин тоді потрапляє в випарник, де відбувається розділення пари і рідини. Час перебування матеріалу в зоні підвищених температур зменшується до мінімуму за рахунок малих витрат рідини і одноразового її пропускання через апарат, тобто без циркуляції. Такі випарні апарати швидко запускаються в роботу, але є чутливими до порушень їх режиму роботи і важкими в регулюванні.
6.1.2 Масовий та енергетичний баланси
Розглянемо випарний апарат, в якому підвищується концентрація вихідного розчину, що має масову витрату Fo, від початкової масової частки твердої речовини wo до кінцевої масової частки wn. Якщо витрата кінцевого продукту Fn, то баланс маси для твердої речовини описується рівнянням:

Загальний баланс маси для багатокорпусного випарного апарату буде враховувати всю кількість вторинної пари , видаленої з різних корпусів:
, видаленої з різних корпусів:

Об'єднавши ці два рівняння, отримаємо кількість вторинної пари, яку необхідно видалити для досягнення необхідної кінцевої концентрації розчину:

Кількість видаленої в першому корпусі вторинної пари пов'язана з кількістю гріючої водяної пари, що потрапляє в перший корпус, і з її термічним к.к.д. Е такою залежністю:

Аналогічно кількість вторинної пари, видаленої з другого корпусу, пов'язана з кількістю пари, виділеної в першому корпусі, відношенням:
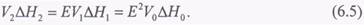
Таку послідовність можна продовжувати до n корпусів і після просумувати окремі витрати вторинної пари:
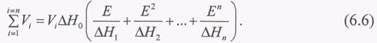
Збільшення ентальпії1  вторинної пари, що утворюється в процесі
вторинної пари, що утворюється в процесі
випаровування в даному корпусі, не дорівнює точно її прихованій теплоті пароутворення.
При прямотечійній схемі руху потоків розчин, що потрапляє в наступний корпус, внаслідок пониженого тиску буде мати більш високу температуру кипіння. Пара, що потрапляє в кожен наступний корпус, внаслідок підвищення температури кипіння розчину перегрівається.
З точки зору сумарного енергетичного балансу, ці фактори незначні. Кінцевий продукт, виходячи з прямотечійного випарного апарату, має приблизно
 Термодинамічний потенціал, що характеризує стан термодинамічної системи при виборі як основних незалежних змінних ентропії (S) і тиску (Р).
Термодинамічний потенціал, що характеризує стан термодинамічної системи при виборі як основних незалежних змінних ентропії (S) і тиску (Р).
ту саму температуру, що і вихідний розчин.
Якщо приховану температуру пароутворення використовувати для оцінки  в рівнянні (6.6), то можна легко підрахувати відношення кількості гріючої пари і вторинної пари для будь-якого випарного апарату. В табл.6.1 приведені ці
в рівнянні (6.6), то можна легко підрахувати відношення кількості гріючої пари і вторинної пари для будь-якого випарного апарату. В табл.6.1 приведені ці
співвідношення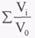 для випарних апаратів, що мають число корпусів п=8,
для випарних апаратів, що мають число корпусів п=8,
починаючи з температури Т=52°С в останньому корпусі, з припущенням, що різниця температур між корпусами складає 18 °С, а к.к.д. дорівнює 97%.
Таблиця 6.1.1
Співвідношення між гріючою парою і вторинною парою в залежності від числа корпусів при к.к.д. рівному 97%

6.1.3 Підвищення температури кипіння1
З наведених вище міркувань можна побачити, що шляхом зменшення перепаду температури в кожному корпусі можна збільшити число корпусів, отримавши значну економію гріючої пари. Перепад температури в корпусі можна до деякої степені зменшити шляхом збільшення відношення поверхні теплообміну до теплового потоку. Але навіть при великій поверхні або при малому потоці ( як і при умові низького теплового навантаження) в корпусі зберігається залишковий перепад температури, зумовлений підвищенням температури кипіння.
Підвищення температури кипіння, зумовлене присутністю нелеткої твердої
 1 Процес переходу рідини до пари, який характеризується, на відміну від випаровування, тим, що утворення пари відбувається не тільки на поверхні, але й в усій масі рідини.
1 Процес переходу рідини до пари, який характеризується, на відміну від випаровування, тим, що утворення пари відбувається не тільки на поверхні, але й в усій масі рідини.
речовини в розчині, випливає безпосередньо з фізичних законів і навіть може бути використане для розрахунку молекулярних мас твердих матеріалів. Наприклад, температура кипіння 1кг води при атмосферному тиску підвищується на ~ 0.5°С завдяки присутності одного моля нелеткої розчинної речовини. Цей показник змінний, він змінюється в залежності від температури:

де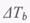 -підвищення температури кипіння, R=8.314 кДж/(кмоль*К) - універсальна газова стала, Т - нормальна температура кипіння в одиницях абсолютної шкали,
-підвищення температури кипіння, R=8.314 кДж/(кмоль*К) - універсальна газова стала, Т - нормальна температура кипіння в одиницях абсолютної шкали, 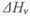 - теплота пароутворення і х - мольна частка розчиненої речовини.(Одиниці виміру можуть бути як британські, так і метричні). В таблиці 6.2 приведені дані про підвищення температури кипіння
- теплота пароутворення і х - мольна частка розчиненої речовини.(Одиниці виміру можуть бути як британські, так і метричні). В таблиці 6.2 приведені дані про підвищення температури кипіння розчинів сахарози при атмосферному тиску в залежності від концентрації твердих речовин w в даному розчині [1].
розчинів сахарози при атмосферному тиску в залежності від концентрації твердих речовин w в даному розчині [1].
Оскільки підвищення температури кипіння є функцією мольної, а не масової частки, тоді розчинені речовини, які мають більш низьку молекулярну масу, будуть істотно впливати на її величину. Розчин сахарози (молекулярна маса 342), що є 50%-ий в масовому вираженні, представляє собою лише 5% розчин в перерахунку на молі, тоді як 50%-ий по масі розчин каустичної соди (молекулярна маса 40), є 21%-им в мольному еквіваленті. Отже, при атмосферному тиску підвищення температури кипіння розчину каустичної соди складатиме ~ 11,12°С або буде в 6 раз перевищувати температуру кипіння розчину сахарози.
Таблиця 6.1.2
Читайте також:
- I. Вступна частина
- II Основна частина
- II Основна частина
- II Основна частина
- II частина.
- II. Основна частина
- II. Основна частина
- II. Основна частина ЗАНЯТТЯ
- III Заключна частина
- III Заключна частина
- III Заключна частина
- III Заключна частина
| <== попередня сторінка | | | наступна сторінка ==> |
| Оксиди сірки | | | Перевищення температури кипіння розчинів сахарози при атмосферному тиску |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |