
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
ЕЛЕКТРОДНИЙ ПОТЕНЦІАЛ. РІВНЯННЯ НЕРНСТА
 Якщо занурити металеву пластинку (електрод) у розчин електроліту, то між пластинкою і розчином виникає різниця потенціалів, яка має назву електродного потенціалу.
Якщо занурити металеву пластинку (електрод) у розчин електроліту, то між пластинкою і розчином виникає різниця потенціалів, яка має назву електродного потенціалу.
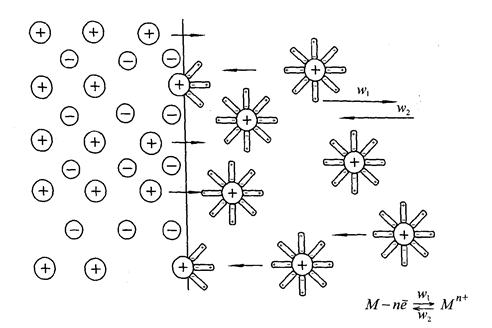
Рис. 16. Перехід іонів металу в розчин під впливом гідратації.
На рис. 16 зображено процеси, що протікають на межі розділу фаз: в результаті гідратації іонів поверхні металу (Меn+) їх зв’язок з кристалічною граткою послаблюється, і вони переходять в розчин. Поверхня металу набуває негативного заряду. Процес швидко досягає стану рівноваги.
При цьому на поверхні металу виникає подвійний електричний шар, падіння напруги в якому називають електродним потенціалом. Кількість іонів, які переходять у розчин з металу, безумовно залежить від їх концентрації в ньому.
Електростатичному притяганню протидіють сили взаємного відштовхування катіонів та їх тепловий рух. Тому подвійний електричний шар має дифузійну будову, концентрація катіону в ньому убуває по мірі віддалення від поверхні металу.
Виникнення подвійного електричного шару пов'язане з протіканням на межі метал – розчин рівноважних електрохімічних реакцій.
Електродний рівноважний потенціал залежить від активності іонів металу в розчині і температури.
Цю залежність виражають рівнянням Нернста:
Е = Ео + 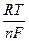 lna,
lna,
де Е - електродний потенціал, В;
Ео – стандартний електродний потенціал – потенціал електроду при активності іонів, що дорівнює 1;
R - універсальна газова стала; R = 8,314  ;
;
Т – температура, К;
n-зарядове число іона;
F- cтала Фарадея; F = 9,648∙104 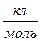
а - активність іонів в розчині.
Для досить розведених розчинів активність іонів в рівнянні Нернста можна замінити моляльністю m, 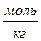 або концентрацією с:
або концентрацією с:
Е = Ео + 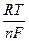 lnm або Е = Ео +
lnm або Е = Ео + 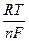 lnс
lnс
Для температури 298 К (25оС) рівняння Нернста при переході від натурального логарифма до десяткового приймає ще постійний вигляд:
Е = Ео + 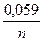 lgm
lgm
Абсолютне значення електродного потенціалу безпосередньо визначити неможливо. Тому для проведення дослідів застосовують умовну величину, що характеризує потенціал електроду відносно потенціалу іншого електроду, взятого за стандарт (електрод порівняння).
Зазвичай як електрод порівняння використовують стандартний водневий електрод, потенціал якого дорівнює нулю.
Відносно потенціалу цього електроду, всі стандартні потенціали металевих електродів будуть або позитивнішими, або від’ємнішими від нього.
Стандартний електродний потенціал – це електродний потенціал, що виникає при зануренні металу у розчин, в якому активність іонів цього металу становить 1 моль/л.
Якщо розташувати метали в порядку зростання значень їх стандартних потенціалів, то одержимо ряд стандартних електродних потенціалів, або електрохімічний ряд напруг:
Таблиця 1.8
Читайте також:
- V Процес інтеріоризації забезпечують механізми ідентифікації, відчуження та порівняння.
- VІI. Утворіть вищий та найвищий ступені порівняння від прислівників із вправи VI.
- Асимптотичний підхід до порівняння оцінок
- Бюджетний контроль - це порівняння показників бюджету зі звітом за відповідний період часу.
- В обох випадках основним розрахунковим рівнянням є рівняння теплопередачі і теплового балансу
- Векторне канонічне параметричне рівняння прямої в просторі.
- Вивід основного рівняння фільтрації
- Визначення типу порівняння даних
- Використання рівняння номінальних витрат за моделлю COCOMO II
- Виробничий і науково-технічний потенціал. Інформаційний потенціал
- Виробничі можливості. Виробничий потенціал. Межа виробничих можливостей.
- ВПРАВА 2. Утворіть де можливо, форми ступенів порівняння від поданих прикметників.
| <== попередня сторінка | | | наступна сторінка ==> |
| Вимірювання електропровідності | | | РЯД СТАНДАРТНИХ ЕЛЕКТРОДНИХ ПОТЕНЦІАЛІВ |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |