
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Лекція 13.
Тема: Ненасичені карбонільні сполуки та кислоти
Зміст
1. Властивості α,β–ненасичених карбонільних сполук, обумовлені їх будовою. Реакції α,β–ненасичених карбонільних сполук із нуклеофілами та магнійорганічними сполуками.
2. Одержання йодзаміщених кетонів, приєднання бромоводню. Відновлення та полімеризація α,β–ненасичених карбонільних сполук.
3. Одержання ненасичених кислот та їх похідних.
4. Відмінності у фізичних властивостях ізомерів етилен-1,2-дикарбонових кислот, обумовлені їх будовою. Хімічні властивості ненасичених кислот.
Ключові слова:
Реакція Міхаеля, реактив Гріньяра.
Цілі та завдання вивчення розділу
Успішне вивчення розділу дозволяє:
Вміти передбачати продукт реакції приєднання до ненасичених карбонільних сполук різних реагентів.
Навчальний матеріал
З курсу органічної хімії згадайте, що таке єноли і чому вони є нестійкими сполуками.
До числа найбільш типових замісників, які активують алкен для нуклеофільної атаки, належить група C=O в таких α,β-ненасичених сполуках, як RCH=CHCHO, RCH=CHCOR', RCH=CHCO2Et і т. п. Оскільки карбонільна група в таких сполуках сама може піддаватися нуклеофільній атаці, стає питання, чи буде переважати приєднання по зв’язку C=C чи C=O або 1,4-приєднання по системі C=C—C=O. Дійсно, останній тип приєднання при використанні, наприклад, реактиву Гріньяра зазвичай веде до того ж продукту, який можна було б одержати при приєднанні за зв’язком C=C, внаслідок таутомерного перетворення єнолу, що утворюється спочатку:
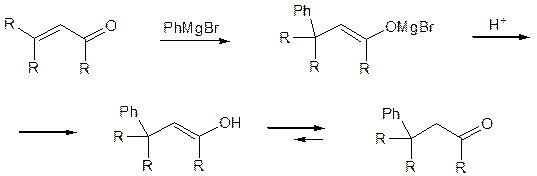
Виділіть основні риси 1,4-приєднання та 1,2-приєднання.
Буде нуклеофільне приєднання проходити переважно як 1,4-приєднання або ж по групі C=O, залежить від того, чи оборотна дана реакція чи ні. Якщо вона оборотна, тоді утворення продукту контролюється термодинамічно (рівноважно) і переважати буде 1,4-приєднання. Це пов’язано з тим, що С–С-аддукт (А), одержаний в ході 1,4-приєднання, термодинамічно більш стійкий, ніж С–О-аддукт (В), оскільки перший містить термінальний π–зв’язок групи C=O, а він сильніше аніж термінальний π–зв’язок групи C=C:

Стеричне утруднення на одній ділянці молекули може сильно активувати приєднання на іншій її ділянці. Наприклад, було показано, що PhCH=CHCHO майже на 100 % приєднує PhMgBr до групи C=O, тоді як у випадку сполуки PhCH=CHCOCMe3 тій же реагент майже на 100 % приєднується до С=С-зв’язку. Це також відображає зниження «карбонільної» активності С=О-групи в ряду альдегід > кетон > ефір, яке веде до зростання частки С=С-приєднання.
Аміни, тіоли, –ОН і т. д. також приєднуються до β–карбонового атома α,β-ненасичених сполук і естерів, але найбільш важливі реакції сполук, які містять угрупування C=C—C=O, — це реакції Михаеля із карбаніонами; в цих реакціях утворюються карбон–карбонові зв’язки. Гарним прикладом є синтез 1,1-диметилцикло-гександіону-3,5 (димедону) (Д) з 2-метилпентен-2-ону-4 (окис мезитилу) (А) і карбаніону –CH(CO2Et)2:
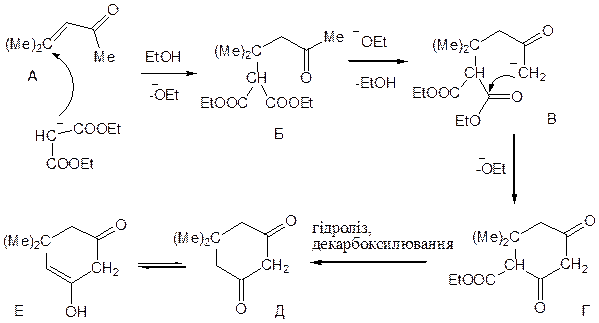
Власне реакція Михаеля завершується утворенням аддукту (Б), але обробка його основою (–OEt) веде до карбаніона (В), який в свою чергу може атакувати карбонільний атом карбону однієї з CO2Et-груп. Оскільки –ОEt — добрий нуклеофуг, то він відходить і внаслідок циклізації утворюється сполука (Г), що нагадує реакцію Дикмана. Гідроліз і декарбоксилювання CO2Et-групи, що залишилась, веде потім до бажаного кінцевого продукту (Д), який на ~ 100 % існує в єнольній формі (Е).
Димедон є цінним реагентом для вибіркової ідентифікації і розділення альдегідів та кетонів, так як він легко утворює похідні А з альдегидами, але не з кетонами. Ця вибірковість, без сумніву, спричинена головним чином стеричними перешкодами.
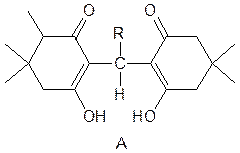
Реакцію, в якій нуклеофіл, що атакує заміщений алкен, є карбаніоном, називають реакцією Міхаеля. Вона є загальним методом утворення карбон-карбонового зв'язку, наприклад:
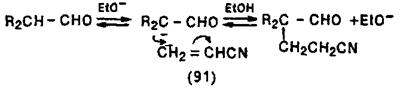
Реакція прискорюється різними основами, які використовуються тільки в каталітичних кількостях, під дією яких генерується карбаніон. Реакція є зворотньою, її швидкістьлімітуючою стадією вважають утворення карбон-карбонового зв'язку, тобто реакцію карбаніону із заміщеним алкеном. У реакції може бути використане велике число різних заміщених алкенів і карбаніонів. Найбільш типові карбаніони — це ті, що утворюються з CH2(CO2Et)2, MeCOCH2CO2Et, NCCH2CO2Et, RCH2NO2 і т.д. В багатьох реакціях Міхаеля як заміщений алкен використовують сполуки, що містять угрупування C=C—C=O.
Що таке каталітична кількість чогось?
Питання для самоконтролю
1. Як контролюється нуклеофільне приєднання до ненасичених кетонів?
Висновки
α,β-Ненасичені карбонільні сполуки та кислоти містять в якості функціональної групи спряжену систему С=С–С=О, яка не є механічним поєднанням подвійного зв’язка і карбонільної групи, а характеризується притаманними тільки їй особливими властивостями.
Читайте також:
- Вид заняття: лекція
- Вид заняття: лекція
- Вид заняття: лекція
- Вид заняття: лекція
- Вид заняття: лекція
- Вступна лекція
- Вступна лекція 1. Методологічні аспекти технічного регулювання у
- Клітинна селекція рослин.
- Колекція фонограм з голосами осіб, які анонімно повідомляли про загрозу вибуху
- ЛЕКЦІЯ (4): Мануфактурний період світової економіки
- Лекція - Геополітика держави на міжнародній арені
- Лекція 02.04.2013
| <== попередня сторінка | | | наступна сторінка ==> |
| Лекція 12. | | | Лекція 14. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |