
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Швидкість хімічних реакцій
Тема 4.3. Хімічні реакції
Лекція № 13
Значення електролізу. Практичне використання електролізу.
Електроліз знаходить досить широке застосування. Для захисту металевих виробів від корозії на їх поверхню наносять дуже тонкий шар іншого металу — хрому,срібла, золота, то тощо. Іноді застосовують багатошарові покриття. Наприклад, зовнішні деталі автомобіля спочатку покривають паром міді, на мідь наносять дуже тонкий шар нікелю а на нього — шар хрому.
Нанесені на метали за допомогою електролізу покриття мають однакову товщину, міцні, довго служать, і, крім того, таким способом можна покривати вироби будь-якої форми. Цю галузь прикладної електрохімії називають гальваностегією. Крім захисту від корозії, гальванічні покриття іноді надають красивого декоративного вигляду предметам.
Інша галузь електрохімії, близька за принципом до гальваностегії, названа гальванопластикою.Це виготовлення точних металевих копій з різних предметів. Предмет, з якого хочуть зняти копію, покривають воском, дають воску затверднути і одержують воскову матрицю, на якій всі заглибини предмета, що копіюється, будуть випуклостями. Внутрішню поверхню матриці покривають тонким шаром графіту, який проводить електричний струм. Цей графітовий катод занурюють у ванну з розчином сульфату купруму, анодом є мідь. Під час електролізу мідний анод розчиняється, а на катоді осаджується мідь. Таким способом виготовляють точну мідну копію предмета. За допомогою гальванопластики виготовляють кліше для друку, грамплатівки, металізують різні предмети. Гальванопластика відкрита російським ученим Б. С. Якобі (1838).
Електроліз використовується для добування багатьох металів — лужних, лужноземельних, алюмінію, лантаноїдів тощо, а також для очищення деяких металів від домішок.
Завдання для самоконтролю:
1. Чи проходять реакції до кінця? Для цих реакцій скласти молекулярно-йонні рівняння:
а) CuSO4+KOH→
б) К2СО3+НNO3→
в) Н2 SO4+Са(ОН)2→
г) Nа2 SO3+ СаСl2→
2. Визначте на основі наведених нижче рівнянь, які реакції є окисно-відновними:
а) Zn+ Н2SO4= Zn SO4+H2
б) ZnSO4 + Nа2 SO3= ZnSO3↓+ Nа2 SO4
в) ZnСl2+ Н2S=Zn S+2HCl
г) Zn+ S= Zn S
д) ZnO+ Н2=Zn+ H2O
е) ZnO+ Н2 SO4=Zn SO4+ H2O
3. Складіть рівняння електролізу розплавів таких сполук: а) NаCl; б) К2S; в) ВаСl.
1. Швидкість хімічних реакцій.
2. Каталіз.
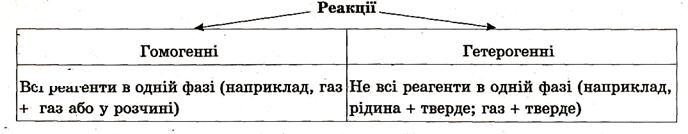
Швидкість реакціївизначається кількістю речовини, що прореагувала в одиниці об'єму за одиницю часу (моль/л∙с).
Швидкість реакції залежить від природи реагуючих речовин і, як правило, зростає:
1) з підвищенням температури;
2) з підвищенням концентрації реагентів;
3) для гетерогенних реакцій - зі зростанням площі поверхні стикання реагентів. Vгомоген= – 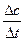 ; Vгетерог=
; Vгетерог=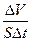 ;
;
Закон дії мас:швидкість хімічної реакції за сталої температури прямо пропорційна добутку концентрацій реагуючих речовин (крім твердої фази).
2А + В → С V = К∙с2(А)∙с(В) або V = К [а]2 ∙ [в]
Правило Вант-Гоффа:з підвищенням температури на кожні 10о швидкість більшості реакцій зростає у 2 — 4 рази (γ-температурний коефіцієнт)
Vt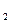 = Vt
= Vt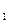 ∙ γ
∙ γ
Суть хімічних реакцій зводиться до розриву зв'язків у вихідних речовинах і виникнення нових зв'язків у продуктах реакції. При цьому загальне число атомів кожного елемента до і після реакції залишається сталим. Оскільки утворення зв'язків відбувається з виділенням, а розрив зв'язків — з поглинанням енергії, то хімічні реакції супроводжуються енергетичними ефектами. Очевидно, що коли зв'язки, які розриваються у вихідних речовинах, слабкіші, ніж ті, що утворюються в продуктах реакції, то енергія виділяється, і навпаки. Звичайно енергія виділяється і поглинається у формі теплоти.
Зі швидкістю реакцій пов'язані уявлення про перетворення речовин, а також економічна ефективність їх добування у промислових масштабах. Учення про швидкість і механізми хімічних реакцій називається хімічною кінетикою.
Читайте також:
- Vу -швидкість ударника
- Будова атомів хімічних елементів.
- Валентність — це здатність атомів одного елемента сполучатися з певним числом атомів інших елементів під час утворення хімічних сполук.
- Видаток і середня швидкість ламінарного потоку.
- Визначення опорних реакцій трьохшарнірної арки
- Визначення реакцій балки
- Визначення реакцій в’язей
- Викривлення реакцій горя
- Вимірювання інформації та швидкість її передачі
- ВЛАСТИВОСТІ ХІМІЧНИХ СИНАПСIВ
- Вплив геохімічних та геофізичних чинників біосфери на здоров’я людини
- Вплив геохімічних чинників біосфери нa здоров'я людини
| <== попередня сторінка | | | наступна сторінка ==> |
| Електроліз. | | | Під швидкістю хімічної реакції розуміють зміну концентрації однієї з реагуючих речовин за одиницю часу за незмінного об'єму системи. |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |