
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Види електрохімічної обробки
Поряд з фізичними ефектами в технології дедалі частіше використовуються позитивні результати, досягнуті в хімії та електрохімії.
До електрохімічної обробки відносять як електроерозійну, так і травлення металів. Ерозійна обробка протікає або шляхом направленого розчинення матеріалу заготовки без контакту її з інструментом, як у випадку свердління, фрезерування, полірування і зачищення, або при контакті їх, як при шліфуванні і хонінгуванні, причому в останньому випадку електрохімічна дія доповнюється механічною. У промисловості застосовують електроерозійне шліфування і зачищення та електрохімічне полірування. У порівнянні зі звичайними способами обробки ці методи дозволяють знімати матеріал незалежно від його механічних властивостей, без зносу інструменту, без розігріву і без виникнення внутрішніх напружень. Продуктивність при цьому може сягати 10 см/хв.
Хоча способи електрохімічного розчинення і не можуть повністю замінити традиційні способи, вони з успіхом доповнюють їх, і в майбутньому сфера їхнього застосування пошириться. Електроерозійну обробку застосовують не тільки для матеріалів, що важко піддаються обробці різанням, але все більше і більше використовують для виготовлення деталей складної форми. Травлення фасонних деталей цілком відповідає вимогам їх мініатюризації і набагато перевищує можливості звичайної штамповки. В майбутньому можна буде говорити і про травлення більш товстих листів.
Електролітичне нагрівання дає змогу за допомогою електричного розряду розігріти тверді провідники (метали, графіт) у струмопровідній рідині (електроліті) до температури порядку 2000 °С. В процесі цього виникає відновне середовище. Спосіб цікавий як для зварювання і пайки, так і для термообробки і особливо для дифузійних процесів, коли в спеціально підібраному електроліті водночас з основним процесом дифундуючий елемент (Мп, С, S, Сг, А1) частково діє на деталі.
Як наймолодший і перспективний спосіб у технології обробки поверхонь треба назвати електрополімеризацією. За цим способом, в основі якого лежать принципи гальванотехніки, можна покрити поверхню металу тонким шаром пластмаси. Особливо важливий він при виготовленні тонких ізоляційних або антикорозійних захисних покриттів на металевих деталях.
Явище анодного розчинення. Електрохімічна обробка (ЕХО) металів заснована на їх здатності розчинятися в результаті окислювальних реакцій, що відбуваються в середовищі електропровідного розчину - електроліту під дією на нього постійного електричного струму. Такий хімічний процес розчинення металів називають електролізом. Електроліз протікає при наявності джерела живлення, електроліту і двох металевих провідників, які називаються електродами, кожен з яких знаходиться в електролітичній ванні з електролітом.
В електроліті вільними електричними зарядами є іони, що утворюються при розчиненні, наприклад, у воді солей, кислот або лугів. Молекули таких речовин, взаємодіючи з молекулами розчинника - води, розпадаються (дисоціюють) на позитивно і негативно заряджені іони. При цьому рух іонів в електроліті невпорядкований. Під дією електричного поля, створюваного джерелом живлення, між електродом, з’єднаним з позитивним полюсом - анодом, і електродом - катодом, з'єднаним з негативним полюсом, виникає спрямований рух іонів - негативно заряджені іони (аніони) рухаються до аноду, а позитивно заряджені іони (катіони) - до катоду.
В електроліті, таким чином, виникає електричний струм, що являє собою впорядкований рух позитивно і негативно заряджених іонів.
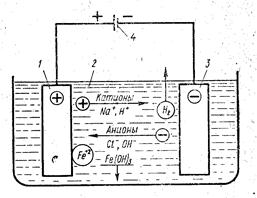
Рисунок 4. 1 – Схема анодного розчинення: 1 - електрод-анод; 2 – електроліт; 3 – електрод-катод; 4 – джерело живлення
Схема руху іонів в найчастіше вживаному для ЕХО електроліті – водному розчині хлористого натрію Nacl (наведено на рис. 4.1. ) при розчиненні хлористого натрію у воді його молекула розпадається на катіон натрію Na+ і аніон хлору Cl–. Вода Н2О при цьому також частково диссоціює на катіони водню Н+ і аніони гидроксила ОН–. При подачі на електроди напруги від джерела живлення аніони гидроксила і катіони водню разом з аніонами хлору і катіонами натрію вимушені під дією сил сил електричного поля переміщуватися відповідно до катоду й аноду.
Атоми поверхневого шару електроду-аноду 1, отримуючи від аніонів хлору і гидроксила, що рухаються до нього, додаткові негативні заряди, перетворюються на позитивні іони заліза. Останні під дією складних катодних і анодних реакцій взаємодіють з іонами гидроксила і утворюють гідрат окислу заліза Fe (OH) 3, який у вигляді нерозчинної хімічної сполуки випадає в осад.
Таким чином відбувається електрохімічне анодне розчинення заліза. Одночасно з цим на катоді виділяється водень, що виходить з електроліту у вигляді бульбашок. Реакції, що протікають на катоді як правило, не руйнують його, тобто катод при ЕХО не зношується.
Параметри анодного розчинення. Електроліз протікає в міжелектродному проміжку, під яким прийнято розуміти простір між поверхнями катода і анода. Отже, електрохімічне анодне розчинення відбувається без безпосереднього механічного контакту поверхонь катода і анода.
Відповідно до першого закону Фарадея об'єм V розчиненого металу при електролізі прямо пропорційний об'ємному електрохімічному еквіваленту k цього металу, силі струму I і часу t
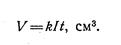 (4.1)
(4.1)
Об'ємний електрохімічний еквівалент k металу залежить від його валентності і атомної маси. На практиці об'єм розчиненого металу не завжди відповідає величині, розрахованій за цим рівнянням. Так, об'єм розчиненого металу істотно залежить від густини струму на аноді, що визначається відношенням сили струму I до площі S анода
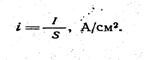 (4.2)
(4.2)
При певному поєднанні параметрів процесу - густини струму, виду оброблюваного металу, складу і швидкості оновлення електроліту в міжелектродному просторі - об'єм V розчиненого металу відносно розрахункового його значення може зменшуватися, а в деяких випадках процес анодного розчинення повністю припиняється. Це пояснюється утворенням на поверхнях анода важкорозчинних окисних плівок, які часто називають пасивними.
За наявності в електроліті достатньої кількості активуючих аніонів, наприклад аніонів хлору Cl¯, відбувається витіснення з окисної плівки кисню і руйнування її без додаткових витрат електричної енергії. У таких процесах, що називаються активними, електрична енергія витрачається безпосередньо на електрохімічне розчинення металу анода. Якщо в електроліті бракує активуючих аніонів, то на електрохімічне анодне розчинення цих плівок витрачається додаткова електрична енергія. При цьому ефективність процесів ЕХО істотно знижується. Такий процес електрохімічного анодного розчинення металу називають пасивним.
Активне анодне розчинення відрізняється від пасивного особливостями реакцій, що відбуваються на аноді. Активне розчинення характеризується високою розчинністю металу анода, оскільки при цьому побічні реакції, окрім основної - анодного розчинення, не протікають. Активне розчинення металу відбувається, наприклад, при електрохімічному травленні. При пасивному розчиненні частина електричної енергії витрачається на побічні реакції, що забезпечують видалення з поверхонь анода важкорозчинних окисних плівок. Пасивне розчинення металу відбувається, наприклад, при електрохімічному поліруванні.
Підвищення густини струму відносно оптимального його значення може привести за певних умов до утворення окисних плівок складного складу, які не розчиняються при електролізі. При цьому настає повна пасивація, тобто перехід поверхневого шару металу з активного стану в пасивний, при якому процес анодного розчинення припиняється. Подібні плівки видаляють з поверхонь анода механічно, наприклад абразивною обробкою.
Ефективність процесів ЕХО оцінюють так званим коефіцієнтом виходу металу за струмом, який визначають за формулою
η = Vф / V, (4.3)
де Vф – фактичний об’єм розчиненого металу при пропусканні певної кількості електрики, см3; V – розрахунковий об’єм металу, який повинен розчинитися при пропусканні тої же самої кількості електрики, см3.
З урахуванням коефіцієнта η рівняння, що характеризує об'єм розчиненого металу, набуває наступного вигляду
Vф = kIt, см3. (4.4)
Об’єм Vф, як правило, завжди менше розрахункового V, тобто η<1. Значення цього коефіцієнта η відображає характер анодного розчинення: активне і пасивне. При активному розчиненні коефіцієнт виходу металу за струмом складає зазвичай 0,5-1,0; при пасивному розчиненні - η<0,5.
Електрохімічна обробка. Електрохімічна обробка заснована на законах анодного розчинення металів при електролізі. При проходженні електричного струму через електроліт на поверхні заготовки відбуваються хімічні реакції, і поверхневий шар металу перетворюється в хімічну сполуку. Продукти електролізу переходять у розчин або видаляються механічним способом. Продуктивність цього способу залежить від електрохімічних властивостей електроліту, оброблюваного матеріалу і густини струму.
Електрохімічне полірування. Електрохімічне полірування здійснюється у ванні, заповненої електролітом (розчини кислот і лугів). Оброблювану заготівлю підключають до катода (рис. 4.2). Катодом служить металева пластинка зі свинцю, міді, сталі (іноді електроліт підігрівають).
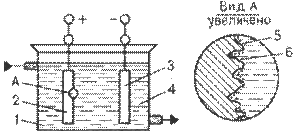
Рисунок 4.2. - Схема електрохімічного полірування: 1 - ванна; 2 - оброблювана заготовка; 3 - пластина-електрод; 4 - електроліт; 5 - мікровиступи; 6 - продукти анодного розчинення
При подачі напруги починається процес розчинення металу заготівлі (в основному на виступах мікронерівностей). В результаті вибіркового розчинення, мікронерівності згладжуються, і оброблювана поверхня набуває металевий блиск. Поліпшуються електрофізичні характеристики деталей: зменшується глибина мікротріщин, поверхневий шар не деформується, не допускаються термічні зміни структури, підвищується корозійна стійкість.
Цим методом отримують поверхні під гальванічні покриття, доводять робочі поверхні різального інструменту, виготовляють тонкі стрічки і фольгу, очищають і декоративно обробляють деталі.
Електрохімічна розмірна обробка. Електрохімічна розмірна обробка виконується в струмені електроліту, прокачуваного під тиском через міжелектродний простір. Електроліт розчиняє утворювані на поверхні заготівлі - анода солі і видаляє їх із зони обробки. Висока продуктивність процесу полягає в тому, що одночасно обробляється вся поверхня заготівлі. Ділянки, що не вимагають обробки, ізолюють. Інструменту надають форму, зворотну формі оброблюваної поверхні. Формоутворення відбувається за методом копіювання (рис. 4.3).

Рисунок 4.3 - Схема електрохімічної розмірної обробки: 1 - інструмент - катод; 2 - заготівля - анод
Точність обробки підвищується при зменшенні робочого зазору. Для його контролю використовують високочутливі елементи, які вбудовують в слідкуючу систему.
Цей спосіб рекомендують для обробки заготівель з високоміцних сталей, карбідних і важкооброблюваних матеріалів. Також можна обробляти тонкостінні деталі з високою точністю і якістю обробленої поверхні (відсутній тиск інструменту на заготівку).
Комбіновані методи обробки.
Електроабразівная і електроалмазная обробка. При таких видах обробки інструментом служить шліфувальний круг з абразивного матеріалу на електропровідний зв'язці (бакелітова зв'язка з графітовим наповнювачем). Між анодом - заготівлею та катодом - шліфувальним кругом є зазор, куди подають електроліт. Продукти анодного розчинення видаляються абразивними зернами; шліфувальний круг має обертальний рух, а заготовка - рух подачі, які відповідають процесу механічного шліфування (рис. 4.4).

Рисунок 4.4 - Схема електроабразівного шліфування: 1 - заготівля; 2 - абразивні зерна; 3 - зв'язка шліфувального круга
Введення в зону різання ультразвукових коливань підвищує продуктивність в 2 - 2,5 рази при поліпшенні якості поверхні. Ці методи застосовують для оздоблювальної обробки заготовок з важкооброблюваних матеріалів, а також нежорстких заготовок, так як сили різання незначні.
Анодно-механічна обробка. Анодно-механічна обробка заснована на поєднанні електротермічних та електромеханічних процесів і займає проміжне місце між електроерозійним і електрохімічним методами. Заготівлю підключають до анода, а інструмент - до катода. Як інструмент використовують металеві диски, циліндри, стрічки, дріт. Обробку ведуть у середовищі електроліту (водний розчин рідкого натрієвого скла). Робочі рухи такі ж, як при механічній обробці різанням.
Електроліт в зону обробки подають через сопло (рис. 4.5)
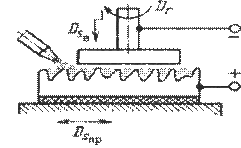
Рисунок 4.5. - Схема анодно-механічної обробки плоскої поверхні
При пропущенні через розчин електроліту постійного електричного струму відбувається процес анодного розчинення, як при електрохімічній обробці.
При зіткненні інструмента з мікронерівностями заготівлі відбувається електроерозія, притаманна електроіскровий обробці. Метал заготівлі в місці контакту з інструментом розігрівається і розріджується. Продукти електроерозіі і анодного розчинення видаляються при відносних рухах інструменту і заготівлі. Цим способом обробляють заготівлі з високоміцних і важкооброблюваних сплавів, в'язких матеріалів.
Цим способом розрізають заготівлі на частини, прорізають пази і щілини, обробляють поверхні тіл обертання, шліфують плоскі поверхні і поверхні, що мають форму тіл обертання, полірують поверхні, заточують різальний інструмент.
Читайте також:
- Автомобільний комплект для спеціальної обробки військової техніки ДК-4К
- Алгоритм проведення санобробки при зараженні БЗ
- Аналіз умов технічної експлуатації територіально розподілених ПФС екстремальної комп’ютерно-інтегрованої системи керування технологічними процесами обробки даних
- Бази даних як засіб зберігання й обробки інформації
- В умовах автоматизованої обробки даних
- Вибір режимів обробки заготовки різанням
- Вивчення структури сталей після різних видів термічної обробки
- Виготовлення до обробки яєць
- Види слюсарно-механічної обробки
- Визначення комплексних показників якості за варіантами обробки
- Визначення послідовності обробки поверхонь заготовки
| <== попередня сторінка | | | наступна сторінка ==> |
| Завдання на практичне заняття | | | Електроліти для електрохімічної обробки |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |