
РЕЗОЛЮЦІЯ: Громадського обговорення навчальної програми статевого виховання
ЧОМУ ФОНД ОЛЕНИ ПІНЧУК І МОЗ УКРАЇНИ ПРОПАГУЮТЬ "СЕКСУАЛЬНІ УРОКИ"
ЕКЗИСТЕНЦІЙНО-ПСИХОЛОГІЧНІ ОСНОВИ ПОРУШЕННЯ СТАТЕВОЇ ІДЕНТИЧНОСТІ ПІДЛІТКІВ
Батьківський, громадянський рух в Україні закликає МОН зупинити тотальну сексуалізацію дітей і підлітків
Відкрите звернення Міністру освіти й науки України - Гриневич Лілії Михайлівні
Представництво українського жіноцтва в ООН: низький рівень культури спілкування в соціальних мережах
Гендерна антидискримінаційна експертиза може зробити нас моральними рабами
ЛІВИЙ МАРКСИЗМ У НОВИХ ПІДРУЧНИКАХ ДЛЯ ШКОЛЯРІВ
ВІДКРИТА ЗАЯВА на підтримку позиції Ганни Турчинової та права кожної людини на свободу думки, світогляду та вираження поглядів
- Гідрологія і Гідрометрія
- Господарське право
- Економіка будівництва
- Економіка природокористування
- Економічна теорія
- Земельне право
- Історія України
- Кримінально виконавче право
- Медична радіологія
- Методи аналізу
- Міжнародне приватне право
- Міжнародний маркетинг
- Основи екології
- Предмет Політологія
- Соціальне страхування
- Технічні засоби організації дорожнього руху
- Товарознавство продовольчих товарів
Тлумачний словник
Авто
Автоматизація
Архітектура
Астрономія
Аудит
Біологія
Будівництво
Бухгалтерія
Винахідництво
Виробництво
Військова справа
Генетика
Географія
Геологія
Господарство
Держава
Дім
Екологія
Економетрика
Економіка
Електроніка
Журналістика та ЗМІ
Зв'язок
Іноземні мови
Інформатика
Історія
Комп'ютери
Креслення
Кулінарія
Культура
Лексикологія
Література
Логіка
Маркетинг
Математика
Машинобудування
Медицина
Менеджмент
Метали і Зварювання
Механіка
Мистецтво
Музика
Населення
Освіта
Охорона безпеки життя
Охорона Праці
Педагогіка
Політика
Право
Програмування
Промисловість
Психологія
Радіо
Регилия
Соціологія
Спорт
Стандартизація
Технології
Торгівля
Туризм
Фізика
Фізіологія
Філософія
Фінанси
Хімія
Юриспунденкция
Міцелярна теорія будови колоїдних частинок
Електричний заряд колоїдних частинок і електрокінетичні явища
Міцелярна теорія будови колоїдних частинок
ЕЛЕКТРИЧНИЙ ЗАРЯД КОЛОЇДНИХ ЧАСТИНОК І ЕЛЕКТРОКІНЕТИЧНІ ЯВИЩА
3 СТІЙКІСТЬ І КОАГУЛЯЦІЯ ДИСПЕРСНИХ СИСТЕМ
Частинки дисперсної фази ліофобних золів мають складну структуру, що залежить від умов їх одержання. Оскільки у самих частинок досить великі розміри (це скупчення великої кількості молекул або частинок, які часто мають кристалічну будову), то вони здатні адсорбувати на своїй поверхні речовини, які присутні у розчині (інтерміцелярній рідині або дисперсійному середовищі). Найважливішим з процесів адсорбції на поверхні твердих частинок (дисперсної фази) є адсорбція заряджених частинок (йонів) із розчину, оскільки такий процес має великий вплив на стабільність утвореної системи.
Колоїдні системи одержують шляхом подрібнення або агрегації слаборозчинних у воді сполук і навіть металів.
Тому в дисперсійному середовищі містяться різні незаряджені (молекули розчинених газів, органічних сполук) і заряджені частинки (йони), які можуть адсорбуватись на твердій поверхні. Адсорбція заряджених частинок може відбуватись навіть у тому випадку, якщо в дисперсійне середовище (наприклад, воду) попередньо не було додано електроліту: йони можуть утворюватись за рахунок часткового переходу металу на розчин чи дисоціації малорозчинних солей. Саме такі процеси відбуваються при утворенні колоїдів у ґрунтах, мінеральних водах тощо.
Але найчастіше надлишок електроліту додається у розчин при приготуванні колоїдів для їх стабілізації. На основі вивчення електрокінетичних явищ у колоїдних системах було виявлено, що на поверхні колоїдних частинок на межі розділу фаз утворюється так званий подвійний електричний шар(ПЕШ) і виникає стрибок потенціалу. Це обумовлено тим, що йони одного знака необмінно адсорбуються (поглинаються) на поверхні (твердої частинки), а йони протилежного знаку за рахунок електростатичного притягання розташовуються біля них. При цьому величина і знак заряду поверхні залежать від природи твердих частинок і від природи рідини, в якій вони знаходяться.
Розглянемо будову гідрофобної колоїдної частинки на прикладі утворення золю AgI обмінною реакцією
АgNO3 + KI à AgI¯ + KNO3.
Якщо речовини беруться в еквівалентних кількостях, то випадає кристалічний осад AgI. Але, якщо одна з вихідних речовин буде у надлишку , наприклад КІ, процес кристалізації AgI веде до утворення колоїдного розчину – міцели AgI.
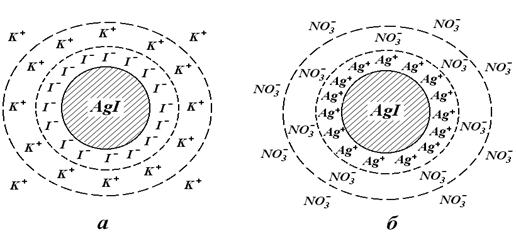
Будова міцели гідрозолю AgI схематично зображена на рис.3. Агрегат молекул [nAgI] кількістю 100-1000 (мікрокристал, ядро) є зародком нової фази, на поверхні якого відбувається адсорбція іонів електроліту, які знаходяться в дисперсійному середовищі.
Згідно з правилом Панета-Фаянса краще адсорбуються іони, однакові з іонами, які входять до кристалічної решітки ядра і добудовують цю решітку. Іони, адсорбо-вані безпосередньо на ядрі, яке не розчиняється в даному дисперсійному середовищі, називаються потенціалвизна-чаючими, тому що вони визначають величину потенціалу та знак заряду поверхні, а також і знак заряду всієї частинки.
Потенціалвизначаючими іонами в даній системі є іони І-, які знаходяться в надлишку, входять до складу кристалічної решітки ядра AgI, виконують роль стабілі-заторів і складають внутрішню оболонку у жорсткій частині подвійного електричного шару (ПЕШ) міцели.
Агрегат з адсорбованими на ньому іонами І- утворює ядро міцели.
До негативно зарядженої поверхні часток AgI на відстані, близькому до радіуса гідратованого іона, з розчину притягуються іони протилежного знаку (протиіони) – позитивно заряджені іони К+. Шар протиіонів – зовнішня обгортка подвійного електричного шару (ПЕШ), утримується як електростатичними силами, так і силами адсорбційного притягання.
Агрегат молекул разом з твердим подвійним шаром називається колоїдною частинкою.
Частина протиіонів внаслідок теплового руху розміщується дифузно углиб розчину, і притягання їх здійснюється тільки за рахунок електростатичних сил. Колоїдні частинки разом з оточуючим її дифузним шаром називається міцелою. Міцела електронейтральна, тому що заряд ядра дорівнює зарядові всіх проти іонів, а частинка звичайно має заряд, який називається електрокінетичним, або x-дзета-потенціалом.
AgNO3 + KI = AgI¯ + KNO3


 {[nAgI]mI- (m-x)K+}-x xK+
{[nAgI]mI- (m-x)K+}-x xK+
 Ядро Адсорбцій-
Ядро Адсорбцій-

 ний шар Дифуз-
ний шар Дифуз-
 ний шар
ний шар
 Гранула
Гранула
Міцела
 |
Рисунок 3 – Будова міцели AgI
Будову міцели можна подати такою формулою:
 |
{[nAgI]mI- (m-x)K+}-x xK+
Ядро Тверда Дифуз-
частина ПЕШ
на час-
тина ПЕШ
Частинка
Читайте також:
- E) теорія раціонального вибору.
- I. Теорія граничної продуктивності і попит на ресурси
- V теорія граничної корисності визначає вартість товарів ступенем корисності останньої одиниці товару для споживача.
- Агрегативна стійкість і коагуляція колоїдних розчинів
- Аксіоматичний метод у математиці та суть аксіоматичної побудови теорії.
- Алгоритм побудови сітьових графіків.
- Алгоритми побудови дерев екстремальної ваги
- Атомарний рівень будови речовини
- Балансова теорія визначення статі. Диференціація статі і роль гормонів у цьому процесі.
- Банківська система: сутність, принципи побудови та функції. особливості побудови банківської системи в Україн
- Банківська система: сутність, принципи побудови та функції. Особливості побудови банківської системи в Україні.
- Банківська система: сутність, принципи побудови та функції. Особливості побудови банківської системи в Україні.
| <== попередня сторінка | | | наступна сторінка ==> |
| Класифікація колоїдно-дисперсних систем за агрегатним станом | | | Методические указания |
|
Не знайшли потрібну інформацію? Скористайтесь пошуком google: |
© studopedia.com.ua При використанні або копіюванні матеріалів пряме посилання на сайт обов'язкове. |